23-24高三下·四川成都·开学考试
名校
解题方法
1 . 葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过如下实验流程制得:
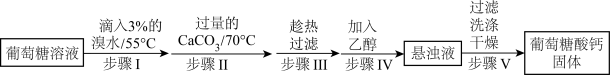
已知:a.反应原理: 。
。
b.相关物质的溶解性如下表:
c.相关物质的酸性:氢溴酸>葡萄糖酸>碳酸。
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是___________ ,恒压滴液漏斗使用时需要打开的活塞或玻璃塞是___________ (填“a”“b”或“a和b”)。烧杯中 溶液水浴的作用是
溶液水浴的作用是___________ 。
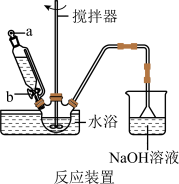
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
(3)步骤Ⅱ中加入过量的 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为___________ 。加入过量的 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)洗涤操作中最合适的洗涤剂是___________ (填序号),理由是___________ 。
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:___________ (填序号,操作步骤不可重复使用)。
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出
④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液

已知:a.反应原理:
 。
。b.相关物质的溶解性如下表:
| 物质的名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是
 溶液水浴的作用是
溶液水浴的作用是
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
A.新制 悬浊液 悬浊液 | B.酸性 溶液 溶液 |
C. /葡萄糖氧化酶 /葡萄糖氧化酶 | D. 溶液 溶液 |
(3)步骤Ⅱ中加入过量的
 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是(4)洗涤操作中最合适的洗涤剂是
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入
 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入
 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
您最近一年使用:0次
2023·辽宁·高考真题
2 . 某工厂采用如下工艺制备 ,已知焙烧后
,已知焙烧后 元素以
元素以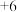 价形式存在,下列说法错误的是
价形式存在,下列说法错误的是
 ,已知焙烧后
,已知焙烧后 元素以
元素以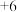 价形式存在,下列说法错误的是
价形式存在,下列说法错误的是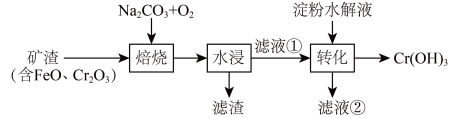
A.“焙烧”中产生 | B.滤渣的主要成分为 |
C.滤液①中 元素的主要存在形式为 元素的主要存在形式为 | D.淀粉水解液中的葡萄糖起还原作用 |
您最近一年使用:0次
2023-06-13更新
|
10454次组卷
|
21卷引用:第四章 生物大分子(B卷)
(已下线)第四章 生物大分子(B卷)2023年高考辽宁卷化学真题(已下线)T10-物质反应及转化(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)陕西省汉中中学2024届高三上学期8月质量检测化学试题陕西省渭南市2023-2024学年高三上学期期中检测化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河北省迁安市2023-2024学年高三上学期期中考试化学试题(已下线)第3讲 物质制备实验的设计与评价黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)陕西省西安市长安区第一中学2023-2024学年高三上学期第二次教学质量检测化学试题河北省保定市蠡县中学2023-2024学年高二上学期化学月考试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题福建泉州科技中学2022-2023学年高二下学期期末考化学试题(已下线)FHgkyldyjhx03福建省厦门第一中学2023-2024学年高三下学期5月第2次月考化学试卷
3 . 氮循环是海洋生态系统的基础和关键,其中无机氮循环过程如下图所示。
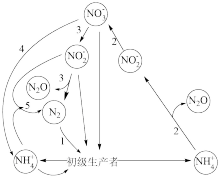
亚硝酸盐是氮循环中的重要物质。下列关于亚硝酸钠 性质的推测中,
性质的推测中,不合理 的是资料: 为弱酸,
为弱酸, 在碱性条件下能稳定存在。
在碱性条件下能稳定存在。

亚硝酸盐是氮循环中的重要物质。下列关于亚硝酸钠
 性质的推测中,
性质的推测中, 为弱酸,
为弱酸, 在碱性条件下能稳定存在。
在碱性条件下能稳定存在。A. 具有氧化性 具有氧化性 | B. 具有还原性 具有还原性 |
C. 能与 能与 反应 反应 | D. 能与 能与 反应 反应 |
您最近一年使用:0次
2023-01-05更新
|
809次组卷
|
6卷引用:章末检测卷(三) 物质的性质与转化
名校
解题方法
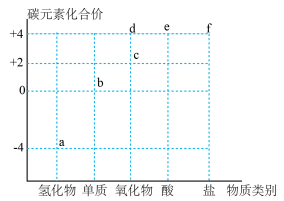
4 . 下图是碳及其化合物的“价一类”二维图,f为 、
、 。下列说法正确的是
。下列说法正确的是
 、
、 。下列说法正确的是
。下列说法正确的是
| A.a只能被氧化,c是酸性氧化物 | B.d的水溶液能导电,d属于电解质 |
| C.d→f的转化一定不是氧化还原反应 | D.向 饱和溶液中通入d有沉淀析出 饱和溶液中通入d有沉淀析出 |
您最近一年使用:0次
21-22高一下·江苏淮安·阶段练习
解题方法
5 . 下图所示的氮循环是生态系统物质循环的重要组成部分。___________ 。
(2)下列说法中错误的是___________(填字母)。
(3)氮循环过程中发生的反应之一可表示为 + 2O2
+ 2O2
 +2H+ +H2O,该反应中每生成1mol
+2H+ +H2O,该反应中每生成1mol  转移的电子数目是
转移的电子数目是___________ 、还原剂是___________ 、在标准状况下消耗的氧气体积为 ___________ 。
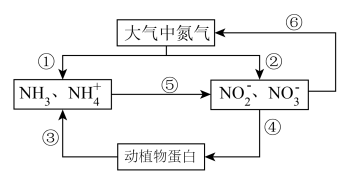
(2)下列说法中错误的是___________(填字母)。
| A.图中①和②的转化过程属于氮的固定 |
| B.③和④的转化说明含氮有机物和含氮无机物可以相互转化 |
| C.发生⑤转化的过程中,氮元素被氧化 |
| D.⑥是在反硝化细菌作用下的反硝化过程,该过程无助于弥补人工固氮对氮循环造成的影响 |
(3)氮循环过程中发生的反应之一可表示为
 + 2O2
+ 2O2
 +2H+ +H2O,该反应中每生成1mol
+2H+ +H2O,该反应中每生成1mol  转移的电子数目是
转移的电子数目是
您最近一年使用:0次
2022高三·全国·专题练习
6 . 在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是
| A.反应转移电子为0.1mol | B.HCl溶液中 数为3NA 数为3NA |
C.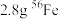 含有的中子数为1.3NA 含有的中子数为1.3NA | D.反应生成标准状况下气体3.36L |
您最近一年使用:0次
2022-07-04更新
|
7965次组卷
|
18卷引用:【知识图鉴】单元讲练测必修第一册第三单元03巩固练
(已下线)【知识图鉴】单元讲练测必修第一册第三单元03巩固练(已下线)专题02 化学计量与化学计算-2022年高考真题模拟题分项汇编2022年海南省高考真题化学试题(已下线)2022年海南省高考真题变式题1-14(已下线)第04讲 物质的量 气体摩尔体积 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖北省华中师范大学第一附属中学2022-2023学年高一上学期新生入学测试化学试题(已下线)易错点04 氧化还原反应-备战2023年高考化学考试易错题(已下线)专题02 阿伏加德罗常数及其化学计算 (讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题2 “阿伏加德罗常数”的应用河北省保定市2022-2023学年高一上学期期末调研考试化学试题(已下线)回归教材重难点03 “NA”应用再思考-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)题型4 阿伏伽德罗常数的综合应用-高考必备50个题型(已下线)考点08 物质的量在化学方程式计算中的应用(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点03 物质的量浓度及溶液配制(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题03 化学计量-2023年高考化学真题题源解密(全国通用)(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)江西省宜春市百树学校2023-2024学年高三上学期11月期中考试化学试卷
2022·浙江·高考真题
7 . 下列说法正确的是
| A.工业上通过电解六水合氯化镁制取金属镁 |
| B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫 |
| C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸 |
| D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用 |
您最近一年使用:0次
2022-06-14更新
|
8119次组卷
|
21卷引用:【知识图鉴】单元讲练测必修第二册第五单元 03巩固练
(已下线)【知识图鉴】单元讲练测必修第二册第五单元 03巩固练2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题1-10(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)河南省濮阳市第一高级中学2022-2023学年高三上学期第一次月考化学试题湖南省怀化市沅陵县第一中学2022-2023学年高三上学期第一次阶段性考试化学试题浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题河南省洛阳市新安县第一高级中学2022-2023学年高三上学期9月阶段性考试化学试题浙江省杭州市2022-2023学年高三上学期第一次适应性考试化学试题安徽省六安市裕安区新安中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题08 元素及其化合物(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题卷08 无机物的性质与用途-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)查补易混易错01 元素化合物部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题05 元素化合物性质(已下线)专题05 元素化合物性质(已下线)考点11 镁、铝及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)陕西省西北工业大学附属中学2022-2023学年高一下学期期末考试化学试题上海市曹杨第二中学2023-2024学年高三上学期期中考试化学试题2024届河北省实验中学高三年级上学期第一次月考化学试题
21-22高一下·陕西汉中·期中
名校
8 . “84”消毒液(有效成分为NaClO)、洁厕液(主要成分为HCl)是生活中常见的消毒剂、清洁用品,二者混合使用会产生毒气(Cl2)。从氧化还原的角度推测,下列关于Cl2性质的猜想正确的是
| A.只有氧化性 | B.只有还原性 |
| C.既有氧化性又有还原性 | D.无法判断 |
您最近一年使用:0次
2022-05-05更新
|
1392次组卷
|
6卷引用:第一章 物质及其变化(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第一章 物质及其变化(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)陕西省汉中市镇巴县2021-2022学年高一下学期期中考试化学试题(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )黑龙江省鹤岗市第一中学2022-2023学年高一上学期10月月考化学试题课时2 氧化剂和还原剂
21-22高一下·山东日照·期中
9 . 碘是人体生长发育不可缺少的微量元素,海带中富含碘元素,从海带中提取碘的工艺流程如下。回答下列问题:

(1)步骤①中发生反应的离子方程式为_______ ,当生成0.3molI2时,转移电子的物质的量为_______ mol。
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为_______ 。
(3)步骤③中发生反应的化学方程式为_______ 。
(4)步骤⑤的实验操作名称为_______ 。
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为_______ 法。

(1)步骤①中发生反应的离子方程式为
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为
(3)步骤③中发生反应的化学方程式为
(4)步骤⑤的实验操作名称为
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
您最近一年使用:0次
21-22高一下·上海杨浦·期中
名校
10 . 氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的关键环节。
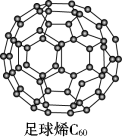
I.C60可用作储存氢气的材料,结构如下图所示。
(1)继C60后,科学家合成了Si60、N60,三者结构相似。下列说法正确的是_______(填序号)
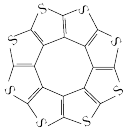
II.最近科学家对一种新型储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如下图所示),每个平面小上下最多可吸附10个H2分子。
(2)C16S8与H2间以_______ (填微粒间作用力类型)结合。
(3)C16S8中C-S键的共用电子对偏向于S,举出一个事实,说明硫的非金属性比碳强(用化学方程式表示):_______ 。
III.LiBH4是储氢材料,已知其由Li+和BH 构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
(4)锂位于元素周期表的_______ 。
(5)由元素周期律能得到_______。(填序号)。
(6)LiBH4中不存在的作用力有_______(填序号)。
(7)氢化锂(LiH)是离子化合物,写出其电子式_______ ,LiH中负离子半径大于正离子半径,其原因是_______ 。
(8)若该反应中释放67.2LH2(标况下),则转移的电子数为_______ 个。
I.C60可用作储存氢气的材料,结构如下图所示。

(1)继C60后,科学家合成了Si60、N60,三者结构相似。下列说法正确的是_______(填序号)
| A.C60、Si60、N60都属于共价晶体 |
| B.C60、Si60、N60分子内共用电子对数目相同 |
| C.由于N-N键能小于N≡N,故N60的稳定性弱于N2 |
| D.由于C-C键长小于Si-Si键,所以C60熔沸点低于Si60 |
II.最近科学家对一种新型储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如下图所示),每个平面小上下最多可吸附10个H2分子。

(2)C16S8与H2间以
(3)C16S8中C-S键的共用电子对偏向于S,举出一个事实,说明硫的非金属性比碳强(用化学方程式表示):
III.LiBH4是储氢材料,已知其由Li+和BH
 构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。
构成,LiBH4释放氢气的原理为2LiBH4→2LiH+2B+3H2↑。(4)锂位于元素周期表的
(5)由元素周期律能得到_______。(填序号)。
| A.碱性:LiOH<NaOH | B.与水反应的剧烈程度:Li<Na |
| C.溶解度:LiOH<NaOH | D.密度:Li<Na |
| A.离子键 | B.共价键 | C.金属键 | D.分子间作用力 |
(8)若该反应中释放67.2LH2(标况下),则转移的电子数为
您最近一年使用:0次



