名校
1 . 84消毒液是常用的消毒剂之一,下列有关84消毒液的说法正确的是
A.基态Cl原子的价电子排布式为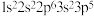 |
B.向该溶液中加入浓盐酸,每产生1 mol ,转移的电子数约为 ,转移的电子数约为 |
C.向该溶液中滴入少量 溶液,反应的离子方程式为 溶液,反应的离子方程式为 |
D.该溶液中, 、 、 、 、 , , 可以大量共存 可以大量共存 |
您最近一年使用:0次
2 . 二氧化铈(CeO2)作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO2,并引起氧空位的形成,得到新的铈氧化物[Cex(Ⅲ)Cey(Ⅳ)Oz]。当二氧化铈晶胞发生如下图变化时,有关说法错误的是
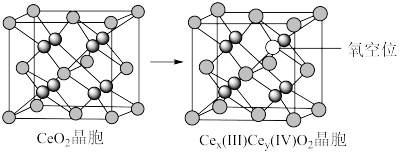
| A.铈位于氧原子形成的八面体空隙中 |
| B.生成新的铈氧化物中x、y、z的最简整数比为2:2:7,当1 mol CeO2发生变化时,可吸收标况下NO的体积为5.6 L |
C.晶胞的俯视图为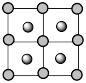 |
D.若晶胞边长为a pm,则CeO2晶体的密度为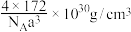 (NA表示阿伏加德罗常数的值) (NA表示阿伏加德罗常数的值) |
您最近一年使用:0次
3 . 稀有气体氙的氟化物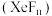 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:
下列说法正确的是
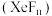 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:| 与水反应 | 与 溶液反应 溶液反应 |
i.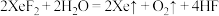 | ii.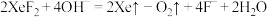 |
iii. | Ⅳ.  |
A. 具有平面三角形结构 具有平面三角形结构 | B. 的还原性比 的还原性比 强 强 |
C.反应 均为氧化还原反应 均为氧化还原反应 | D.反应iv每生成 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
名校
解题方法
4 . 某课题组利用工业废气中的NO制备NH4NO3的工艺流程如图所示,若装置Ⅰ和装置Ⅱ中反应后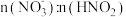 都为
都为 (不考虑HNO2电离),下列说法错误的是
(不考虑HNO2电离),下列说法错误的是
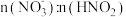 都为
都为 (不考虑HNO2电离),下列说法错误的是
(不考虑HNO2电离),下列说法错误的是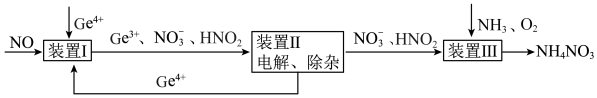
A.装置Ⅰ中反应的离子方程式为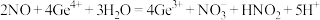 |
| B.装置Ⅰ中若有5.6L(标准状况下)NO参与反应,则转移0.5mol电子 |
C.装置Ⅲ中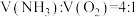 ,可实现原子利用率最大化 ,可实现原子利用率最大化 |
D.装置Ⅲ发生的氧化还原反应中氧化剂和还原剂物质的量之比为 |
您最近一年使用:0次
5 . Romanenko利用微生物电池将 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是
 针催化还原的工作原理如图所示,下列说法正确的是
针催化还原的工作原理如图所示,下列说法正确的是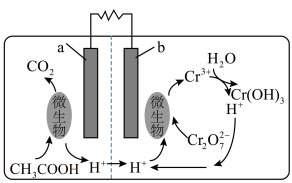
| A.b极电势比a极电势低 |
B.a极反应式: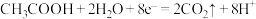 |
C.每处理1mol ,至少消耗 ,至少消耗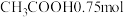 |
D.每生成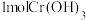 ,左池 ,左池 增加4mol 增加4mol |
您最近一年使用:0次
6 . 已知:
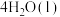
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是

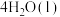
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是A.0.1  溶液中含有NA个K+ 溶液中含有NA个K+ |
B.1mol  参与反应断裂的π键数目为NA 参与反应断裂的π键数目为NA |
C.反应每放出m kJ的热量,生成NA个 分子 分子 |
| D.每转移10NA个电子,产生CO2的体积标况下约为44.8L |
您最近一年使用:0次
名校
解题方法
7 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是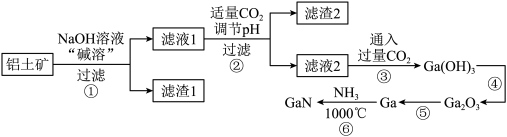
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知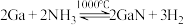 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为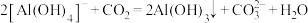 |
您最近一年使用:0次
2024-05-12更新
|
230次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
8 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为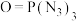 ,其分解产物 ,其分解产物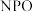 的电子式为 的电子式为 |
您最近一年使用:0次
2024-05-12更新
|
111次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
9 . 为测定Cu和Cu2O混合粉末中Cu的含量。某同学将44.8g Cu和Cu2O混合粉末加入500mL 4.5mol/L的稀硝酸中,得到6.72LNO(标准状况下),忽略溶液体积的变化。下列说法正确的是
| A.反应后有固体剩余 | B.混合粉末中Cu的质量分数约为37% |
| C.反应后的溶液中c(Cu2+)=1.2mol/L | D.在反应后的溶液中加入足量铁粉,可置换出41.6g Cu |
您最近一年使用:0次
10 . 在微生物作用下电解有机废水 含
含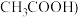 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
 含
含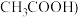 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
A.电极 极为负极 极为负极 |
B.与电源 极相连的惰性电极上发生的反应为: 极相连的惰性电极上发生的反应为: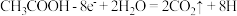  |
C.通电后,  通过质子交换膜向右移动。若导线中转移 通过质子交换膜向右移动。若导线中转移  电子,左侧溶液质量减轻 电子,左侧溶液质量减轻 |
D.通电后,若有   生成,则转移 生成,则转移  电子 电子 |
您最近一年使用:0次



