名校
解题方法
1 . 草酸是化工上常用的还原剂,实验中可以用浓硝酸在Hg(NO3)2催化氧化C2H2气体来制备,可能用到的仪器如图所示。
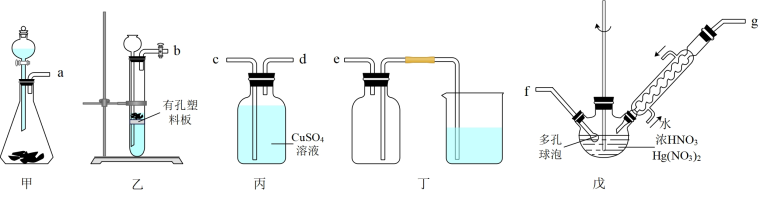
已知电石(主要成分为CaC2,含少量CaS和Ca3P2等杂质)遇水可以迅速生成C2H2,CuSO4溶液能够吸收H2S、PH3气体,浓硝酸氧化C2H2时会被还原为NO2.问答下列问题:
(1)CaC2与H2O反应制备C2H2的化学反应方程式为_______ 。
(2)选择所需的仪器,接口正确的连接顺序为_______ →e。
(3)为便于控制电石与水反应制备C2H2,有同学认为宜选取仪器乙,不宜选取甲,该观点是否正确_______ ?请说明原因_______ 。
(4)制备C2H2气体时,常用饱和食盐水代替水的原因是_______ 。
(5)装置戊中生成草酸的反应方程式为_______ ,反应一般控制在50℃左右,若高于50℃,则生成草酸的速率会减慢,原因是_______ 。
(6)三颈烧瓶中液体经过蒸发浓缩。冷却结晶、过滤等操作可得到草酸晶体(H2C2O4·2H2O),设计一个实验证明草酸属于二元弱酸:_______ 。

已知电石(主要成分为CaC2,含少量CaS和Ca3P2等杂质)遇水可以迅速生成C2H2,CuSO4溶液能够吸收H2S、PH3气体,浓硝酸氧化C2H2时会被还原为NO2.问答下列问题:
(1)CaC2与H2O反应制备C2H2的化学反应方程式为
(2)选择所需的仪器,接口正确的连接顺序为
(3)为便于控制电石与水反应制备C2H2,有同学认为宜选取仪器乙,不宜选取甲,该观点是否正确
(4)制备C2H2气体时,常用饱和食盐水代替水的原因是
(5)装置戊中生成草酸的反应方程式为
(6)三颈烧瓶中液体经过蒸发浓缩。冷却结晶、过滤等操作可得到草酸晶体(H2C2O4·2H2O),设计一个实验证明草酸属于二元弱酸:
您最近一年使用:0次
2 . 2021年,贵阳市空气质量优良率达98.9%,这得益于贵阳市对含硫化合物等排放的有效控制。回答下列问题:
(1)燃煤的烟气中含有 ,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
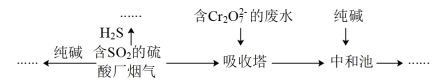
①写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
②用含 的烟气处理含
的烟气处理含 的酸性废水时,所发生的离子反应为
的酸性废水时,所发生的离子反应为___________ :
___________ +___________
+___________ +___________
+___________ =___________
=___________ +___________
+___________ +___________
+___________
配平该离子反应,并判断该处理方式利用了 的
的___________ 性。
(2)实验室提供以下试剂:浓 、稀
、稀 、酸性
、酸性 溶液、
溶液、 溶液、Cu、品红溶液。若要实现
溶液、Cu、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是___________ ,所发生反应的化学方程式为___________ ;设计实验,证明能实现该转化的操作和现象为___________ 。
(1)燃煤的烟气中含有
 ,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
①写出
 与
与 反应的化学方程式
反应的化学方程式②用含
 的烟气处理含
的烟气处理含 的酸性废水时,所发生的离子反应为
的酸性废水时,所发生的离子反应为___________
 +___________
+___________ +___________
+___________ =___________
=___________ +___________
+___________ +___________
+___________
配平该离子反应,并判断该处理方式利用了
 的
的(2)实验室提供以下试剂:浓
 、稀
、稀 、酸性
、酸性 溶液、
溶液、 溶液、Cu、品红溶液。若要实现
溶液、Cu、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是
您最近一年使用:0次
2022-07-14更新
|
371次组卷
|
2卷引用:湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题
名校
3 . 以电镀厂含锌废液(主要成分为 ,还含有少量的
,还含有少量的 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:

溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1)“氧化”工序作用之一是除锰,发生反应的离子反应方程式是_______ 。
(2)工业生产中,“试剂a”通常可选用_______ (填字母代号)
A. 溶液 B.
溶液 B. C.稀硫酸 D.
C.稀硫酸 D.
滤渣X的成分是_______ ,调 的范围是
的范围是_______ 。
(3)“沉锌”主要反应的离子反应方程式是_______ ;过滤出的产品经过多次洗涤,如何证明产品已洗净_______ 。
(4)对产品 进行系列加工可得单质
进行系列加工可得单质 和
和 ,科研团队进一步研发了可逆
,科研团队进一步研发了可逆 电池,电池工作时复合膜(由a、b膜复合而成)层间的
电池,电池工作时复合膜(由a、b膜复合而成)层间的 解离成
解离成 和
和 。
。 电池工作原理如图所示:
电池工作原理如图所示:

闭合 时,电池复合膜中
时,电池复合膜中 向
向_______ (填“左”或“右”)迁移;闭合 时,
时, 电极发生的电极反应式为
电极发生的电极反应式为_______ 。
 ,还含有少量的
,还含有少量的 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:
溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |  |  |
开始沉淀 | 1.9 | 7.0 | 3.0 | 6.6 |
完全沉淀 | 3.2 | 9.0 | 4.7 | 9.1 |
回答下列问题:
(1)“氧化”工序作用之一是除锰,发生反应的离子反应方程式是
(2)工业生产中,“试剂a”通常可选用
A.
 溶液 B.
溶液 B. C.稀硫酸 D.
C.稀硫酸 D.
滤渣X的成分是
 的范围是
的范围是(3)“沉锌”主要反应的离子反应方程式是
(4)对产品
 进行系列加工可得单质
进行系列加工可得单质 和
和 ,科研团队进一步研发了可逆
,科研团队进一步研发了可逆 电池,电池工作时复合膜(由a、b膜复合而成)层间的
电池,电池工作时复合膜(由a、b膜复合而成)层间的 解离成
解离成 和
和 。
。 电池工作原理如图所示:
电池工作原理如图所示:
闭合
 时,电池复合膜中
时,电池复合膜中 向
向 时,
时, 电极发生的电极反应式为
电极发生的电极反应式为
您最近一年使用:0次
2022-04-30更新
|
774次组卷
|
4卷引用:湖南省怀化市第三中学2022届高三下学期第三次模拟预测化学试题
湖南省怀化市第三中学2022届高三下学期第三次模拟预测化学试题湖南省株洲市第八中学2022-2023学年高二上学期期中考试化学试题河北省唐山市2022届高三普通高中学业水平选择性考试第二次模拟演练化学试题(已下线)微专题16 热点金属及其化合物制备流程(Li、Sr、Pb、Zn、Ti、Mo)-备战2023年高考化学一轮复习考点微专题
名校
解题方法
4 . 高铁酸盐在污水处理,水体消杀等方面用途广泛。高铁酸钾(K2FeO4)是一种重要的高铁酸盐。某学校化学学习小组通过下列装置制备K2FeO4,回答下列问题:

已知K2FeO4的部分性质如下:
(1)仪器a的名称是_______ 。
(2)装置乙可选用下列_______ (填标号)。

(3)连接好装置乙后,需对整套装置气密性进行检查:先_______ ,再向丁中烧杯加水至没过球形干燥管,用酒精灯微热甲中圆底烧瓶,若观察到丁中产生气泡,移去酒精灯后,丁中球形干燥管中形成一段稳定水柱,则说明装置气密性良好。
(4)该装置中,以1molFeCl3为原料,完全转化为K2FeO4需要消耗KOH_______ g。
(5)从容器丙中分离得到K2FeO4粗产品,先用冷的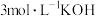 溶液洗涤,然后再用适量
溶液洗涤,然后再用适量_______ (填一常用试剂)洗涤2-3次后,最后在真空干燥箱中干燥,可得纯净的K2FeO4晶体。
(6)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,用离子方程式解释将K2FeO4投入水中达到以上净水效果的原因:_______ 。
(7)取适量K2FeO4晶体,向其中加入少量盐酸,产生大量气体,_______ (填“能”或“不能”)证明 被K2FeO4氧化了。
被K2FeO4氧化了。

已知K2FeO4的部分性质如下:
| 溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
| 稳定性 | 温度为0-5℃或强碱性溶液中能稳定存在;酸性或中性溶液中放出O2 |
(2)装置乙可选用下列

(3)连接好装置乙后,需对整套装置气密性进行检查:先
(4)该装置中,以1molFeCl3为原料,完全转化为K2FeO4需要消耗KOH
(5)从容器丙中分离得到K2FeO4粗产品,先用冷的
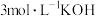 溶液洗涤,然后再用适量
溶液洗涤,然后再用适量(6)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,用离子方程式解释将K2FeO4投入水中达到以上净水效果的原因:
(7)取适量K2FeO4晶体,向其中加入少量盐酸,产生大量气体,
 被K2FeO4氧化了。
被K2FeO4氧化了。
您最近一年使用:0次
5 . 氮族元素包括氮、磷、砷、锑、铋等几种元素,请根据所掌握知识,回答以下问题。
(1)古代农谚中有“雷雨发庄稼”、“豆茬种谷,必定有福”,其中雷雨、豆茬涉及到的是自然固氮,请再写一种人工固氮方法的名称___________ 。
(2)N2是最稳定的双原子分子,原因是___________ 。
(3)联氨(N2H4)可由NH3与NaClO溶液反应制得,请写出相应的离子反应方程式___________ 。已知联氨与一水合氨类似,是一种二元弱碱向联氨溶液中加入过量硫酸生成的酸式盐的化学式为___________ 。
(4)标准状况下,将体积为VL的试管中充满NO2,倒置于水槽中,同时立即向其中通入O2,充分反应后,试管中剩余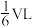 的气体,则通入的O2体积为
的气体,则通入的O2体积为___________ (保留3位小数)。
(5)常见的磷酸有:正磷酸H3PO4,亚磷酸H3PO3,次磷酸H3PO2,偏磷酸HPO3,焦磷酸H4P2O7等,其中亚磷酸和次磷酸都有强还原性,请写出次磷酸与AgNO3溶液反应的离子方程式___________ 。
(6)铜与足量浓硝酸反应后,溶液会呈现出绿色,经过科学探究证明是溶解了NO2所致,现有反应后的绿色溶液,请设计一个简单实验,证明上述科学探究结论___________ (写出操作 和现象 )。
(1)古代农谚中有“雷雨发庄稼”、“豆茬种谷,必定有福”,其中雷雨、豆茬涉及到的是自然固氮,请再写一种人工固氮方法的名称
(2)N2是最稳定的双原子分子,原因是
(3)联氨(N2H4)可由NH3与NaClO溶液反应制得,请写出相应的离子反应方程式
(4)标准状况下,将体积为VL的试管中充满NO2,倒置于水槽中,同时立即向其中通入O2,充分反应后,试管中剩余
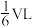 的气体,则通入的O2体积为
的气体,则通入的O2体积为(5)常见的磷酸有:正磷酸H3PO4,亚磷酸H3PO3,次磷酸H3PO2,偏磷酸HPO3,焦磷酸H4P2O7等,其中亚磷酸和次磷酸都有强还原性,请写出次磷酸与AgNO3溶液反应的离子方程式
(6)铜与足量浓硝酸反应后,溶液会呈现出绿色,经过科学探究证明是溶解了NO2所致,现有反应后的绿色溶液,请设计一个简单实验,证明上述科学探究结论
您最近一年使用:0次
2021-11-02更新
|
393次组卷
|
3卷引用:湖南省株洲市攸县第四中学2022-2023学年高三上学期第四次月考化学试题
湖南省株洲市攸县第四中学2022-2023学年高三上学期第四次月考化学试题河南省信阳市2021-2022学年高三上学期第一次教学质量检测化学试题(已下线)微专题29 非金属及其化合物制备流程与实验探究(Si、N、P、As)-备战2023年高考化学一轮复习考点微专题
名校
6 . 根据所学知识回答下列问题:

(1)将一小块新切的金属钠迅速放入平底烧瓶底部按图甲所示塞紧瓶塞。一段时间后可观察到的现象有_______ ,发生反应的化学方程式为_______ 。
(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。
①能证明钠的密度比水的小的现象是_______ 。
②能证明钠的熔点低的现象是_______ 。
③能证明有氢氧化钠生成的现象是_______ 。
(3)少量 与
与 溶液可发生反应,其化学方程式为
溶液可发生反应,其化学方程式为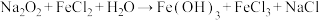 (未配平)。已知
(未配平)。已知 的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:
的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:_______ 。该反应中被还原的元素是_______ (填元素符号),氧化产物是_______ (填化学式)。
(4)向 中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为
中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为_______ 。

(1)将一小块新切的金属钠迅速放入平底烧瓶底部按图甲所示塞紧瓶塞。一段时间后可观察到的现象有
(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。
①能证明钠的密度比水的小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
(3)少量
 与
与 溶液可发生反应,其化学方程式为
溶液可发生反应,其化学方程式为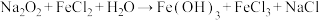 (未配平)。已知
(未配平)。已知 的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:
的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:(4)向
 中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为
中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为
您最近一年使用:0次
2021-11-12更新
|
214次组卷
|
3卷引用:湖南省百所学校大联考2021-2022学年高一上学期期中考试化学试题
名校
7 . 亚硝酰氯(ClNO)常用作催化剂和合成洗涤剂,其沸点为-5.5 ℃,易水解。某学习小组在实验室中用下图所示装置制备ClNO。已知:HNO2既有氧化性又有还原性;AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3+HNO2。
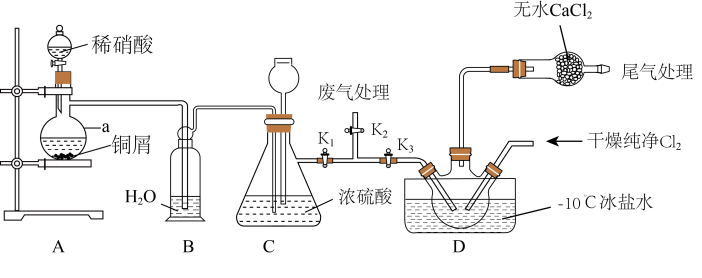
请回答下列问题:
(1)仪器a的名称为________ ,装置B的作用是________ 。
(2)装置A中发生反应的化学方程式为________ 。
(3)装置C中长颈漏斗的作用是________ 。
(4)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴入适量稀硝酸,当观察到装置C中________ 时关闭K1、K2。向装置D三颈瓶中通入干燥纯净的Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备ClNO。
(5)装置D中干燥管的作用是________ 。
(6)ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸:________ (仅提供的试剂:1 mol·L-1盐酸、1 mol·L-1 HNO2溶液、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。
②要验证ClNO与 H2O 反应后的溶液中存在Cl-和HNO2,合理的操作步骤及正确的顺序是________ (填字母代号)。
a.向烧杯中滴加过量KI淀粉溶液,溶液变蓝色
b.取1.0 mL ClNO加入到盛有10.0 mL H2O的烧杯中,充分反应
c.向烧杯中滴加酸性KMnO4溶液,溶液紫红色褪去
d.向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀

请回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的化学方程式为
(3)装置C中长颈漏斗的作用是
(4)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴入适量稀硝酸,当观察到装置C中
(5)装置D中干燥管的作用是
(6)ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸:
②要验证ClNO与 H2O 反应后的溶液中存在Cl-和HNO2,合理的操作步骤及正确的顺序是
a.向烧杯中滴加过量KI淀粉溶液,溶液变蓝色
b.取1.0 mL ClNO加入到盛有10.0 mL H2O的烧杯中,充分反应
c.向烧杯中滴加酸性KMnO4溶液,溶液紫红色褪去
d.向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀
您最近一年使用:0次
名校
解题方法
8 . 铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2可用铁粉和_____________ (填名称)反应制备,FeCl3可用铁粉和____________ (填化学式)反应制备。
(2)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为_____________________________________________________ 。
(3)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe2O3:_________________________________________________ 。
(4)现有一含有FeCl2 和FeCl3的混合样品,实验测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3 的物质的量分数为_________ 。
(5)FeCl3和HI(氢碘酸、强酸)反应时,I-转化为I2,请写出该反应的离子方程式:_________________ ;
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_____________________________________________ 。
(1)在实验室中,FeCl2可用铁粉和
(2)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为
(3)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe2O3:
(4)现有一含有FeCl2 和FeCl3的混合样品,实验测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3 的物质的量分数为
(5)FeCl3和HI(氢碘酸、强酸)反应时,I-转化为I2,请写出该反应的离子方程式:
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
名校
解题方法
9 . 从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______ (填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
回答下列问题:
①在步骤i中产生的有毒气体可能有__________________ 。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为____________ 。
③步骤iv中,生成FeCO3的离子方程式是_________________ 。
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________________ 。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:___________________ 。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:
复分解反应ii的离子方程式是________________ 。
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
_____________________ 。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):

回答下列问题:
①在步骤i中产生的有毒气体可能有
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为
③步骤iv中,生成FeCO3的离子方程式是
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:

若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
您最近一年使用:0次
2017-03-13更新
|
1442次组卷
|
5卷引用:湖南省长沙市雅礼中学2017届高考模拟试卷(二)理综化学试题
名校
解题方法
10 . 常用于印染工业的连二亚硫酸钠(Na2S2O4)俗称保险粉,可溶于水,但不溶于甲醇,其固体受热、遇水都会发生反应放出大量的热,甚至引起燃烧,工业制备流程如下:
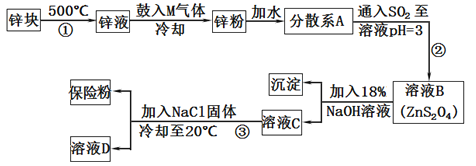
请回答下列问题:
(1)保险粉应如何保存?_______________________ (填一个注意事项)。
(2)由锌块制备锌粉的目的是___________ ;向液锌中鼓入M气体,使液态锌雾化,冷却得到粒度约为180μm(1m=106μm)的锌粉.鼓入气体M为常见的双原子单质分子,则M的化学式为___________ ;分散系A为____________ (填“溶液”“胶体”或“悬浊液”)。
(3)流程②的化学方程式为_____________________ 。
(4)流程③的分离方法步骤为___________ 、洗涤、干燥,其中洗涤所用试剂是__________ ;实验室加入NaCl固体的作用是_____________ 。
(5)保险粉可以用于除去废水中的重铬酸根离子(Cr2O72-被转化为Cr3+,S2O42-被转化为SO42-),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式____________________ 。
(6)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O=4NaHSO3或②2Na2S2O4+O2+H2O==4NaHSO3+NaHSO4
若在此条件下NaHSO3不会被氧化,请设计实验证明氧化时发生的反应是②__________________ 。

请回答下列问题:
(1)保险粉应如何保存?
(2)由锌块制备锌粉的目的是
(3)流程②的化学方程式为
(4)流程③的分离方法步骤为
(5)保险粉可以用于除去废水中的重铬酸根离子(Cr2O72-被转化为Cr3+,S2O42-被转化为SO42-),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式
(6)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O=4NaHSO3或②2Na2S2O4+O2+H2O==4NaHSO3+NaHSO4
若在此条件下NaHSO3不会被氧化,请设计实验证明氧化时发生的反应是②
您最近一年使用:0次
2017-02-17更新
|
1264次组卷
|
2卷引用:2017届湖南省株洲市高三上教学质检一化学试卷



