解题方法
1 . 试用化合价升降法配平下列化学方程式。
(1)___________Cu+___________HNO3(浓)=___________Cu(NO3)2+___________NO2↑+___________H2O,___________ ;
(2)___________NO2+___________H2O=___________HNO3+___________NO↑,___________ 。
(1)___________Cu+___________HNO3(浓)=___________Cu(NO3)2+___________NO2↑+___________H2O,
(2)___________NO2+___________H2O=___________HNO3+___________NO↑,
您最近一年使用:0次
解题方法
2 .  具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、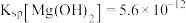 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:___________ ;加入 的目的是
的目的是___________ 。
(2)滤渣1的主要成分为___________ 、___________ 及不溶于酸、碱的杂质;加入 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
___________ 。
(3)若通入过量 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为___________ 。
(4)写出洗去固体A表面杂质的简要操作:___________ 。
(5)“煅烧”固体A反应的化学方程式为___________ 。
 具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、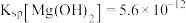 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:
 的目的是
的目的是(2)滤渣1的主要成分为
 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
(3)若通入过量
 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为(4)写出洗去固体A表面杂质的简要操作:
(5)“煅烧”固体A反应的化学方程式为
您最近一年使用:0次
2024-04-25更新
|
180次组卷
|
3卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
3 . 写出下列反应的离子方程式。
(1)往澄清石灰水中通入少量二氧化碳:______ 。
(2) 与
与 溶液反应:
溶液反应:______ 。
(3)小苏打可以用于治疗胃酸过多:______ 。
(4)向 溶液中加入少量
溶液中加入少量 溶液:
溶液:______ 。
(5)常温下, 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液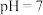 :
:______ 。
(6)高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:______
(1)往澄清石灰水中通入少量二氧化碳:
(2)
 与
与 溶液反应:
溶液反应:(3)小苏打可以用于治疗胃酸过多:
(4)向
 溶液中加入少量
溶液中加入少量 溶液:
溶液:(5)常温下,
 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液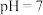 :
:(6)高铁酸钠(
 )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
您最近一年使用:0次
解题方法
4 . 锶(Sr)为第五周期IIA族元素,工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):

已知:25 ℃时, 的
的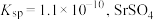 的
的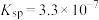 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于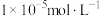 时,认为沉淀完全。
时,认为沉淀完全。
下列说法错误的是
 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):
已知:25 ℃时,
 的
的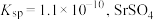 的
的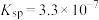 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于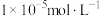 时,认为沉淀完全。
时,认为沉淀完全。下列说法错误的是
A.“高温焙烧”时 转化为SrS的化学方程式为 转化为SrS的化学方程式为 |
| B.“操作1”是蒸发浓缩、冷却结晶 |
C.为除去“溶液”中的 ,提高原料利用率,“滤液”中 ,提高原料利用率,“滤液”中 的浓度应小于 的浓度应小于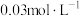 |
D.制取无水 时,一定要在无水氯化氢气流中加热 时,一定要在无水氯化氢气流中加热 至恒重 至恒重 |
您最近一年使用:0次
解题方法
5 .  是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体
是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体 具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性
具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性 。回答下列问题:
。回答下列问题:
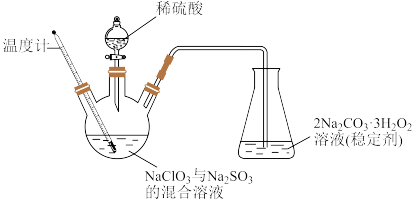
(1)盛装稀硫酸的仪器名称为___________ ;控制温度为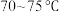 ,缓慢滴加稀硫酸,则该过程中适宜的加热方式为
,缓慢滴加稀硫酸,则该过程中适宜的加热方式为___________ ;写出生成 反应的化学方程式:
反应的化学方程式:___________ 。
(2)长导管的作用为___________ 。
(3)使用过碳酸钠( ,在水中转化为
,在水中转化为 和
和 )溶液作稳定剂时,
)溶液作稳定剂时, 被还原成较稳定的
被还原成较稳定的 ,可较长时间保存,写出锥形瓶中
,可较长时间保存,写出锥形瓶中 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(4)稳定液中的 并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使
并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使 转化成
转化成 释放出来。
释放出来。 活化率与不同活化剂(浓度均为
活化率与不同活化剂(浓度均为 )用量的关系如表。
)用量的关系如表。
①请分析盐酸活化效果最好的原因:___________ 。
②使用盐酸作活化剂时发生反应的离子方程式为___________ 。
 是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体
是一种强氧化剂,具有高效、广谱、安全的杀菌消毒能力。但是液体 具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性
具有强烈刺激性、不稳定性、高浓度易爆等特点,可通过如图(加热及夹持装置已省略)装置制备稳定性 。回答下列问题:
。回答下列问题:
(1)盛装稀硫酸的仪器名称为
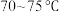 ,缓慢滴加稀硫酸,则该过程中适宜的加热方式为
,缓慢滴加稀硫酸,则该过程中适宜的加热方式为 反应的化学方程式:
反应的化学方程式:(2)长导管的作用为
(3)使用过碳酸钠(
 ,在水中转化为
,在水中转化为 和
和 )溶液作稳定剂时,
)溶液作稳定剂时, 被还原成较稳定的
被还原成较稳定的 ,可较长时间保存,写出锥形瓶中
,可较长时间保存,写出锥形瓶中 与
与 反应的离子方程式:
反应的离子方程式:(4)稳定液中的
 并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使
并不能起到杀菌的作用,因此在实际应用中,必须对其进行活化,使 转化成
转化成 释放出来。
释放出来。 活化率与不同活化剂(浓度均为
活化率与不同活化剂(浓度均为 )用量的关系如表。
)用量的关系如表。活化剂用量 活化率 活化剂 | 5mL | 10mL | 15mL | 20mL | 25mL |
盐酸 | 29.32% | 58.02% | 86.91% | 99.57% | 100.00% |
醋酸 | 26.75% | 55.52% | 79.01% | 97.22% | 97.53% |
柠檬酸 | 20.03% | 41.22% | 52.13% | 53.76% | 59.80% |
②使用盐酸作活化剂时发生反应的离子方程式为
您最近一年使用:0次
2024-03-31更新
|
112次组卷
|
2卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
6 . 水体中过量氨氮(以 表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
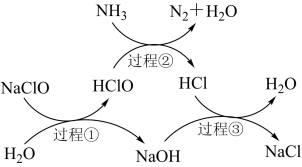
| A.上述三个过程对应的化学反应中氧化还原反应有两个 |
| B.温度越高越有利于去除氨氮 |
C.过程②生成标况下 的 的 ,转移电子数目为6 ,转移电子数目为6 |
D.上述去除氨氮的总反应可以表示为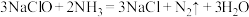 |
您最近一年使用:0次
解题方法
7 . 一种锂离子电池的正极材料中含钴酸锂( )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
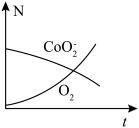
 )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
A.反应中的还原剂是 |
B.氧化性: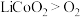 |
| C.反应配平后氧化剂与还原剂的化学计量数之比为2:1 |
D.每生成2分子 转移8个电子 转移8个电子 |
您最近一年使用:0次
解题方法
8 . 羰基硫( ,沸点:
,沸点: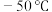 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:
(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:__________________________________ .
(2)以 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去):
 溶液
溶液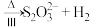
①反应Ⅰ中另一种产物是_____________ 。
②写出反应Ⅲ的离子方程式:_____________________________________________ 。
(3) 和
和 反应是制备
反应是制备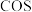 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入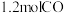 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含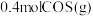 。
。
①平衡时, 的浓度为
的浓度为_____________  ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率_____________  。
。
②下列描述中能说明上述反应已达平衡状态的是_____________ (填字母)。
a.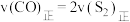
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
 ,沸点:
,沸点: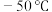 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备
 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:(2)以
 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去): 溶液
溶液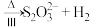
①反应Ⅰ中另一种产物是
②写出反应Ⅲ的离子方程式:
(3)
 和
和 反应是制备
反应是制备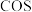 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入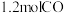 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含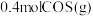 。
。①平衡时,
 的浓度为
的浓度为 ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率 。
。②下列描述中能说明上述反应已达平衡状态的是
a.
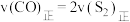
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
您最近一年使用:0次
解题方法
9 . 在硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、生石灰、铁片和7种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应。

(1)请推断它们的化学式:
①________ ;②________ ;③________ ;④________ ;⑤________ 。
(2)写出下列序号对应的物质发生反应的化学方程式:
①和②________________________ 。
②和④________________________ 。
②和⑤________________________ 。
④和⑤________________________ 。

(1)请推断它们的化学式:
①
(2)写出下列序号对应的物质发生反应的化学方程式:
①和②
②和④
②和⑤
④和⑤
您最近一年使用:0次
名校
解题方法
10 . 根据所学知识,回答下列问题。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:___________ 。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:___________ 。
(3)胶体和溶液的本质区别是___________ (填标号)。
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
(5)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下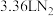 ,则转移的电子数目为
,则转移的电子数目为___________ 。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成
 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
(3)胶体和溶液的本质区别是
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
| A.熔融的NaCl | B.纯净的矿泉水 | C.某品牌的饮料 | D.熟石灰固体 |
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下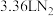 ,则转移的电子数目为
,则转移的电子数目为
您最近一年使用:0次



