名校
解题方法
1 . 已知Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒属于一个氧化还原反应中的反应物和生成物。下列叙述中不正确的是
| A.还原产物为NH4+ |
| B.氧化剂与还原剂的物质的量之比为1∶8 |
| C.Fe3+和Fe2+分别属于反应物和生成物 |
| D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
您最近一年使用:0次
2016-12-09更新
|
106次组卷
|
8卷引用:宁夏六盘山高级中学2018届高三上学期第一次月考化学试题
宁夏六盘山高级中学2018届高三上学期第一次月考化学试题2015届河南省郑州市高三第一次质量预测化学试卷2016届安徽省合肥一六八中学高三上第四次段考化学试卷2016届辽宁省大连八中高三上学期期中测试化学试卷2015-2016学年重庆市第一中学高二上学期期末化学试卷安徽省六安市第一中学2018届高三上学期第三次月考化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】福建省厦门市湖滨中学2019届高三上学期第一次阶段检测化学试题
13-14高三·海南海口·阶段练习
2 . 已知A为常见的金属单质,根据如图所示的转化关系回答下列问题。
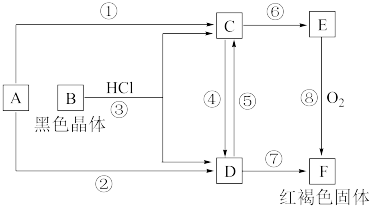
(1)确定A、B、C、D、E、F的化学式:
A为________ ,B为________ ,C为________ 。
D为________ ,E为________ ,F为________ 。
(2)写出⑧的化学方程式及④、⑤的离子方程式:___________________________ 。

(1)确定A、B、C、D、E、F的化学式:
A为
D为
(2)写出⑧的化学方程式及④、⑤的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
1001次组卷
|
4卷引用:宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题
宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题(已下线)2015届海南省海口市琼山区海政学校高三第四次月考化学试卷2015-2016学年辽宁省实验中学高一上12月月考化学试卷【全国百强校】江苏省苏州市第九高级中学2018-2019学年高一上学期十一月份月考化学试题
10-11高三上·上海·期中
3 . 某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内。
Au2O3+_____ +______ →______ +________ +_________
(2)反应中,被还原的元素是_______ ,还原剂是____________ 。
(3)将氧化剂与还原剂填入空格中,并用单线桥表示出电子转移的方向和数目。______
(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂的个数之比为_______ 。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内。
Au2O3+
(2)反应中,被还原的元素是
(3)将氧化剂与还原剂填入空格中,并用单线桥表示出电子转移的方向和数目。
(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂的个数之比为
您最近一年使用:0次
2016-12-09更新
|
344次组卷
|
8卷引用:2017届宁夏石嘴山三中高三上第二次适应性考试化学卷
2017届宁夏石嘴山三中高三上第二次适应性考试化学卷(已下线)2011届上海市南汇中学高三上学期期中考试化学卷(已下线)2011-2012学年辽宁省抚顺县高中高一上学期期中考试化学试卷(已下线)2012-2013学年河北省唐山市第一中学高二下学期期末考试化学试卷2013—2014福建省闽侯一中高三上学期10月月考化学试卷2015-2016学年四川省双流中学高一下入学考试化学试卷步步为赢 初高中衔接教材化学暑假作业:第16课时 氧化还原反应的应用(已下线)2019年7月18日 《每日一题》2020届高考一轮复习—— 氧化还原反应的配平
12-13高三·河南许昌·阶段练习
真题
解题方法
4 . 由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是_______ ,
_______ 反射炉内生成炉渣的主要成分是________ ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是________ 、________ ;
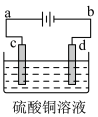
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为_______ ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为______ 。

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为

您最近一年使用:0次
2016-12-09更新
|
1098次组卷
|
11卷引用:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷
2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷2016届宁夏六盘山高中高三三模理综化学试卷(已下线)2014届河南省许昌平顶山新乡三市高三第一次调研理综化学试卷(已下线)2014届江西省赣州市四所重点中学高三上学期期末联考理综化学试卷2012年普通高等学校招生全国统一考试化学(新课标)(已下线)2014高考名师推荐化学--预测102015届江西省上饶市高三第二次高考模拟化学试卷2016届重庆市巴蜀中学高三上学期期中考试理综化学试卷2016届黑龙江省牡丹江高级中学高三上期末热身理综化学试卷2016届福建省福安市高级中学高三3月月考化学试卷2016届福建省龙岩市高中毕业班3月质量检查理综化学试卷
11-12高三·宁夏银川·阶段练习
解题方法
5 . HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为 Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是____________ (填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是____________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:____________________ 。
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是___________ (填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
__________________________________
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体.高铁酸钾作为水处理剂发挥的作用是______________________ 。
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为 Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体.高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次
2016-12-09更新
|
287次组卷
|
6卷引用:2013届宁夏银川一中高三第一次月考理综化学试卷
(已下线)2013届宁夏银川一中高三第一次月考理综化学试卷(已下线)2013届吉林省榆树市第一高级中学高三第一次月考化学试卷2016届四川省宜宾三中高三上学期第一次月考化学试卷12016届福建省福州市第一中学高三上学期期中测试化学试卷2016届四川省宜宾三中高三上学期第一次月考化学试卷2黑龙江省佳木斯学校(佳木斯市实验中学)2021-2022学年高三上学期第二次月考化学试题
9-10高二·山东·假期作业
名校
6 . 做实验时不小心沾了一些高锰酸钾,皮肤上的斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO4-+C2O42-+H+=CO2↑+Mn2++ ,关于此反应的叙述正确的是
,关于此反应的叙述正确的是
 ,关于此反应的叙述正确的是
,关于此反应的叙述正确的是| A.该反应的氧化剂是C2O42- | B.该反应右边方框内的产物是OH- |
| C.该反应电子转移总数是5e- | D.配平该反应式后,H+的系数是16 |
您最近一年使用:0次
2016-12-09更新
|
1165次组卷
|
11卷引用:宁夏育才中学2018届高三上学期第一次月考化学试题
宁夏育才中学2018届高三上学期第一次月考化学试题(已下线)2010年安丘中学高二暑期练习化学卷(六)(已下线)09~10年西南师大附中高一下期期末考试化学卷(已下线)2011-2012学年辽宁省实验中学分校高二下学期期末考试化学试卷(已下线)2015届吉林省公主岭市第一中学高三上学期第二次月考化学试卷辽宁省大连市第一中学2021-2022学年高一上学期第一次阶段性学情反馈化学试题(已下线)1.3.3 氧化还原反应方程式的书写与配平-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)(已下线)【知识图鉴】单元讲练测必修第一册第一单元03巩固练(已下线)专题03 氧化还原反应【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)(已下线)期中测试卷二【测试范围:第一、二章】-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)浙江省嘉兴市八校2023-2024学年高一上学期期中联考化学试题
11-12高三上·河北唐山·期中
名校
解题方法
7 . 前一时期“非典型肺炎”在我国部分地区流行,严重危害广大人民的身体健康,做好环境消毒是预防“非典型肺炎”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
| A.ClO2的分子结构呈V形,属非极性分子 |
| B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 |
| C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
| D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
您最近一年使用:0次
2016-12-09更新
|
1117次组卷
|
4卷引用:宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2
宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷云南省西双版纳州民族中学2017-2018学年高二6月份考试化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题
10-11高一上·宁夏银川·期中
8 . 某反应中反应物与生成物有:AsH3、H2SO4、HBrO3、K2SO4、H3AsO4、Br2和水。
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2________________ 。
(2)反应中,被还原的元素是___________ ,还原剂是________________ 。
(3)根据上述反应可推知_________ 。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2
(2)反应中,被还原的元素是
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
您最近一年使用:0次
2014·宁夏银川·二模
9 . 第五主族的磷单质及其化合物在工业上有广泛应用.
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)═3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)═6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)═P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)═CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,则△H=______ ;
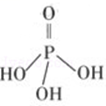
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两个水分子产物,其结构式为______ ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为______ ;
(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍.
①化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性等条件下发生下述反应:
(a) Ni2++ H2PO2﹣+ → Ni++ H2PO3﹣+
(b)6H2PO﹣2+2H+═2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a)___________________________ ;
②利用①中反应可在塑料镀件表面沉积镍﹣磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:______ ;
原理上的不同点:______ ;
化学镀的优点:______ .
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)═3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)═6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)═P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)═CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,则△H=
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两个水分子产物,其结构式为

(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍.
①化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性等条件下发生下述反应:
(a) Ni2++ H2PO2﹣+ → Ni++ H2PO3﹣+
(b)6H2PO﹣2+2H+═2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a)
②利用①中反应可在塑料镀件表面沉积镍﹣磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:
原理上的不同点:
化学镀的优点:
您最近一年使用:0次
2014-06-17更新
|
1050次组卷
|
4卷引用:2013-2014宁夏银川市第一中学高三第二次模拟考试理综化学试卷
(已下线)2013-2014宁夏银川市第一中学高三第二次模拟考试理综化学试卷2015届北京市怀柔区高三4月模拟练习化学试卷贵州省织金县一中2019届高三上学期12月份考试化学试题山东省泰安市2020届高三化学一轮复习《化学与技术》专题测试



