解题方法
1 . 芬顿试剂是以 和
和 组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体
组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体 产生机理如图所示。下列说法正确的是
产生机理如图所示。下列说法正确的是
 和
和 组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体
组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体 产生机理如图所示。下列说法正确的是
产生机理如图所示。下列说法正确的是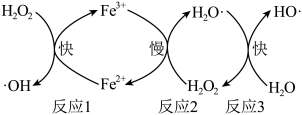
A. 在 在 产生的过程中作催化剂 产生的过程中作催化剂 |
| B.芬顿试剂去除有机污染物时使用温度不宜过高 |
C.“反应1”为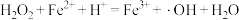 |
D.芬顿试剂降解 苯酚为 苯酚为 和 和 ,理论上消耗 ,理论上消耗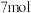 的 的 |
您最近一年使用:0次
名校
解题方法
2 . 硝酸铈(Ⅳ)铵的化学式为(NH4)2Ce(NO3)6,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验步骤进行制备。
步骤一:先制备NH4HCO3溶液,再与CeCl3溶液反应制备难溶于水的Ce2(CO3)3,制备装置图如下:
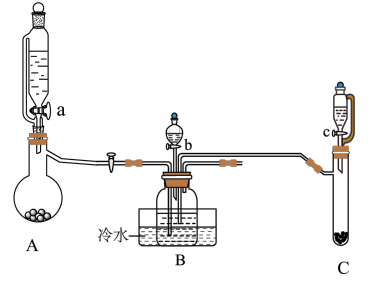
(1)装置A、C中相同仪器的名称为______ ,装置B中分液漏斗盛装的试剂是______ ,冷水浴的作用是______ 。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为______ 。装置B中发生反应的离子方程式有______ 、______ 。
(3)该实验装置存在的一处缺陷为______ 。
步骤二:取用制取的Ce2(CO3)3固体,先加硝酸溶解,再加入氨水调节溶液的pH生成氢氧化铈(Ⅳ)沉淀,过滤后在滤渣中加入浓硝酸和硝酸铵,就析出硝酸铈(Ⅳ)铵晶体。
(4)沉淀氢氧化铈(Ⅳ)的总反应离子方程式为______ 。
(5)硝酸铈(Ⅳ)铵晶体洗涤后要采取自然干燥的原因为______ 。
步骤一:先制备NH4HCO3溶液,再与CeCl3溶液反应制备难溶于水的Ce2(CO3)3,制备装置图如下:

(1)装置A、C中相同仪器的名称为
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
步骤二:取用制取的Ce2(CO3)3固体,先加硝酸溶解,再加入氨水调节溶液的pH生成氢氧化铈(Ⅳ)沉淀,过滤后在滤渣中加入浓硝酸和硝酸铵,就析出硝酸铈(Ⅳ)铵晶体。
(4)沉淀氢氧化铈(Ⅳ)的总反应离子方程式为
(5)硝酸铈(Ⅳ)铵晶体洗涤后要采取自然干燥的原因为
您最近一年使用:0次
名校
3 . 某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到______ 种单质。
(2)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有______ (填化学式),写出生成TeOSO4的离子方程式______ 。
(4)“还原”步骤生成碲单质的离子方程式为______ ,得到的粗碲经洗涤后可以得到较为纯净的碲单质,检验碲单质是否洗涤干净的实验操作:______ 。

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到
(2)煅烧时,Cr2O3发生反应的化学方程式为
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有
(4)“还原”步骤生成碲单质的离子方程式为
您最近一年使用:0次
解题方法
4 . 低品位铜矿(主要含CuS、FeO)提铜是解决我国铜产量低这一问题的重要技术,利用低品位铜矿制备Cu2O的一种工艺流程如下图所示:

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、______ 。“溶浸”中MnO2的作用是______ 。
(2)检验“溶浸”后所得溶液中是否含有 的试剂是
的试剂是______ 。
(3)“调pH”后判断 是否完全沉淀的操作是
是否完全沉淀的操作是______ 。
(4)“还原”中还原产物与氧化产物的物质的量之比为______ 。
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为______ 。
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有______ (写出一项即可)。

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、
(2)检验“溶浸”后所得溶液中是否含有
 的试剂是
的试剂是(3)“调pH”后判断
 是否完全沉淀的操作是
是否完全沉淀的操作是(4)“还原”中还原产物与氧化产物的物质的量之比为
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有
您最近一年使用:0次
5 . 湿法制备多功能水处理剂K2FeO4固体的工艺流程如下:
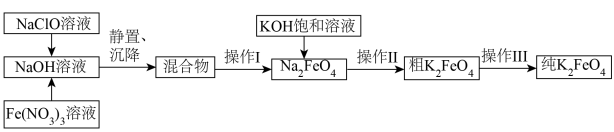
已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是

已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是
| A.溶解度:K2FeO4大于Na2FeO4 |
| B.“操作Ⅱ”所得副产物可循环使用 |
| C.“操作Ⅰ、Ⅱ、Ⅲ”都要使用的玻璃仪器有漏斗、玻璃棒、烧杯、酒精灯 |
D.生成Na2FeO4的离子方程式为 |
您最近一年使用:0次
解题方法
6 . 用某软锰矿(主要成分是 ,还含有
,还含有 、
、 等杂质)制备
等杂质)制备 的流程如下,下列说法错误的是
的流程如下,下列说法错误的是
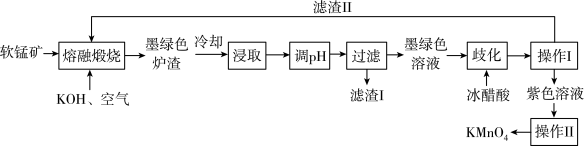
已知: 固体和溶液均为墨绿色
固体和溶液均为墨绿色
 ,还含有
,还含有 、
、 等杂质)制备
等杂质)制备 的流程如下,下列说法错误的是
的流程如下,下列说法错误的是
已知:
 固体和溶液均为墨绿色
固体和溶液均为墨绿色A.“熔融煅烧”时 参与反应的化学方程式为 参与反应的化学方程式为 |
B.“调节pH”可通入足量 |
C.“滤渣Ⅰ”的成分为 和 和 |
| D.“歧化”中氧化剂与还原剂的物质的量之比为1∶2,可以用盐酸代替冰醋酸 |
您最近一年使用:0次
解题方法
7 . 利用含硒物料(主要成分为Se、S、 、
、 和少量含Cu、Ag的化合物)制取精硒的工业流程如下:
和少量含Cu、Ag的化合物)制取精硒的工业流程如下:

已知:硫单质熔点:单斜硫119℃、正交硫95℃;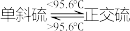 。
。
回答下列问题:
(1)“脱硫”选择温度为95℃的原因是___________ ;实验室进行“过滤”操作时,用到的玻璃仪器除烧杯外,还有___________ 。
(2)“氧化浸取”中,Se被氧化为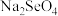 并收集到
并收集到 气体,该反应的化学反应方程式为
气体,该反应的化学反应方程式为___________ 。
(3)“除杂”中, 浓度对粗硒除杂的影响如图所示,精硒中的杂质含量先降低后上升的原因是
浓度对粗硒除杂的影响如图所示,精硒中的杂质含量先降低后上升的原因是___________ 。

(4)“酸化”过程中制取精硒的离子方程式为___________ 。
(5)测定精硒中硒的含量:
准确称量0.2000g样品,用浓 将样品中的Se氧化得到
将样品中的Se氧化得到 ;生成的
;生成的 加入到硫酸酸化的KI溶液中充分反应。用0.4000
加入到硫酸酸化的KI溶液中充分反应。用0.4000 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL。精硒中硒的质量分数为
溶液24.00mL。精硒中硒的质量分数为___________ 。上述过程发生的反应: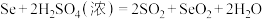 、
、 、
、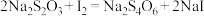
 、
、 和少量含Cu、Ag的化合物)制取精硒的工业流程如下:
和少量含Cu、Ag的化合物)制取精硒的工业流程如下:
已知:硫单质熔点:单斜硫119℃、正交硫95℃;
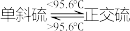 。
。回答下列问题:
(1)“脱硫”选择温度为95℃的原因是
(2)“氧化浸取”中,Se被氧化为
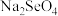 并收集到
并收集到 气体,该反应的化学反应方程式为
气体,该反应的化学反应方程式为(3)“除杂”中,
 浓度对粗硒除杂的影响如图所示,精硒中的杂质含量先降低后上升的原因是
浓度对粗硒除杂的影响如图所示,精硒中的杂质含量先降低后上升的原因是
(4)“酸化”过程中制取精硒的离子方程式为
(5)测定精硒中硒的含量:
准确称量0.2000g样品,用浓
 将样品中的Se氧化得到
将样品中的Se氧化得到 ;生成的
;生成的 加入到硫酸酸化的KI溶液中充分反应。用0.4000
加入到硫酸酸化的KI溶液中充分反应。用0.4000 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL。精硒中硒的质量分数为
溶液24.00mL。精硒中硒的质量分数为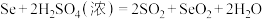 、
、 、
、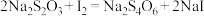
您最近一年使用:0次
2023-10-11更新
|
315次组卷
|
3卷引用:山东省济南市2023-2024学年高三上学期10月份校级联考化学试题
解题方法
8 . 钽(Ta)和铌(Nb)是性质相似的两种单质,一种以钽铌伴生矿(主要成分为SiO2、MnO2、Nb2O5、Ta2O5和少量的TiO2、FeO、CaO、MgO)为原料制取钽和铌的流程如下:

“浸取”后的浸出液中含有H2TaF7、H2NbF7两种二元强酸和锰、钛等元素。
已知:①MIBK为甲基异丁基酮;
② ,
, ,
, 。
。
(1)加快“浸取”速率可采取的措施是___________ 。
(2)浸渣的主要成分是___________ ,Ta2O5与氢氟酸反应的离子方程式为___________ 。
(3)MIBK“萃取”时可分为扩散萃取和动力学萃取两种类型。浸出液中钽的萃取率随搅拌速度的增加而进一步增加时为扩散萃取,若浸出液受到化学反应的控制则萃取类型将变为动力学萃取。搅拌速度对钽萃取率的影响如图所示。

搅拌速度在150rpm时的萃取类型为___________ ,350rpm到400rpm时但萃取率不再增加的原因是___________ 。
(4)金属铌可用金属钠还原K2NbF7,制取,也可用电解熔融的K2NbF7,制取。
①流程中钠热还原法制备铌粉的化学方程式为___________ 。
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,利用该方法制备1 mol Nb理论上消耗NaCl的物质的量为___________ mol。

“浸取”后的浸出液中含有H2TaF7、H2NbF7两种二元强酸和锰、钛等元素。
已知:①MIBK为甲基异丁基酮;
②
 ,
, ,
, 。
。(1)加快“浸取”速率可采取的措施是
(2)浸渣的主要成分是
(3)MIBK“萃取”时可分为扩散萃取和动力学萃取两种类型。浸出液中钽的萃取率随搅拌速度的增加而进一步增加时为扩散萃取,若浸出液受到化学反应的控制则萃取类型将变为动力学萃取。搅拌速度对钽萃取率的影响如图所示。

搅拌速度在150rpm时的萃取类型为
(4)金属铌可用金属钠还原K2NbF7,制取,也可用电解熔融的K2NbF7,制取。
①流程中钠热还原法制备铌粉的化学方程式为
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,利用该方法制备1 mol Nb理论上消耗NaCl的物质的量为
您最近一年使用:0次
10-11高三·山东聊城·阶段练习
名校
解题方法
9 . 高铁酸钾(K2FeO4)是一种既能杀菌消毒又能絮凝净水的水处理剂。工业制备高铁酸钾反应的离子方程式为Fe(OH)3+ClO-+OH-→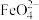 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是
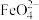 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为3:2 |
| B.高铁酸钾中铁显+6价 |
C.由上述反应可知,Fe(OH)3的氧化性强于FeO |
| D.K2FeO4处理水时,不仅能杀菌消毒,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
2023-08-23更新
|
430次组卷
|
26卷引用:山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)
(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)(已下线)2012届山东莘县实验高中高三第三次月考化学试卷2016届北京市通州区潞河中学高三上学期期中测试化学试卷2017届四川省泸州市泸化中学高三上10月月考化学卷新疆生产建设兵团第二中学2017-2018学年高一上学期期中考试化学试题福建省龙海市第二中学2019届高三年级上学期开学考化学试题【全国百强校】黑龙江省哈尔滨市第三中学校2019届高三上学期第二次调研考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期12月月考化学试题广东省佛山市第一中学2020届高三10月月考化学试题甘肃省武威市第六中学2019-2020学年高一上学期第二次段考化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应福建省永春第一中学2018-2019学年高二下学期期末考试化学试题内蒙古包钢第一中学2020届高三上学期10月月考化学试题山东省潍坊第四中学2021-2022学年高三上学期10月月考化学试题山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)辽宁省沈阳市新民市第一高级中学2021-2022学年高三上学期第二次阶段测试化学试题浙江省杭州地区(含周边)重点中学2022-2023学年高一上学期期中考试化学试卷【2022】【高一上】【杭师大附中】【期中考】【高中化学】【徐外兰收集】(已下线)第二章 单元测试卷黑龙江省黑河市第九中学2023-2024学年高三上学期摸底考试化学试题河北省衡水市武强中学2023-2024学年高一上学期期中考试化学试题河北省石家庄精英中学2023-2024学年高一上学期期中考试化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题河南省郑州市第四高级中学2023-2024学年高一上学期第二次月考 化学试题陕西省兴平市南郊高级中学2023-2024学年高一上学期第三次化学质量检测题
名校
解题方法
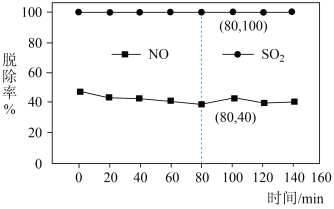
10 . 煤燃烧排放的烟气中含有 和
和 ,是大气的主要污染源之一。用
,是大气的主要污染源之一。用 溶液对烟气
溶液对烟气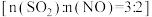 同时脱硫脱硝(分别生成
同时脱硫脱硝(分别生成 、
、 ,得到
,得到 、
、 )脱除率如图,下列说法不正确的是
)脱除率如图,下列说法不正确的是
 和
和 ,是大气的主要污染源之一。用
,是大气的主要污染源之一。用 溶液对烟气
溶液对烟气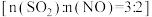 同时脱硫脱硝(分别生成
同时脱硫脱硝(分别生成 、
、 ,得到
,得到 、
、 )脱除率如图,下列说法不正确的是
)脱除率如图,下列说法不正确的是
A.脱除 的反应: 的反应: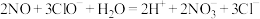 |
B.依据图中信息,在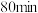 时,吸收液中 时,吸收液中 |
C. 脱除率高于 脱除率高于 的原因可能是 的原因可能是 在水中的溶解度大于 在水中的溶解度大于 |
D.随着脱除反应的进行,吸收剂溶液的 逐渐减小 逐渐减小 |
您最近一年使用:0次
2023-08-16更新
|
163次组卷
|
10卷引用:山东省师范大学附属中学2021届高三上学期第二次考试化学试题
山东省师范大学附属中学2021届高三上学期第二次考试化学试题北京大兴区2020届高三一模考试化学试题河南省三门峡市2021届高三10月阶段性考试化学试题辽宁省丹东市2021届高三上学期10月阶段测试化学试题黑龙江省大庆铁人、鸡西一中、鹤岗一中三校2021届高三上学期联考化学试题(已下线)专项特训2 非金属及其化合物对环境的影响黑龙江省齐齐哈尔市实验中学等3校2022-2023学年高三上学期11月期中考试化学试题山东省滕州市2023-2024学年高三上学期期中考试化学试题河南省周口恒大中学2023-2024学年高一上学期10月月考化学试题北京市顺义区第一中学2023-2024学年高一下学期3月月考化学试题



