名校
解题方法
1 . 硝酸铈(Ⅳ)铵的化学式为(NH4)2Ce(NO3)6,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验步骤进行制备。
步骤一:先制备NH4HCO3溶液,再与CeCl3溶液反应制备难溶于水的Ce2(CO3)3,制备装置图如下:
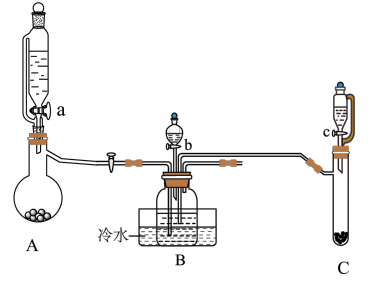
(1)装置A、C中相同仪器的名称为______ ,装置B中分液漏斗盛装的试剂是______ ,冷水浴的作用是______ 。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为______ 。装置B中发生反应的离子方程式有______ 、______ 。
(3)该实验装置存在的一处缺陷为______ 。
步骤二:取用制取的Ce2(CO3)3固体,先加硝酸溶解,再加入氨水调节溶液的pH生成氢氧化铈(Ⅳ)沉淀,过滤后在滤渣中加入浓硝酸和硝酸铵,就析出硝酸铈(Ⅳ)铵晶体。
(4)沉淀氢氧化铈(Ⅳ)的总反应离子方程式为______ 。
(5)硝酸铈(Ⅳ)铵晶体洗涤后要采取自然干燥的原因为______ 。
步骤一:先制备NH4HCO3溶液,再与CeCl3溶液反应制备难溶于水的Ce2(CO3)3,制备装置图如下:

(1)装置A、C中相同仪器的名称为
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
步骤二:取用制取的Ce2(CO3)3固体,先加硝酸溶解,再加入氨水调节溶液的pH生成氢氧化铈(Ⅳ)沉淀,过滤后在滤渣中加入浓硝酸和硝酸铵,就析出硝酸铈(Ⅳ)铵晶体。
(4)沉淀氢氧化铈(Ⅳ)的总反应离子方程式为
(5)硝酸铈(Ⅳ)铵晶体洗涤后要采取自然干燥的原因为
您最近半年使用:0次
名校
2 . 某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到______ 种单质。
(2)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有______ (填化学式),写出生成TeOSO4的离子方程式______ 。
(4)“还原”步骤生成碲单质的离子方程式为______ ,得到的粗碲经洗涤后可以得到较为纯净的碲单质,检验碲单质是否洗涤干净的实验操作:______ 。

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到
(2)煅烧时,Cr2O3发生反应的化学方程式为
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有
(4)“还原”步骤生成碲单质的离子方程式为
您最近半年使用:0次
3 . 化学基本概念和研究方法要准确掌握,下列是某同学对有关物质进行分类的列表:
(1)上述三组分类中的错误物质有______ 种。
(2)砷是与磷相邻同主族元素,则其在周期表的位置是______ ;砷化氢的电子式:______ ,它是一种有剧毒恶臭的无色气体,还原性极强,能与硝酸银反应生成Ag和砒霜(As2O3),反应的离子方程式为______ 。
(3)已知: ,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出
,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出______ 克I2(小数点后保留2位)。
(4)除去KCl溶液中少量的K2SO4杂质,要判断所加BaCl2溶液已经过量,操作是______ 。
(5)依据化学方程式,回答下列问题: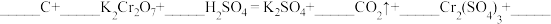
①配平完善化学方程式:_______________ 。
②H2SO4在上述反应中表现出来的性质是______ 。
③若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为______ L。
| 组序号 | 单质 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| ① | 灰砷(α-As) | Na2CO3 | H2C2O4 | K2SO4 | Na2O2 | SO3 |
| ② | 臭氧 | Fe(OH)3胶体 | H37Cl | KAl(SO4)2 | CaO | As2O3 |
| ③ | I2 | Al(OH)3 | CH3OH | K2Cr2O7 | Al2O3 | NO2 |
(2)砷是与磷相邻同主族元素,则其在周期表的位置是
(3)已知:
 ,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出
,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出(4)除去KCl溶液中少量的K2SO4杂质,要判断所加BaCl2溶液已经过量,操作是
(5)依据化学方程式,回答下列问题:
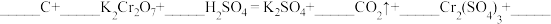
①配平完善化学方程式:
②H2SO4在上述反应中表现出来的性质是
③若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为
您最近半年使用:0次
名校
4 . 某工厂废液中含有大量的 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下:
称取m g产品溶解于大量较浓盐酸中,在 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。
已知:①氧化性 ;
;
②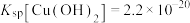 ,
, ;
;
③当溶液中离子浓度小于等于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。
根据上述产品含量测定的实验原理,下列说法错误的是
 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下: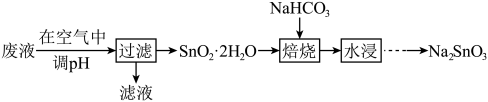
称取m g产品溶解于大量较浓盐酸中,在
 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。已知:①氧化性
 ;
;②
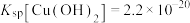 ,
, ;
;③当溶液中离子浓度小于等于
 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。根据上述产品含量测定的实验原理,下列说法错误的是
A.实验室配制 溶液时需加入盐酸和锡粉 溶液时需加入盐酸和锡粉 |
| B.若加入的还原剂不足,则测定结果偏小 |
C.滴定时选用淀粉作指示剂,产生 的离子方程式: 的离子方程式: |
D.则产品中Sn的质量分数为 % % |
您最近半年使用:0次
解题方法
5 . 低品位铜矿(主要含CuS、FeO)提铜是解决我国铜产量低这一问题的重要技术,利用低品位铜矿制备Cu2O的一种工艺流程如下图所示:

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、______ 。“溶浸”中MnO2的作用是______ 。
(2)检验“溶浸”后所得溶液中是否含有 的试剂是
的试剂是______ 。
(3)“调pH”后判断 是否完全沉淀的操作是
是否完全沉淀的操作是______ 。
(4)“还原”中还原产物与氧化产物的物质的量之比为______ 。
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为______ 。
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有______ (写出一项即可)。

已知:Ⅰ.MnCO3难溶于水,CuS难溶于水及强酸。
Ⅱ.Cu2O是一种难溶于水的红色物质。
回答下列问题:
(1)“溶浸”包括以下操作:研磨、混合、加热并搅拌、冷却、
(2)检验“溶浸”后所得溶液中是否含有
 的试剂是
的试剂是(3)“调pH”后判断
 是否完全沉淀的操作是
是否完全沉淀的操作是(4)“还原”中还原产物与氧化产物的物质的量之比为
(5)将Cu2O固体加入过量稀硫酸中,溶液变成蓝色,且仍有红色固体存在,发生反应的离子方程式为
(6)有人提出“将低品位铜矿灼烧后用酸溶解制得铜盐”的工艺流程,该流程不足之处有
您最近半年使用:0次
6 . 湿法制备多功能水处理剂K2FeO4固体的工艺流程如下:
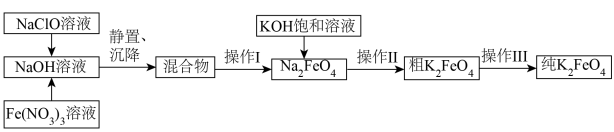
已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是

已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是
| A.溶解度:K2FeO4大于Na2FeO4 |
| B.“操作Ⅱ”所得副产物可循环使用 |
| C.“操作Ⅰ、Ⅱ、Ⅲ”都要使用的玻璃仪器有漏斗、玻璃棒、烧杯、酒精灯 |
D.生成Na2FeO4的离子方程式为 |
您最近半年使用:0次
解题方法
7 . 用某软锰矿(主要成分是 ,还含有
,还含有 、
、 等杂质)制备
等杂质)制备 的流程如下,下列说法错误的是
的流程如下,下列说法错误的是
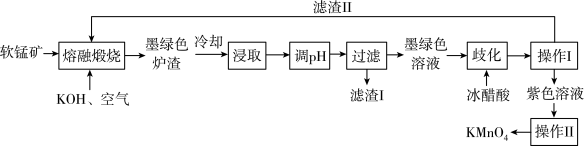
已知: 固体和溶液均为墨绿色
固体和溶液均为墨绿色
 ,还含有
,还含有 、
、 等杂质)制备
等杂质)制备 的流程如下,下列说法错误的是
的流程如下,下列说法错误的是
已知:
 固体和溶液均为墨绿色
固体和溶液均为墨绿色A.“熔融煅烧”时 参与反应的化学方程式为 参与反应的化学方程式为 |
B.“调节pH”可通入足量 |
C.“滤渣Ⅰ”的成分为 和 和 |
| D.“歧化”中氧化剂与还原剂的物质的量之比为1∶2,可以用盐酸代替冰醋酸 |
您最近半年使用:0次
解题方法
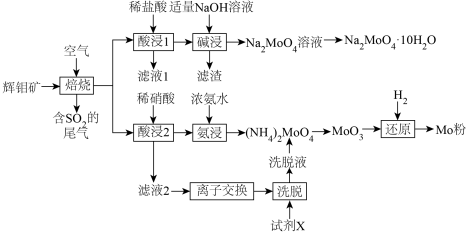
8 . 金属钼(Mo)及其化合物在合金工业中起着重要的作用,生产中常常以辉钼矿(主要成分为 ,含有FeS、CuS、
,含有FeS、CuS、 等杂质)为原料制备金属钼及其化合物。以下是生产的部分流程。
等杂质)为原料制备金属钼及其化合物。以下是生产的部分流程。
已知:①Mo的常见价态有+4、+6价。
②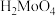 是微溶于水的无机酸,可溶于碱。
是微溶于水的无机酸,可溶于碱。
③氧气不足时,焙烧产物中可能混有 与
与 反应生成的
反应生成的 。
。
回答下列问题:
(1)焙烧的产物中Mo元素主要以 、
、 盐的形式存在。生成有
盐的形式存在。生成有 的化学方程式
的化学方程式______________________ 。
(2)与酸浸1相比,酸浸2使用稀硝酸的优点是___________ ,但是缺点是造成 的污染。
的污染。
(3)滤渣的成分主要是___________ 。碱浸时应控制pH不宜过大,原因是______________ 。
(4)已知离子交换环节,阴离子交换树脂R-OH工作原理为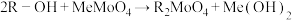 (Me代表金属阳离子),洗脱时使用的试剂X为
(Me代表金属阳离子),洗脱时使用的试剂X为___________ 。
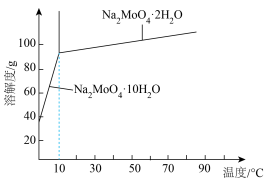
(5)钼酸钠某些晶体的溶解度曲线如图,获得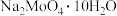 的操作为蒸发浓缩、
的操作为蒸发浓缩、___________ 、过滤、洗涤。
(6)工业上还有电氧化法 制备
制备 的方法,装置如下图所示
的方法,装置如下图所示
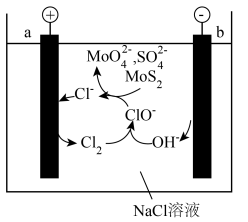
每生成0.1mol 时,外电路转移的电子数为
时,外电路转移的电子数为___________ (阿伏加德罗常数的值用 表示)
表示)
(7)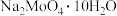 中可能混有
中可能混有 ,以硝酸铅
,以硝酸铅 为标准液测量
为标准液测量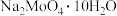 的纯度。根据下表信息,应选用的指示剂为
的纯度。根据下表信息,应选用的指示剂为___________ 。滴定终点的现象为___________ 。
取m g 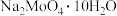 (式量为M)样品配成200mL溶液,取出20.00mL用c mol/L
(式量为M)样品配成200mL溶液,取出20.00mL用c mol/L 标准溶液进行滴定,消耗标准液V mL,
标准溶液进行滴定,消耗标准液V mL,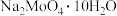 的百分含量为
的百分含量为___________ (写出表达式即可)。
 ,含有FeS、CuS、
,含有FeS、CuS、 等杂质)为原料制备金属钼及其化合物。以下是生产的部分流程。
等杂质)为原料制备金属钼及其化合物。以下是生产的部分流程。
已知:①Mo的常见价态有+4、+6价。
②
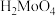 是微溶于水的无机酸,可溶于碱。
是微溶于水的无机酸,可溶于碱。③氧气不足时,焙烧产物中可能混有
 与
与 反应生成的
反应生成的 。
。回答下列问题:
(1)焙烧的产物中Mo元素主要以
 、
、 盐的形式存在。生成有
盐的形式存在。生成有 的化学方程式
的化学方程式(2)与酸浸1相比,酸浸2使用稀硝酸的优点是
 的污染。
的污染。(3)滤渣的成分主要是
(4)已知离子交换环节,阴离子交换树脂R-OH工作原理为
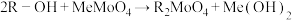 (Me代表金属阳离子),洗脱时使用的试剂X为
(Me代表金属阳离子),洗脱时使用的试剂X为(5)钼酸钠某些晶体的溶解度曲线如图,获得
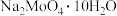 的操作为蒸发浓缩、
的操作为蒸发浓缩、
(6)工业上还有电氧化法
 制备
制备 的方法,装置如下图所示
的方法,装置如下图所示
每生成0.1mol
 时,外电路转移的电子数为
时,外电路转移的电子数为 表示)
表示)(7)
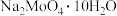 中可能混有
中可能混有 ,以硝酸铅
,以硝酸铅 为标准液测量
为标准液测量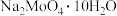 的纯度。根据下表信息,应选用的指示剂为
的纯度。根据下表信息,应选用的指示剂为 |  | PbS | 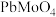 | |
 | 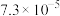 |  | 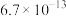 | 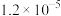 |
| 颜色 | 白色 | 亮黄色 | 黑色 | 白色 |
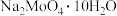 (式量为M)样品配成200mL溶液,取出20.00mL用c mol/L
(式量为M)样品配成200mL溶液,取出20.00mL用c mol/L 标准溶液进行滴定,消耗标准液V mL,
标准溶液进行滴定,消耗标准液V mL,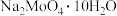 的百分含量为
的百分含量为
您最近半年使用:0次
名校
9 . 二氯异氰尿酸钠(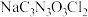 )是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入
)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入 产生高浓度NaClO溶液,然后与氰尿酸(
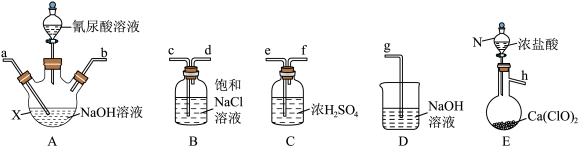
产生高浓度NaClO溶液,然后与氰尿酸( )反应制取二氯异氰尿酸钠。从下面选择所需装置完成实验。
)反应制取二氯异氰尿酸钠。从下面选择所需装置完成实验。
已知:
回答下列问题:
(1)按气流从左至右,导管口连接顺序为___________ 。(填小写字母)
(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为___________ 。
(3)装置A中制备NaClO溶液完成的现象是___________ ,在加氰尿酸溶液过程仍需不断通入 的理由是
的理由是___________ 。实验过程中若温度过度,pH过小会生成 ,写出
,写出 生成
生成 的化学方程式
的化学方程式______________________ 。
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为: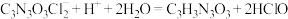 ,
, ,
, ,准确称取0.5600g样品,配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol/L
,准确称取0.5600g样品,配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol/L  标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗 溶液15.00mL。
溶液15.00mL。
①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒和量筒外,还需要___________ 。
②滴定至溶液呈微黄色时,加入的指示剂是___________ ,该样品的有效氯为___________ %。(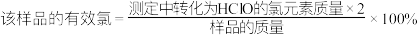 ,保留三位有效数字)
,保留三位有效数字)
③下列操作将导致样品有效氯测定值偏低的是___________ (填标号)。
a.碘量瓶中加入稀硫酸的量过少
b.滴定前滴定管未排气泡滴定后气泡消失
c.读数时,滴定前仰视、滴定后俯视
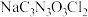 )是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入
)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入 产生高浓度NaClO溶液,然后与氰尿酸(
产生高浓度NaClO溶液,然后与氰尿酸( )反应制取二氯异氰尿酸钠。从下面选择所需装置完成实验。
)反应制取二氯异氰尿酸钠。从下面选择所需装置完成实验。
已知:

回答下列问题:
(1)按气流从左至右,导管口连接顺序为
(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为
(3)装置A中制备NaClO溶液完成的现象是
 的理由是
的理由是 ,写出
,写出 生成
生成 的化学方程式
的化学方程式(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为:
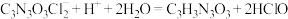 ,
, ,
, ,准确称取0.5600g样品,配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol/L
,准确称取0.5600g样品,配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol/L  标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗 溶液15.00mL。
溶液15.00mL。①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒和量筒外,还需要
②滴定至溶液呈微黄色时,加入的指示剂是
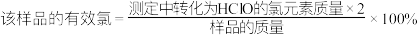 ,保留三位有效数字)
,保留三位有效数字)③下列操作将导致样品有效氯测定值偏低的是
a.碘量瓶中加入稀硫酸的量过少
b.滴定前滴定管未排气泡滴定后气泡消失
c.读数时,滴定前仰视、滴定后俯视
您最近半年使用:0次
2023-11-23更新
|
266次组卷
|
3卷引用:山东省济南市2023-2024学年高三上学期11月期中考试化学试题
解题方法
10 . 钕铁硼因其超强的磁性被誉为“永磁之王”,广泛应用于新能源汽车、信息存储等方面。从钕铁硼废料(主要成分为Nd、铁、硼、铝,少量的硅酸盐)中回收钕元素的工艺流程如图所示:
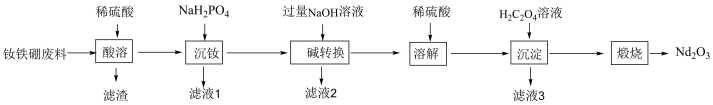
已知:①硼难溶于非氧化性酸, 难溶于水和稀酸,滤液1中主要金属离子为
难溶于水和稀酸,滤液1中主要金属离子为 、
、 ,沉淀时得到
,沉淀时得到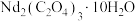 。
。
②部分金属离子( )形成氢氧化物沉淀的pH范围如表:
)形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)“滤渣”的主要成分是___________ (填化学式)。
(2)除去铝元素的操作单元为___________ 。
(3)若“酸溶”后溶液中 的浓度为1.0
的浓度为1.0 ,则“沉钕”时调节pH范围为
,则“沉钕”时调节pH范围为___________ ,“碱转化”过程Nd元素发生反应的离子方程式为___________ 。
(4)“煅烧”过程中固体质量变化( )随温度变化曲线如图所示:
)随温度变化曲线如图所示:

750K时得到的固体是___________ ,若在1000K下进行煅烧,发生反应的化学方程式为___________ 。

已知:①硼难溶于非氧化性酸,
 难溶于水和稀酸,滤液1中主要金属离子为
难溶于水和稀酸,滤液1中主要金属离子为 、
、 ,沉淀时得到
,沉淀时得到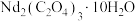 。
。②部分金属离子(
 )形成氢氧化物沉淀的pH范围如表:
)形成氢氧化物沉淀的pH范围如表:| 金属离子 |  |  |  |
| 开始沉淀 | 6.3 | 1.5 | 3.4 |
完全沉淀(离子浓度: ) ) | 8.3 | 2.8 | 4.7 |
(1)“滤渣”的主要成分是
(2)除去铝元素的操作单元为
(3)若“酸溶”后溶液中
 的浓度为1.0
的浓度为1.0 ,则“沉钕”时调节pH范围为
,则“沉钕”时调节pH范围为(4)“煅烧”过程中固体质量变化(
 )随温度变化曲线如图所示:
)随温度变化曲线如图所示:
750K时得到的固体是
您最近半年使用:0次
2023-10-11更新
|
581次组卷
|
3卷引用:山东省济南市2023-2024学年高三上学期10月份校级联考化学试题



