名校
1 . 工业上以钛铁矿(主要成分为 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: 反应。回答下列问题:
反应。回答下列问题:
(1)矿渣的主要成分是__________ ;试剂A为__________ (填化学式)。
(2)“操作Ⅱ”为__________ 、__________ 、过滤、洗涤、干燥。
(3)沸腾氯化中,氯气与矿料逆流而行,目的是__________ ,充分反应后,混合气体中CO与 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为__________ 。
(4)高温下镁与 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是__________ (填选项)。
a. b.
b. c.
c. d.Ar
d.Ar
 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: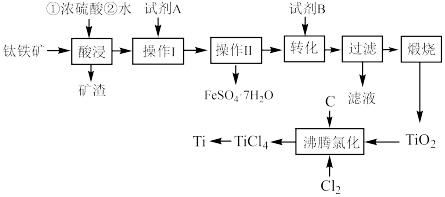
 反应。回答下列问题:
反应。回答下列问题:(1)矿渣的主要成分是
(2)“操作Ⅱ”为
(3)沸腾氯化中,氯气与矿料逆流而行,目的是
 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为(4)高温下镁与
 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是a.
 b.
b. c.
c. d.Ar
d.Ar
您最近半年使用:0次
名校
解题方法
2 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中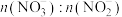 都为
都为 。下列说法错误的是
。下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中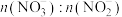 都为
都为 。下列说法错误的是
。下列说法错误的是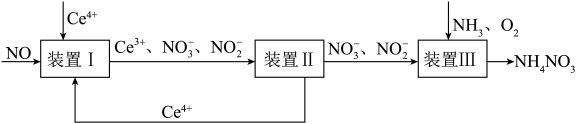
A.装置Ⅰ中若有 参与反应,则转移 参与反应,则转移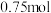 电子 电子 |
B.装置Ⅰ中反应为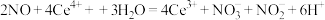 |
C.装置Ⅲ中氧化剂和还原剂的物质的量之比为 |
D.装置Ⅲ中 和 和 的体积比 的体积比 时,可实现原子利用率最大化 时,可实现原子利用率最大化 |
您最近半年使用:0次
3 . K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
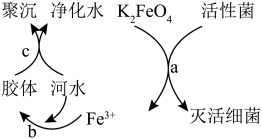
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近半年使用:0次
解题方法
4 . 水体中过量氨氮(以NH3表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
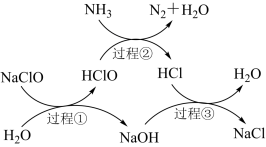

| A.过程①②③均属于氧化还原反应 |
| B.在较高温度下,氨氮去除率会降低 |
| C.每生成一个N2分子,转移6个电子 |
D.过程②中氧化剂与还原剂的物质的量之比是 |
您最近半年使用:0次
解题方法
5 . 根据所学知识回答下列问题:
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为__________ 。
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:__________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:
方案一:碱性条件下用 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为__________ 。
方案二:在碱性条件下,用铝粉处理,已知反应时Al与 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是__________ ,还原产物是__________ ,请写出反应的离子方程式:__________ 。
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:方案一:碱性条件下用
 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为方案二:在碱性条件下,用铝粉处理,已知反应时Al与
 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是
您最近半年使用:0次
解题方法
6 . 物质分类与转化是学习化学的基石,如图为氯及其化合物的“价-类”二维图,请正确回答下列问题:
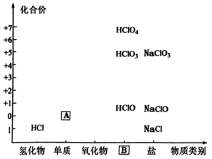
(1)填写二维图缺失的内容:化学式A__________ ;类别B__________ 。
(2)A可与热的 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式__________ 。
(3)关于盐酸与 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于__________ 反应类型(填四大基本反应类型);乙同学认为发生氧化还原反应,因为他曾经看到一篇报道称:某家庭主妇在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式__________ ,该反应从化合价角度体现了盐酸具有__________ 性。

(1)填写二维图缺失的内容:化学式A
(2)A可与热的
 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式(3)关于盐酸与
 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式
您最近半年使用:0次
解题方法
7 . 由含硒废料(主要含SiO2、S、Se、Fe2O3、CuO、ZnO等)制取硒的流程如图:
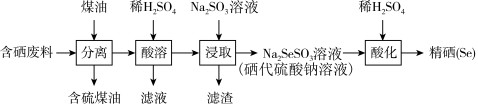
| A.加入煤油的目的是溶解S |
B.“酸溶”所得的滤液中存在 |
| C.“酸溶”时能除去废料中的全部氧化物杂质 |
D.“酸化”的离子反应为: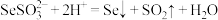 |
您最近半年使用:0次
2024-01-22更新
|
188次组卷
|
2卷引用:山东省淄博市张店区潘庄高级中学2023-2024学年高一下学期第一次月考化学试题
解题方法
8 . 某化学学习小组同学用如下实验探究 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是___________ 。
(2)乙组同学取 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:___________ 。
(3)丙组同学认为乙组的实验不够严谨,该组同学在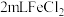 溶液中先加入
溶液中先加入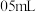 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是___________ 。
(4)丁组同学探究证实了 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式___________ 。
(5)戊组同学模拟工业上用 氧化酸性
氧化酸性  废液制备
废液制备  。
。
①若酸性 废液中:
废液中: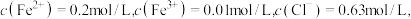 则该溶液的
则该溶液的
___________ 。
②完成 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
___________ +___________
+___________ ___________=___________
___________=___________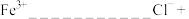 ___________。
___________。
 的性质。请回答下列问题:
的性质。请回答下列问题:(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是(2)乙组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:(3)丙组同学认为乙组的实验不够严谨,该组同学在
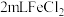 溶液中先加入
溶液中先加入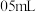 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(4)丁组同学探究证实了
 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式(5)戊组同学模拟工业上用
 氧化酸性
氧化酸性  废液制备
废液制备  。
。①若酸性
 废液中:
废液中: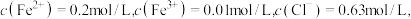 则该溶液的
则该溶液的
②完成
 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
 +___________
+___________ ___________=___________
___________=___________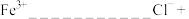 ___________。
___________。
您最近半年使用:0次
解题方法
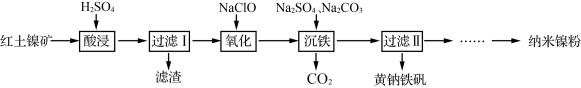
9 . 以红土镍矿(主要含有  等)为原料,获取净水剂黄钠铁矾
等)为原料,获取净水剂黄钠铁矾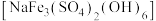 和纳米镍粉的部分工艺流程如图:
和纳米镍粉的部分工艺流程如图:
已知:
① 在
在  约为3.7时可完全转化为Fe(OH)3,Fe2+ 在
约为3.7时可完全转化为Fe(OH)3,Fe2+ 在 为9时可完全转化为
为9时可完全转化为  ;
;
② 为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
下列说法错误的是
 等)为原料,获取净水剂黄钠铁矾
等)为原料,获取净水剂黄钠铁矾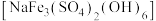 和纳米镍粉的部分工艺流程如图:
和纳米镍粉的部分工艺流程如图:
已知:
①
 在
在  约为3.7时可完全转化为Fe(OH)3,Fe2+ 在
约为3.7时可完全转化为Fe(OH)3,Fe2+ 在 为9时可完全转化为
为9时可完全转化为  ;
;②
 为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。下列说法错误的是
A.“滤渣”的主要成分是  |
B.黄钠铁矾 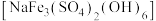 中 中 的化合价为+2价 的化合价为+2价 |
C.“氧化"过程发生的离子程式为: |
D.“沉铁”过程中加入碳酸钠的作用是调节溶液的酸碱度,使  转化为 转化为  沉淀 沉淀 |
您最近半年使用:0次
名校
解题方法
10 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
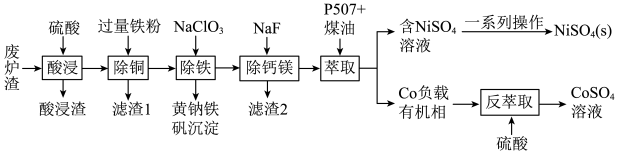
已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是___________ 。(写化学式)
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是___________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F-)最小为___________ mol·L-1。[已知离子浓度≤10-5mol/L时,认为该离子沉淀完全,Ksp(CaF2)=1.0×10-10(mol/L)3,Ksp(MgF2)=7.5×10-11(mol/L)3]
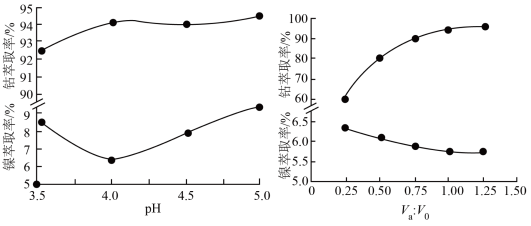
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为___________ 、___________ 。
(5)获得NiSO4(s)的“一系列操作”是___________ 。
(6)该工艺流程中,可循环利用的物质是___________ 。

已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为

(5)获得NiSO4(s)的“一系列操作”是
(6)该工艺流程中,可循环利用的物质是
您最近半年使用:0次
2023-12-27更新
|
584次组卷
|
4卷引用:山东省淄博市部分学校2023-2024学年高三上学期联考化学试卷
山东省淄博市部分学校2023-2024学年高三上学期联考化学试卷山东省实验中学2023-2024学年高三上学期11月二诊化学试题(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题



