1 . 某科研小组通过以下方案制备连二亚硫酸钠( )并测定其纯度。
)并测定其纯度。
资料: 具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时
具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时 在水溶液中以
在水溶液中以 形态结晶,高于52℃时
形态结晶,高于52℃时 在碱性溶液中脱水成无水盐。
在碱性溶液中脱水成无水盐。
回答下列问题:
(1)无氧条件下,用锌粉还原 和
和 的混合液,即可制得连二亚硫酸钠;
的混合液,即可制得连二亚硫酸钠;

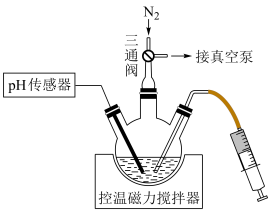
操作步骤:连接装置,关闭三通阀→___________ (填操作名称)→称取一定质量Zn置于三颈烧瓶中→___________ (填标号)pH传感→搅拌直至完全溶解。 和
和 的混合液→充入
的混合液→充入 →抽真空
→抽真空
B.抽真空→注入 和
和 的混合液→充入
的混合液→充入
C.抽真空→充入 →注入
→注入 和
和 的混合液
的混合液
(2)在上述所得溶液中滴加稍过量NaOH溶液控制pH在8.2~10.5之间,使 转化为
转化为 沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→
沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→___________ →用乙醇洗涤→干燥,可获得 。
。
(3)隔绝空气加热 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和
和 ,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有
,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有 :
:___________ 。
(4)下图是硫的四种含氧酸根的结构推断具有强氧化性的是___________ (填标号); 转化为
转化为 的离子反应方程式为
的离子反应方程式为___________ 。
(5) 含量的测定
含量的测定
实验原理: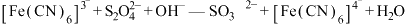 (未配平)。
(未配平)。
实验过程:称取0.25g产品加入三颈烧瓶中,维持氮气氛围,加入适量NaOH溶液,再滴加0.10
 标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中
标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中 的质量分数为
的质量分数为
___________ %(杂质不参与反应,保留四位有效数字)。
 )并测定其纯度。
)并测定其纯度。资料:
 具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时
具有强还原性,空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定:低于52℃时 在水溶液中以
在水溶液中以 形态结晶,高于52℃时
形态结晶,高于52℃时 在碱性溶液中脱水成无水盐。
在碱性溶液中脱水成无水盐。回答下列问题:
(1)无氧条件下,用锌粉还原
 和
和 的混合液,即可制得连二亚硫酸钠;
的混合液,即可制得连二亚硫酸钠;
操作步骤:连接装置,关闭三通阀→
 和
和 的混合液→充入
的混合液→充入 →抽真空
→抽真空B.抽真空→注入
 和
和 的混合液→充入
的混合液→充入
C.抽真空→充入
 →注入
→注入 和
和 的混合液
的混合液(2)在上述所得溶液中滴加稍过量NaOH溶液控制pH在8.2~10.5之间,使
 转化为
转化为 沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→
沉淀过滤除去:将所得溶液分批逐步加入一定量的NaCl固体搅拌,水蒸气加热略高于52℃左右结晶→ 。
。(3)隔绝空气加热
 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和
和 ,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有
,但实验过程未能做到完全隔绝空气,设计实验证明该分解产物中含有 :
:(4)下图是硫的四种含氧酸根的结构推断具有强氧化性的是
A.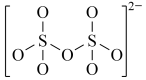 B.
B.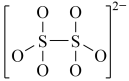 C.
C.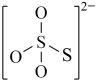 D.
D.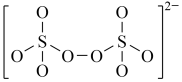
 转化为
转化为 的离子反应方程式为
的离子反应方程式为(5)
 含量的测定
含量的测定实验原理:
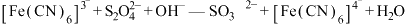 (未配平)。
(未配平)。实验过程:称取0.25g产品加入三颈烧瓶中,维持氮气氛围,加入适量NaOH溶液,再滴加0.10

 标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中
标准溶液,达到滴定终点时消耗22.00mL标准溶液。则产品中 的质量分数为
的质量分数为
您最近半年使用:0次
解题方法
2 . 用软锰矿( ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: ,
,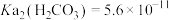 ,
,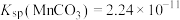
有关离子沉淀时的pH:
回答下列问题:
(1)“滤渣1”除了S、 外,还有
外,还有___________ (填化学式)。
(2)“试剂a”可以选用___________ (填标号),“除杂”应调pH范围是___________ 。
A.NaClO B. C.
C. D.NaOH
D.NaOH
(3)“沉锰”时发生反应的离子方程式为___________ 。
(4)“沉锰”后上层清液中
___________ 。
(5)“焙烧”时发生反应的化学方程式为___________ 。
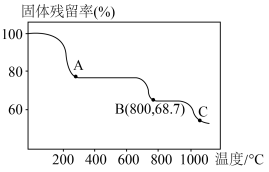
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为___________ 。
 ,含
,含 、
、 杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料
杂质)和方铅矿(PbS含少量FeS)为原料制备电极材料 的工艺流程如下:
的工艺流程如下: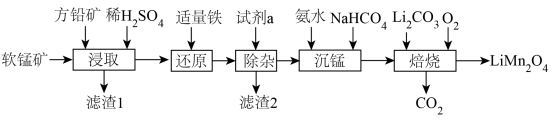
 ,
,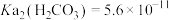 ,
,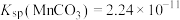
有关离子沉淀时的pH:
 |  |  |  | |
| 开始沉淀时 | 8.3 | 7.6 | 2.7 | 3.0 |
| 沉淀完全时 | 9.8 | 9.6 | 3.7 | 4.7 |
(1)“滤渣1”除了S、
 外,还有
外,还有(2)“试剂a”可以选用
A.NaClO B.
 C.
C. D.NaOH
D.NaOH(3)“沉锰”时发生反应的离子方程式为
(4)“沉锰”后上层清液中

(5)“焙烧”时发生反应的化学方程式为
(6)碳酸锰在空气中加热,固体残留率随温度变化如图。碳酸锰在300℃时已完全脱碳,则B点对应的物质的化学式为
您最近半年使用:0次
解题方法
3 . 以含钒钢渣(含 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
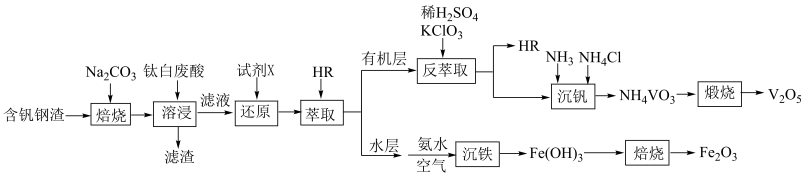
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
已知:有机萃取剂 的萃取原理为
的萃取原理为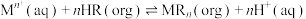 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
回答下列问题:
(1)在空气中“焙烧”时, 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
(2)“溶浸”时生成的滤渣除了 外,还有
外,还有___________ (填化学式)。
(3)“还原”的目的是将溶液中的+5价钒和 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。
(4)在“萃取”操作后从水层中获得 的离子方程式是
的离子方程式是___________ 。
(5)在“反萃取”操作中 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)上述流程中可循环利用的物质除 外,还有
外,还有___________ (填化学式)。
(7)常温“沉钒”,维持溶液中 的总浓度为
的总浓度为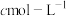 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
___________  [已知
[已知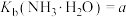 ;
; ]。
]。
 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
已知:有机萃取剂
 的萃取原理为
的萃取原理为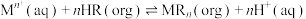 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。回答下列问题:
(1)在空气中“焙烧”时,
 转化为
转化为 的化学方程式为
的化学方程式为(2)“溶浸”时生成的滤渣除了
 外,还有
外,还有(3)“还原”的目的是将溶液中的+5价钒和
 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。A. | B. | C. | D. |
(4)在“萃取”操作后从水层中获得
 的离子方程式是
的离子方程式是(5)在“反萃取”操作中
 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为(6)上述流程中可循环利用的物质除
 外,还有
外,还有(7)常温“沉钒”,维持溶液中
 的总浓度为
的总浓度为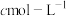 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
 [已知
[已知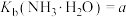 ;
; ]。
]。
您最近半年使用:0次
4 . 下图是某些单质及其化合物之间的转化关系图。已知: 为一种金属单质,
为一种金属单质, 为淡黄色固体,
为淡黄色固体, 为一种常见液体,常温常压下
为一种常见液体,常温常压下 是一种气态单质,反应条件省略。
是一种气态单质,反应条件省略。
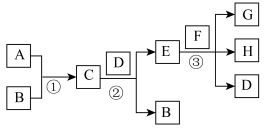
回答下列问题:
(1)反应①中的还原剂为______ (填名称),消耗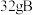 需要转移的电子数目为
需要转移的电子数目为______  。
。
(2) 与
与 在酸性条件下反应生成
在酸性条件下反应生成 的离子方程式为
的离子方程式为______ 。
(3)气体 通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为
通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为______ (填化学式)。
(4) 是一种比较安全的漂白剂、消毒剂,其中一种制备
是一种比较安全的漂白剂、消毒剂,其中一种制备 的原理是利用
的原理是利用 与盐酸反应,同时生成气体
与盐酸反应,同时生成气体 ,写出该反应的化学方程式
,写出该反应的化学方程式______ 。
 为一种金属单质,
为一种金属单质, 为淡黄色固体,
为淡黄色固体, 为一种常见液体,常温常压下
为一种常见液体,常温常压下 是一种气态单质,反应条件省略。
是一种气态单质,反应条件省略。
回答下列问题:
(1)反应①中的还原剂为
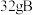 需要转移的电子数目为
需要转移的电子数目为 。
。(2)
 与
与 在酸性条件下反应生成
在酸性条件下反应生成 的离子方程式为
的离子方程式为(3)气体
 通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为
通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为(4)
 是一种比较安全的漂白剂、消毒剂,其中一种制备
是一种比较安全的漂白剂、消毒剂,其中一种制备 的原理是利用
的原理是利用 与盐酸反应,同时生成气体
与盐酸反应,同时生成气体 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近半年使用:0次
解题方法
5 . 叠氮化钠 常用于安全气囊的气体发生剂,
常用于安全气囊的气体发生剂, 与水或酸均易发生爆炸。某学习小组利用如图装置制备叠氮化钠。
与水或酸均易发生爆炸。某学习小组利用如图装置制备叠氮化钠。
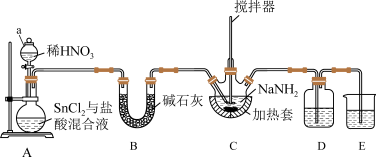
已知:I. 有毒,有氧化性,不与酸、碱反应;
有毒,有氧化性,不与酸、碱反应;
Ⅱ.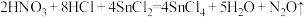 。
。
回答下列问题:
(1)仪器 的名称为
的名称为______ ,装置 的作用为
的作用为______ 。
(2) 是
是 的发生装置,该反应同时生成一种碱性气体
的发生装置,该反应同时生成一种碱性气体 和一种强碱,其反应的化学方程式为
和一种强碱,其反应的化学方程式为______ 。
(3)装置D中的试剂最佳选择为______ , 为
为 的吸收装置。
的吸收装置。
① 溶液 ②浓硫酸 ③稀硫酸
溶液 ②浓硫酸 ③稀硫酸
(4)测定产品纯度:取 反应所得到的固体,与足量
反应所得到的固体,与足量 溶液发生如下反应:
溶液发生如下反应: ,收集反应产生的气体体积为
,收集反应产生的气体体积为 ,本实验条件下气体摩尔体积为
,本实验条件下气体摩尔体积为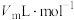 ,则产品中
,则产品中 的纯度为
的纯度为______  (用
(用 、
、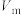 的代数式表示)。
的代数式表示)。
 常用于安全气囊的气体发生剂,
常用于安全气囊的气体发生剂, 与水或酸均易发生爆炸。某学习小组利用如图装置制备叠氮化钠。
与水或酸均易发生爆炸。某学习小组利用如图装置制备叠氮化钠。
已知:I.
 有毒,有氧化性,不与酸、碱反应;
有毒,有氧化性,不与酸、碱反应;Ⅱ.
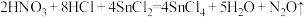 。
。回答下列问题:
(1)仪器
 的名称为
的名称为 的作用为
的作用为(2)
 是
是 的发生装置,该反应同时生成一种碱性气体
的发生装置,该反应同时生成一种碱性气体 和一种强碱,其反应的化学方程式为
和一种强碱,其反应的化学方程式为(3)装置D中的试剂最佳选择为
 为
为 的吸收装置。
的吸收装置。①
 溶液 ②浓硫酸 ③稀硫酸
溶液 ②浓硫酸 ③稀硫酸(4)测定产品纯度:取
 反应所得到的固体,与足量
反应所得到的固体,与足量 溶液发生如下反应:
溶液发生如下反应: ,收集反应产生的气体体积为
,收集反应产生的气体体积为 ,本实验条件下气体摩尔体积为
,本实验条件下气体摩尔体积为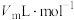 ,则产品中
,则产品中 的纯度为
的纯度为 (用
(用 、
、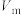 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
6 . 亚氯酸钠 是一种高效的漂白剂和氧化剂。制备亚氯酸钠通常在
是一种高效的漂白剂和氧化剂。制备亚氯酸钠通常在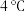 以下进行,装置Ⅰ发生反应
以下进行,装置Ⅰ发生反应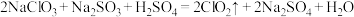 ,产生的
,产生的 气体通入装置Ⅱ制得
气体通入装置Ⅱ制得 。
。
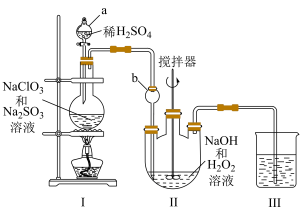
回答下列问题:
(1)仪器 的名称为
的名称为___________ 。仪器 的作用为
的作用为___________ 。
(2)利用装置Ⅱ制备 的离子方程式为
的离子方程式为___________ 。
(3)装置Ⅱ的控温方式为___________(填标号)。
(4)测产品纯度:取 产品溶于去氧蒸馏水配成
产品溶于去氧蒸馏水配成 溶液,取
溶液,取 所配溶液于雉形瓶中,滴加过量
所配溶液于雉形瓶中,滴加过量 溶液,再滴加淀粉溶液,用
溶液,再滴加淀粉溶液,用 的
的 标准溶液滴定,平行滴定3次,消耗
标准溶液滴定,平行滴定3次,消耗 溶液体积平均为
溶液体积平均为 (已知:
(已知: 被还原为
被还原为 ,
, ,且杂质不参与反应)。
,且杂质不参与反应)。
①判断达到滴定终点的方法是___________ 。
②产品中 的纯度为
的纯度为___________ 。
③下列操作会使实验结果偏高的是___________ (填标号)。
A.雉形瓶洗净后残留水 B.滴定结束后俯视读数
C.未用标准液润洗滴定管 D.盛标准液的滴定管尖嘴处滴定前有气泡,滴定后气泡消失
 是一种高效的漂白剂和氧化剂。制备亚氯酸钠通常在
是一种高效的漂白剂和氧化剂。制备亚氯酸钠通常在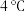 以下进行,装置Ⅰ发生反应
以下进行,装置Ⅰ发生反应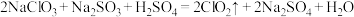 ,产生的
,产生的 气体通入装置Ⅱ制得
气体通入装置Ⅱ制得 。
。
回答下列问题:
(1)仪器
 的名称为
的名称为 的作用为
的作用为(2)利用装置Ⅱ制备
 的离子方程式为
的离子方程式为(3)装置Ⅱ的控温方式为___________(填标号)。
| A.油浴 | B.冰水浴 | C.酒精灯 | D.热水浴 |
(4)测产品纯度:取
 产品溶于去氧蒸馏水配成
产品溶于去氧蒸馏水配成 溶液,取
溶液,取 所配溶液于雉形瓶中,滴加过量
所配溶液于雉形瓶中,滴加过量 溶液,再滴加淀粉溶液,用
溶液,再滴加淀粉溶液,用 的
的 标准溶液滴定,平行滴定3次,消耗
标准溶液滴定,平行滴定3次,消耗 溶液体积平均为
溶液体积平均为 (已知:
(已知: 被还原为
被还原为 ,
, ,且杂质不参与反应)。
,且杂质不参与反应)。①判断达到滴定终点的方法是
②产品中
 的纯度为
的纯度为③下列操作会使实验结果偏高的是
A.雉形瓶洗净后残留水 B.滴定结束后俯视读数
C.未用标准液润洗滴定管 D.盛标准液的滴定管尖嘴处滴定前有气泡,滴定后气泡消失
您最近半年使用:0次
2023-12-03更新
|
71次组卷
|
2卷引用:山东省日照市2023-2024学年高二上学期期中校际联合考试化学试题
7 . 向水中滴加 ,剧烈反应,液面上有白雾形成,并有刺激性气体逸出。下列说法错误的是
,剧烈反应,液面上有白雾形成,并有刺激性气体逸出。下列说法错误的是
 ,剧烈反应,液面上有白雾形成,并有刺激性气体逸出。下列说法错误的是
,剧烈反应,液面上有白雾形成,并有刺激性气体逸出。下列说法错误的是A.该反应方程式为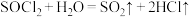 |
B.将 与 与 混合并加热,可得到无水 混合并加热,可得到无水 |
| C.将产生的气体通入石蕊溶液中,会看到石蕊溶液先变红后褪色 |
D.向反应后溶液中滴加 溶液,有不溶于稀硝酸的白色沉淀析出 溶液,有不溶于稀硝酸的白色沉淀析出 |
您最近半年使用:0次
2023-12-03更新
|
91次组卷
|
3卷引用:山东省日照市2023-2024学年高二上学期期中校际联合考试化学试题
8 . 某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。
ⅱ、浓碱条件下,MnO 可被OH-还原为MnO
可被OH-还原为MnO 。
。
ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
(1)B中试剂是_____ 。
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为_____ 。
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是_____ 。
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO 氧化为MnO
氧化为MnO 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:_____ ,但通过实验测定溶液的碱性变化很小。
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_____ ,溶液绿色缓慢加深,原因是MnO2被_____ (填化学式)氧化,可证明实验Ⅲ的悬浊液中氧化剂过量。
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是_____ 。
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:_____ 。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO
 (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。ⅱ、浓碱条件下,MnO
 可被OH-还原为MnO
可被OH-还原为MnO 。
。ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
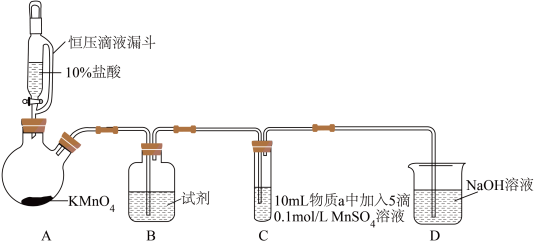
| 实验 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO
 氧化为MnO
氧化为MnO 。
。①用化学方程式表示可能导致溶液碱性减弱的原因:
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:
您最近半年使用:0次
2023-11-29更新
|
662次组卷
|
29卷引用:山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题(已下线)2022年北京市高考真题化学试题(部分试题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)四川省成都市树德中学2022-2023学年高三上学期入学考试理综化学试题2022年北京市高考真题化学试题(已下线)第28讲 定性、定量实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)2022年北京高考真题变式题1-14(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)专题三 离子反应-实战高考·二轮复习核心突破突破超重点 高效突破综合实验 实验4 创新探究实验角度1控制变量法探究(已下线)2022年北京高考真题化学试题变式题(实验探究题)(已下线)题型46 实验原理探究型综合实验(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 氯气和卤族元素(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)新疆乌鲁木齐市第101中学2022-2023学年高一上学期12月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)北京一零一中学2023-2024学年高三上学期11月统练五化学试题(已下线)微专题 物质性质综合实验探究北京市日坛中学2023-2024学年高三上学期10月检测化学试题北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题江苏省苏州市工业园区星海实验高级中学2023-2024学年高一上学期12月调研化学试题
解题方法
9 . 一种以铍矿石(含BeO、 、
、 及少量Ca、Mg、Mn等元素)与配料(氟硅酸钠、碳酸钠)生产氧化铍的工艺流程如下:
及少量Ca、Mg、Mn等元素)与配料(氟硅酸钠、碳酸钠)生产氧化铍的工艺流程如下:
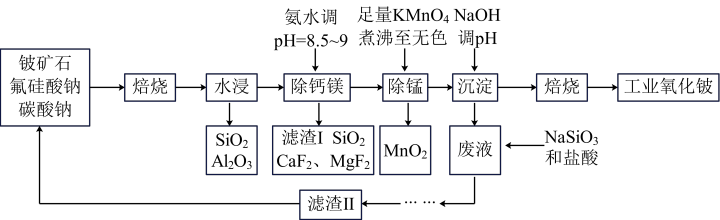
已知:Ⅰ.氟硅酸钠( )、
)、 微溶于冷水,溶解度随温度升高有所增大。
微溶于冷水,溶解度随温度升高有所增大。
Ⅱ.常温下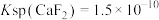 ,
, 。
。
Ⅲ.Be、Al的化合物性质相似。
回答下列问题:
(1)焙烧时Be、Si元素分别转化为 、
、 ,铍矿石中BeO发生反应的化学方程式为
,铍矿石中BeO发生反应的化学方程式为________ 。
(2)水浸时为了增大铍元素的浸出率可采取的措施有________ (答1条即可)。
(3)氨水调pH目的之一是除去未反应的 ,离子方程式为
,离子方程式为________ ,同时产物可除去 、
、 。
。
(4)除锰液中存在 ,常温下,平衡常数
,常温下,平衡常数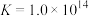 。当溶液中
。当溶液中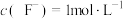 ,
,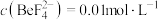 时,加NaOH调pH应稍大于
时,加NaOH调pH应稍大于________ ,若pH过大会造成氧化铍产率________ (填“增大”、“减小”或“不变”)。
(5)废液处理后得到滤渣Ⅱ________ (填化学式)可回收利用。回收滤渣Ⅱ后,废液中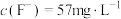 ,每升废液中需要加熟石灰至少
,每升废液中需要加熟石灰至少________ mg,才能达到排放标准 (结果保留整数)。
(结果保留整数)。
 、
、 及少量Ca、Mg、Mn等元素)与配料(氟硅酸钠、碳酸钠)生产氧化铍的工艺流程如下:
及少量Ca、Mg、Mn等元素)与配料(氟硅酸钠、碳酸钠)生产氧化铍的工艺流程如下:
已知:Ⅰ.氟硅酸钠(
 )、
)、 微溶于冷水,溶解度随温度升高有所增大。
微溶于冷水,溶解度随温度升高有所增大。Ⅱ.常温下
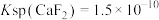 ,
, 。
。Ⅲ.Be、Al的化合物性质相似。
回答下列问题:
(1)焙烧时Be、Si元素分别转化为
 、
、 ,铍矿石中BeO发生反应的化学方程式为
,铍矿石中BeO发生反应的化学方程式为(2)水浸时为了增大铍元素的浸出率可采取的措施有
(3)氨水调pH目的之一是除去未反应的
 ,离子方程式为
,离子方程式为 、
、 。
。(4)除锰液中存在
 ,常温下,平衡常数
,常温下,平衡常数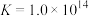 。当溶液中
。当溶液中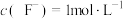 ,
,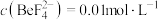 时,加NaOH调pH应稍大于
时,加NaOH调pH应稍大于(5)废液处理后得到滤渣Ⅱ
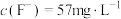 ,每升废液中需要加熟石灰至少
,每升废液中需要加熟石灰至少 (结果保留整数)。
(结果保留整数)。
您最近半年使用:0次
名校
解题方法
10 . 研究小组以 (绿色固体)、
(绿色固体)、 等物质为原料制备无水
等物质为原料制备无水 (紫色固体,易升华),制备装置如图所示(夹持装置略)。
(紫色固体,易升华),制备装置如图所示(夹持装置略)。

(1)仪器A的名称为_______ 。
(2)B处的装置为_______ (填选项),装的药品为_______ 。
(3)本实验持续通入 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、_______ 。
(4)反应管的温度升到 时发生反应,生成
时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为_______ 。 有剧毒,与水反应生成两种酸性气体,
有剧毒,与水反应生成两种酸性气体, 分子中
分子中 原子的杂化方式为
原子的杂化方式为_______ ,C装置中生成的盐是_______ (填化学式)。
(5)反应管右端有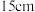 在加热炉外,其作用是
在加热炉外,其作用是_______ 。
(6)反应完成后,得到固体产品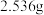 。则该实验的产率为
。则该实验的产率为_______  。[已知
。[已知 的式量为152;
的式量为152; 的式量为158.5]
的式量为158.5]
 (绿色固体)、
(绿色固体)、 等物质为原料制备无水
等物质为原料制备无水 (紫色固体,易升华),制备装置如图所示(夹持装置略)。
(紫色固体,易升华),制备装置如图所示(夹持装置略)。
(1)仪器A的名称为
(2)B处的装置为

(3)本实验持续通入
 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、(4)反应管的温度升到
 时发生反应,生成
时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为 有剧毒,与水反应生成两种酸性气体,
有剧毒,与水反应生成两种酸性气体, 分子中
分子中 原子的杂化方式为
原子的杂化方式为(5)反应管右端有
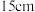 在加热炉外,其作用是
在加热炉外,其作用是(6)反应完成后,得到固体产品
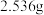 。则该实验的产率为
。则该实验的产率为 。[已知
。[已知 的式量为152;
的式量为152; 的式量为158.5]
的式量为158.5]
您最近半年使用:0次
2023-09-10更新
|
191次组卷
|
3卷引用: 山东省日照市五莲县第一中学2024届高三上学期阶段性测试化学试题



