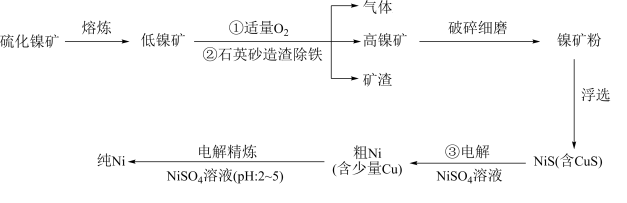
1 . 元素Ni用途广泛,工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:
已知:①电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2 -2e-= 2H+ E=0.00V; Cu-2e- =Cu2+ E=0.34V;
Fe -2e-= Fe2+ E=-0.44V; Ni-2e-=Ni2+ E=-0.25V
②常温下溶度积常数 Ksp(NiS)=1.07×10-21; Ksp(CuS)=1.27×10-36
(1)可用光洁的镍丝代替铂丝蘸取化学试剂在焰色反应实验中灼烧,原因是_________ 。
(2)就制备高镍矿的相关问题请回答:
①通入氧气时控制适量的目的是________________ 。
②已知矿渣能使酸性高锰酸钾溶液褪色,原因是__________________ 。
(3)电解制粗镍时阳极发生的主要电极反应式___________________ 。
(4)电解精炼镍的过程需控制pH为2~5,试分析原因__________________ 。
(5)工业生产中常用加NiS的方法除去溶液中的Cu2+,若过滤后溶液中c(Ni2+) 为0.107 mol/L,则滤液中残留的c(Cu2+)为________ mol/L。

已知:①电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2 -2e-= 2H+ E=0.00V; Cu-2e- =Cu2+ E=0.34V;
Fe -2e-= Fe2+ E=-0.44V; Ni-2e-=Ni2+ E=-0.25V
②常温下溶度积常数 Ksp(NiS)=1.07×10-21; Ksp(CuS)=1.27×10-36
(1)可用光洁的镍丝代替铂丝蘸取化学试剂在焰色反应实验中灼烧,原因是
(2)就制备高镍矿的相关问题请回答:
①通入氧气时控制适量的目的是
②已知矿渣能使酸性高锰酸钾溶液褪色,原因是
(3)电解制粗镍时阳极发生的主要电极反应式
(4)电解精炼镍的过程需控制pH为2~5,试分析原因
(5)工业生产中常用加NiS的方法除去溶液中的Cu2+,若过滤后溶液中c(Ni2+) 为0.107 mol/L,则滤液中残留的c(Cu2+)为
您最近一年使用:0次
解题方法
2 . 高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1) 工业上由软锰矿(主要成分为MnO2)生产高锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4), 该反应的化学方程式是___________________________________________________ 。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在_______ (填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的化学方程式是____________________________ 。
(2) 某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:

①轧钢废酸中Fe2+的作用是_____________________________________________ 。
②操作I、操作Ⅱ、操作Ⅲ的名称是_______________ ,
用到的玻璃仪器有_______________________________________________________ 。
③溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是___________________ 。
(1) 工业上由软锰矿(主要成分为MnO2)生产高锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4), 该反应的化学方程式是
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在
(2) 某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:

①轧钢废酸中Fe2+的作用是
②操作I、操作Ⅱ、操作Ⅲ的名称是
用到的玻璃仪器有
③溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是
您最近一年使用:0次



