名校
解题方法
1 . I.硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
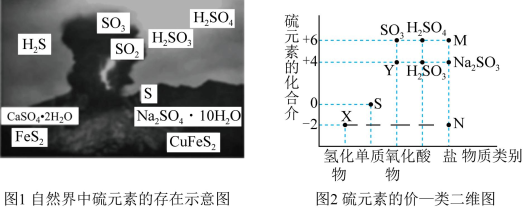
(1)图1中与图2中M、N对应的物质分别是____ 、____ 。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为____ 。
(3)SO2和氯水都有漂白性,为了增强漂白效果,有人将氯水和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为____ 。
II.为探究影响H2O2分解速率的因素,设计如表实验:
(4)实验①③研究的是____ 对H2O2分解速率的影响。
(5)记录实验①在第5min时收集到气体22.4mL(已折算成标准状况),则5min内,v(H2O2)=____ 。
(6)实验①②研究的是____ 对H2O2分解速率的影响。
(7)若向0.4mol/LH2O2中加入少量KI,H2O2的分解机理为:
第一步:H2O2+I-→H2O+IO-
第二步:H2O2+IO-→H2O+O2+I-
据此说明KI在H2O2的分解中起____ 作用。

(1)图1中与图2中M、N对应的物质分别是
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)SO2和氯水都有漂白性,为了增强漂白效果,有人将氯水和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为
II.为探究影响H2O2分解速率的因素,设计如表实验:
| 编号 | 温度 | c(H2O2)/mol·L−1 | V(H2O2)/mL | 催化剂 |
| ① | 20℃ | 0.4 | 10 | 无 |
| ② | 20℃ | 0.8 | 10 | 无 |
| ③ | 30℃ | 0.4 | 10 | 无 |
| ④ | 30℃ | 0.4 | 10 | MnO2 |
(5)记录实验①在第5min时收集到气体22.4mL(已折算成标准状况),则5min内,v(H2O2)=
(6)实验①②研究的是
(7)若向0.4mol/LH2O2中加入少量KI,H2O2的分解机理为:
第一步:H2O2+I-→H2O+IO-
第二步:H2O2+IO-→H2O+O2+I-
据此说明KI在H2O2的分解中起
您最近半年使用:0次
名校
解题方法
2 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
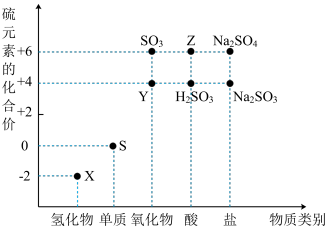
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______ 。
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是_______ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为_______ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近半年使用:0次
2021-04-25更新
|
415次组卷
|
14卷引用:【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题
【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题黑龙江省双鸭山市第一中学2023-2024学年高二上学期开学考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一下学期第一次月考化学试题沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题2贵州省岑巩县第四中学2019-2020学年高一上学期期末考试化学试题贵州省施秉县一中2019-2020学年高一上学期期末考试化学试题辽宁省大连市辽宁师范大学附属中学2019-2020学年高一下学期期末考试化学试题鲁科版(2019)高一必修第一册第三章第2节 硫的转化 课时4 不同价态硫元素之间的转化酸雨及其防治高一必修第一册(苏教2019版)专题4 第二单元 硫及其化合物的相互转化 课时2 含硫物质之间的转化 氧化还原反应方程式的配平河北省安平中学2020-2021学年高一上学期12月月考化学试题山西省长治市第二中学校2020-2021学年高一下学期期中考试化学试题河北省张家口市第一中学2020-2021学年高一下学期4月月考化学试题湖南省衡阳县四中2022-2023学年高二上学期开学摸底考试化学试题(A卷)江苏省盱眙中学2022-2023学年高一下学期6月阶段测试化学试题
3 . 现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近半年使用:0次
4 . I.现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO
(1)属于电解质的是_______ (用序号填空,下同);属于酸性氧化物的是_______ 。
(2)实验室中少量①通常保存在_____ 中;④在工业上大量用于_____ (写出一种用途即可)。
(3)⑧与⑥反应的化学方程式_______
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
Ⅱ.某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: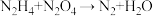 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
(5)①配平该方程式_______ 。
②该反应中,氧化产物与还原产物的质量之比为_______ 。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧与⑥反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
Ⅱ.某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: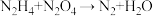 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。(5)①配平该方程式
②该反应中,氧化产物与还原产物的质量之比为
您最近半年使用:0次
名校
解题方法
5 . 氧化还原反应在日常生活和工业生产中有重要应用。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应: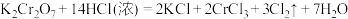
(1)用“双线桥”标明该反应中电子转移的方向和数目。_____
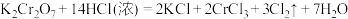
(2)该反应中被氧化的元素是_____ ,还原产物是_____ 。
(3)该反应中氧化剂与还原剂的微粒个数比为_____ 。
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准……
(4)K2FeO4中铁元素的化合价为_____ 。
(5)下列关于K2FeO4的说法中,不正确的是_____ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)将K2FeO4与水反应的化学方程式补充完整并配平:_____ 。
_____K2FeO4+_____H2O=_____Fe(OH)3(胶体)+_____+_____KOH
该反应消耗1个K2FeO4时,转移的电子数为_____ 个。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:
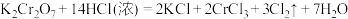
(1)用“双线桥”标明该反应中电子转移的方向和数目。
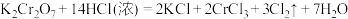
(2)该反应中被氧化的元素是
(3)该反应中氧化剂与还原剂的微粒个数比为
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准……
(4)K2FeO4中铁元素的化合价为
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)将K2FeO4与水反应的化学方程式补充完整并配平:
_____K2FeO4+_____H2O=_____Fe(OH)3(胶体)+_____+_____KOH
该反应消耗1个K2FeO4时,转移的电子数为
您最近半年使用:0次
6 . 铅及其化合物用途多样。查资料得知 是不溶于水的固体,受热会发生分解反应。其晶体内部有空穴,使得电子可以在空穴中跳跃,就像在跳棋中那样,因此
是不溶于水的固体,受热会发生分解反应。其晶体内部有空穴,使得电子可以在空穴中跳跃,就像在跳棋中那样,因此 可以导电,用作铅酸蓄电池的电极。请回答下列问题:
可以导电,用作铅酸蓄电池的电极。请回答下列问题:
(1)铅是碳的同族元索,铅原子基态价电子排布式为___________ ,常见价态为_____ 和_____ 。
(2) 与浓盐酸共热生成黄绿色气体,反应的离子方程式为
与浓盐酸共热生成黄绿色气体,反应的离子方程式为___________ 。
(3) 可由
可由 与次氯酸钠溶液反应制得,反应的离子方程式为
与次氯酸钠溶液反应制得,反应的离子方程式为___________ ; 也可以通过石墨为电极,以
也可以通过石墨为电极,以 和
和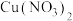 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为___________ 。
(4) 在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重3.35%(即
在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重3.35%(即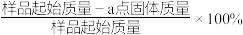 )的残留固体,通过计算求表示a点固体组成的化学式为
)的残留固体,通过计算求表示a点固体组成的化学式为___________ 。 ,从而实现铅的再生利用。在此过程中涉及如下两个反应:
,从而实现铅的再生利用。在此过程中涉及如下两个反应:
①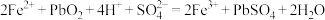
②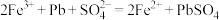
上述过程中 的作用是
的作用是___________ ,请设计实验方案证明 的作用
的作用___________ 。
 是不溶于水的固体,受热会发生分解反应。其晶体内部有空穴,使得电子可以在空穴中跳跃,就像在跳棋中那样,因此
是不溶于水的固体,受热会发生分解反应。其晶体内部有空穴,使得电子可以在空穴中跳跃,就像在跳棋中那样,因此 可以导电,用作铅酸蓄电池的电极。请回答下列问题:
可以导电,用作铅酸蓄电池的电极。请回答下列问题:(1)铅是碳的同族元索,铅原子基态价电子排布式为
(2)
 与浓盐酸共热生成黄绿色气体,反应的离子方程式为
与浓盐酸共热生成黄绿色气体,反应的离子方程式为(3)
 可由
可由 与次氯酸钠溶液反应制得,反应的离子方程式为
与次氯酸钠溶液反应制得,反应的离子方程式为 也可以通过石墨为电极,以
也可以通过石墨为电极,以 和
和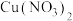 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为(4)
 在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重3.35%(即
在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重3.35%(即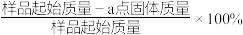 )的残留固体,通过计算求表示a点固体组成的化学式为
)的残留固体,通过计算求表示a点固体组成的化学式为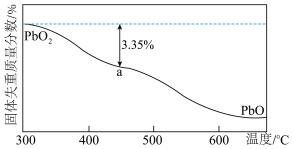
 ,从而实现铅的再生利用。在此过程中涉及如下两个反应:
,从而实现铅的再生利用。在此过程中涉及如下两个反应:①
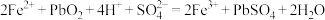
②
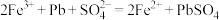
上述过程中
 的作用是
的作用是 的作用
的作用
您最近半年使用:0次
名校
解题方法
7 . 砷及其化合物用途非常广泛。回答下列问题:
(1)已知:砷(As)与磷位于同一主族相邻位置。画出砷的原子结构示意图:___________ 。
(2) (亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出
(亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出 。第一步电离方程式为
。第一步电离方程式为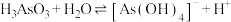 ,第二步的电离方程式为
,第二步的电离方程式为___________ 。
(3)古代《本草衍义》提纯砒霜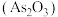 作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是
作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是___________ 。砷黄铁矿(FeAsS)制烧可生成砒霜和红棕色固体,该反应的化学方程式为___________ 。
(4)处理含砷废水的方法很多,在含高浓度 的酸性溶液中加入
的酸性溶液中加入 可将
可将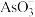 转化为
转化为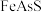 而脱除,该脱除砷的离子方程式为
而脱除,该脱除砷的离子方程式为___________ 。
(1)已知:砷(As)与磷位于同一主族相邻位置。画出砷的原子结构示意图:
(2)
 (亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出
(亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出 。第一步电离方程式为
。第一步电离方程式为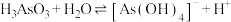 ,第二步的电离方程式为
,第二步的电离方程式为(3)古代《本草衍义》提纯砒霜
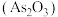 作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是
作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是(4)处理含砷废水的方法很多,在含高浓度
 的酸性溶液中加入
的酸性溶液中加入 可将
可将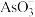 转化为
转化为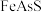 而脱除,该脱除砷的离子方程式为
而脱除,该脱除砷的离子方程式为
您最近半年使用:0次
名校
解题方法
8 . 钪(Sc)是一种稀土金属,钪及其化合物在宇航、电子、超导等方面有着广泛的用途。钛白粉中含有Fe、 、
、 等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪(
等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪( )的工艺流程如下:
)的工艺流程如下:

回答下列问题:
(1)基态Sc原子的价电子排布式为___________ 。
(2)“萃取”时 、
、 、
、 均进入有机相中,则在“洗涤”时加入
均进入有机相中,则在“洗涤”时加入 的目的是
的目的是___________ 。
(3)“滤渣1”的主要成分是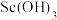 、
、___________ (写化学式)。
(4)在“调pH”时先加氨水调节pH=3,此时过滤所得滤渣主要成分是___________ ;再向滤液中加入氨水调pH=6,此时滤液中 的浓度为
的浓度为___________  ;检验含
;检验含 滤液中是否含
滤液中是否含 的试剂为
的试剂为___________ (写化学式)。(已知: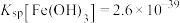 ,
,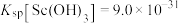 )。
)。
(5)“沉铳”时用到草酸。已知草酸的 ;
; ;则在25℃时pH=3的草酸溶液中
;则在25℃时pH=3的草酸溶液中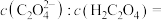
___________ 。
(6)写出草酸钪在空气中“焙烧”时反应的化学方程式___________ 。
 、
、 等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪(
等多种成分,用酸化后的钛白废水富集钪,并回收氧化钪( )的工艺流程如下:
)的工艺流程如下:
回答下列问题:
(1)基态Sc原子的价电子排布式为
(2)“萃取”时
 、
、 、
、 均进入有机相中,则在“洗涤”时加入
均进入有机相中,则在“洗涤”时加入 的目的是
的目的是(3)“滤渣1”的主要成分是
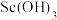 、
、(4)在“调pH”时先加氨水调节pH=3,此时过滤所得滤渣主要成分是
 的浓度为
的浓度为 ;检验含
;检验含 滤液中是否含
滤液中是否含 的试剂为
的试剂为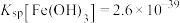 ,
,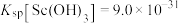 )。
)。(5)“沉铳”时用到草酸。已知草酸的
 ;
; ;则在25℃时pH=3的草酸溶液中
;则在25℃时pH=3的草酸溶液中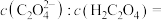
(6)写出草酸钪在空气中“焙烧”时反应的化学方程式
您最近半年使用:0次
名校
解题方法
9 . 阅读下面一段材料并回答问题。
(1)K2FeO4中铁元素的化合价为_______ ;
(2)制备K2FeO4需要在_______ (填“酸性”“碱性”或“中性”)环境中进行。
(3)K2FeO4溶于水发生如下反应,请将化学方程式补充完整_______ 。
_______ K2FeO4+_______H2O=_______Fe(OH)3(胶体)+_______+_______KOH
(4)K2FeO4能用于净水的原因是_______ 。
(5)湿法制备K2FeO4的反应体系里有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O,写出制高铁酸钾的离子反应方程式:
、Cl-、H2O,写出制高铁酸钾的离子反应方程式:_______ 。
| 高铁酸钾使用说明书 |
| 【化学式】K2FeO4 |
| 【性状】暗紫色具有金属光泽的粉末,无臭无味 |
| 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气 |
| 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 |
| 【用量】消毒净化1 L水投放5mgK2FeO4即可达到卫生标准 |
(2)制备K2FeO4需要在
(3)K2FeO4溶于水发生如下反应,请将化学方程式补充完整
_______ K2FeO4+_______H2O=_______Fe(OH)3(胶体)+_______+_______KOH
(4)K2FeO4能用于净水的原因是
(5)湿法制备K2FeO4的反应体系里有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O,写出制高铁酸钾的离子反应方程式:
、Cl-、H2O,写出制高铁酸钾的离子反应方程式:
您最近半年使用:0次
10 . 二氧化氯( )是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
(1) 的制备:制备
的制备:制备 的常用方法有两种,分别为
的常用方法有两种,分别为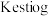 法、
法、 与
与 反应法。
反应法。
①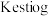 法制备
法制备 的原理为
的原理为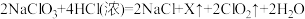 ,X的化学式为
,X的化学式为___________ ,将 通入
通入 溶液中,有红褐色沉淀生成,溶液中的主要阴离子为
溶液中,有红褐色沉淀生成,溶液中的主要阴离子为 、
、 ,若消耗
,若消耗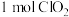 ,则被氧化的
,则被氧化的 为
为___________  。
。
② 与
与 反应法制备
反应法制备 ,生成物只有两种,参加反应的
,生成物只有两种,参加反应的 与
与 物质的量之比为
物质的量之比为___________ ,与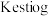 法相比,
法相比, 与
与 反应法的优点是
反应法的优点是___________ (填一条)。
(2) 的用途:除毒、除异味。
的用途:除毒、除异味。
① 可以将剧毒的氰化物氧化成
可以将剧毒的氰化物氧化成 和
和 ,离子方程式为
,离子方程式为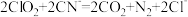 ,
, 属于
属于___________ (填“酸”“碱”或“两”)性氧化物,每转移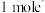 ,生成
,生成___________ L(标准状况下) 。
。
② 能把水溶液中有异味的
能把水溶液中有异味的 氧化成四价锰,使之形成不溶于水的
氧化成四价锰,使之形成不溶于水的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
 )是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:(1)
 的制备:制备
的制备:制备 的常用方法有两种,分别为
的常用方法有两种,分别为 法、
法、 与
与 反应法。
反应法。①
 法制备
法制备 的原理为
的原理为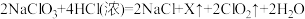 ,X的化学式为
,X的化学式为 通入
通入 溶液中,有红褐色沉淀生成,溶液中的主要阴离子为
溶液中,有红褐色沉淀生成,溶液中的主要阴离子为 、
、 ,若消耗
,若消耗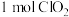 ,则被氧化的
,则被氧化的 为
为 。
。②
 与
与 反应法制备
反应法制备 ,生成物只有两种,参加反应的
,生成物只有两种,参加反应的 与
与 物质的量之比为
物质的量之比为 法相比,
法相比, 与
与 反应法的优点是
反应法的优点是(2)
 的用途:除毒、除异味。
的用途:除毒、除异味。①
 可以将剧毒的氰化物氧化成
可以将剧毒的氰化物氧化成 和
和 ,离子方程式为
,离子方程式为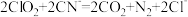 ,
, 属于
属于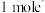 ,生成
,生成 。
。②
 能把水溶液中有异味的
能把水溶液中有异味的 氧化成四价锰,使之形成不溶于水的
氧化成四价锰,使之形成不溶于水的 ,该反应的离子方程式为
,该反应的离子方程式为
您最近半年使用:0次
2023-02-07更新
|
365次组卷
|
2卷引用:黑龙江省黑河市第九中学2023-2024学年高三上学期摸底考试化学试题



