名校
1 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。
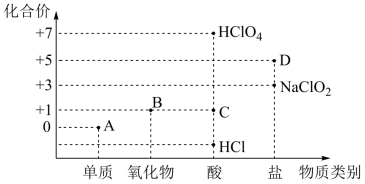
(1)已知D可用于实验室制O2,其焰色试验为紫色。A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则M在水溶液中的电离方程式为_______ 。
(3)已知Br2的性质和Cl2有一定的相似性,写出Br2在一定条件下与NaOH溶液反应的离子方程式_______ 。
(4)臭氧氧化技术被广泛用于饮用水的处理,当水中含有Br-时会产生易致癌的BrO 。但水中BrO
。但水中BrO 能被活性炭有效去除,其去除机理分为两步:
能被活性炭有效去除,其去除机理分为两步:
第一步是活性炭吸附BrO
第二步是BrO 被活性炭还原为Br-,
被活性炭还原为Br-,
其反应方程式(未配平)如下:
①_______。
②*C+BrO-→Br- +*CO2
反应的总方程式为:2BrO + 3*C=2Br-+3*CO2 。
+ 3*C=2Br-+3*CO2 。
已知:其中*C代表活性炭表面,*CO2代表活性炭表面氧化物;每步中的*C被氧化为*CO2,则反应①的方程式为_______ ;则反应①与反应②中参加反应的*C个数之比为_______ 。

(1)已知D可用于实验室制O2,其焰色试验为紫色。A、B、C、D四种物质中,属于电解质的是
(2)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则M在水溶液中的电离方程式为
(3)已知Br2的性质和Cl2有一定的相似性,写出Br2在一定条件下与NaOH溶液反应的离子方程式
(4)臭氧氧化技术被广泛用于饮用水的处理,当水中含有Br-时会产生易致癌的BrO
 。但水中BrO
。但水中BrO 能被活性炭有效去除,其去除机理分为两步:
能被活性炭有效去除,其去除机理分为两步:第一步是活性炭吸附BrO

第二步是BrO
 被活性炭还原为Br-,
被活性炭还原为Br-,其反应方程式(未配平)如下:
①_______。
②*C+BrO-→Br- +*CO2
反应的总方程式为:2BrO
 + 3*C=2Br-+3*CO2 。
+ 3*C=2Br-+3*CO2 。已知:其中*C代表活性炭表面,*CO2代表活性炭表面氧化物;每步中的*C被氧化为*CO2,则反应①的方程式为
您最近半年使用:0次
名校
2 . 非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硫和氮等元素的踪迹。
Ⅰ.利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b,物质的量之比为_______ 。
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______。
(3)已知e为正盐,且能被酸性K2Cr2O7氧化为Na2SO4,Cr2O 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:_______ 。
Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
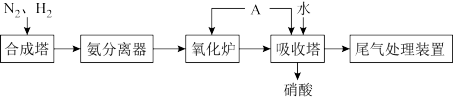
(4)写出氧化炉中的化学反应方程式_______ 。
(5)向吸收塔中通入A的作用_______ 。
(6)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用_______ (填化学式)溶液吸收。
(7)取一定量制取的硝酸加水稀释到50mL,加入过量的铜充分反应,再向溶液中加入足量的稀硫酸,最终共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),铜仍有剩余,将气体充入0.125molO2并倒扣于水槽中,水刚好充满整支试管,则原稀释后的硝酸的物质的量浓度是_______ mol/L,反应溶解的铜有_______ g。
Ⅰ.利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b,物质的量之比为
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______。
| A.H2S溶液 | B.CaCl2溶液 |
| C.H2O2溶液 | D.饱和Na2CO3溶液 |
 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(4)写出氧化炉中的化学反应方程式
(5)向吸收塔中通入A的作用
(6)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用
(7)取一定量制取的硝酸加水稀释到50mL,加入过量的铜充分反应,再向溶液中加入足量的稀硫酸,最终共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),铜仍有剩余,将气体充入0.125molO2并倒扣于水槽中,水刚好充满整支试管,则原稀释后的硝酸的物质的量浓度是
您最近半年使用:0次
名校
3 . 稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。钪(Sc)是一种稀土金属,利用钛尾矿回收金属轨的工艺流程如图所示。回答下列问题: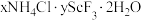 是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
(1)“焙烧”过程生成Sc2O3的化学方程式为_________ ,为“焙烧”过程中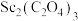 充分反应可采取的措施有
充分反应可采取的措施有__________ 。
(2)“置换”过程需要在氩气做保护气、高温条件下进行,发生反应的化学方程式为_______ 。
(3)“脱水除铵”过程中固体质量与温度的关系如图1所示,其中在380℃到400℃会有白烟冒出,保温至无烟气产生,即得到ScF3,由图象中数据计算复盐中x:z=___________ 。__________ (填“正”或“负”极),d电极上的电极反应式为__________ 。

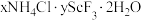 是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。②“脱水除铵”是复盐沉淀的热分解过程。
(1)“焙烧”过程生成Sc2O3的化学方程式为
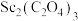 充分反应可采取的措施有
充分反应可采取的措施有(2)“置换”过程需要在氩气做保护气、高温条件下进行,发生反应的化学方程式为
(3)“脱水除铵”过程中固体质量与温度的关系如图1所示,其中在380℃到400℃会有白烟冒出,保温至无烟气产生,即得到ScF3,由图象中数据计算复盐中x:z=

您最近半年使用:0次
4 . 叠氮化钠(NaN3)在防腐、有机合成和汽车行业有着广泛的用途。用氨基钠(NaNH2)制取叠氮化钠的方程式为: 实验室用下列装置制取叠氮化钠。
实验室用下列装置制取叠氮化钠。
(1)仪器a的名称是_______ 。
(2)装置B、D的主要作用分别是_______ 。
(3)检查装置A的气密性的操作是_______ 。
(4)装置A中反应除生成装置C中需要的物质外,还生成SnCl4等。其反应的化学方程式为_______ 。
(5)装置C处充分反应后,应先停止加热,再关闭分液漏斗活塞,原因是_______ 。
(6)取mg反应后装置C中所得固体,用下图所示装置测定产品的纯度(原理为:加入ClO将N1氧化成N2,测定N2的体积,从而计算产品纯度)。_______ 。
②若G的初始读数为V1mL、末读数为V2mL,本实验条件下气体摩尔体积为VL·mol-1,则产品中NaN3的质量分数为_______ 。
 实验室用下列装置制取叠氮化钠。
实验室用下列装置制取叠氮化钠。
(1)仪器a的名称是
(2)装置B、D的主要作用分别是
(3)检查装置A的气密性的操作是
(4)装置A中反应除生成装置C中需要的物质外,还生成SnCl4等。其反应的化学方程式为
(5)装置C处充分反应后,应先停止加热,再关闭分液漏斗活塞,原因是
(6)取mg反应后装置C中所得固体,用下图所示装置测定产品的纯度(原理为:加入ClO将N1氧化成N2,测定N2的体积,从而计算产品纯度)。
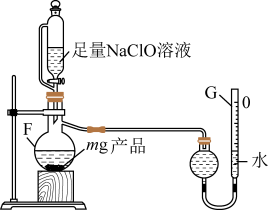
②若G的初始读数为V1mL、末读数为V2mL,本实验条件下气体摩尔体积为VL·mol-1,则产品中NaN3的质量分数为
您最近半年使用:0次
名校
5 . 过硫酸钠(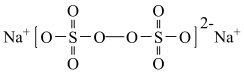 ),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对
),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对 制备和性质及用途进行探究。
制备和性质及用途进行探究。

工业制备过硫酸钠的反应原理:
主反应:

副反应:

实验室设计如图实验装置:
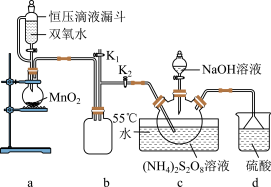
(2)装置b的作用是
(3)上述反应过程中,d装置中主要发生的化学反应方程式为
Ⅱ.探究
 的性质与用途
的性质与用途(4)
 用于废水中苯酚的降解
用于废水中苯酚的降解已知:a.
 具有强氧化性,
具有强氧化性, 浓度较高时会导致
浓度较高时会导致 淬灭。
淬灭。b.
 可将苯酚氧化,但反应速率较慢,加入
可将苯酚氧化,但反应速率较慢,加入 可加快反应。
可加快反应。过程为ⅰ.

ⅱ.
 将苯酚氧化为
将苯酚氧化为 气体
气体①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将含
 的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。
的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。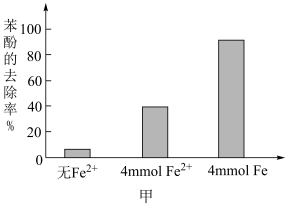
 ,可明显提高苯酚的降解率,主要原因是
,可明显提高苯酚的降解率,主要原因是(5)工业上利用
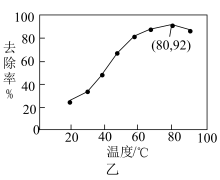
 能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含
能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含 的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为
的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为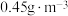 ,
, 达到最大去除率,NO去除的平均反应速率:
达到最大去除率,NO去除的平均反应速率:
 。
。
您最近半年使用:0次
6 . 铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1) 的价层电子排布式为
的价层电子排布式为___________ 。
(2)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(3)工业上用黄铁矿制硫酸的第一步反应化学反应方程式为___________ 。
(4)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为___________ 。
②欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:
溶液循环利用,现有下列试剂:
A.浓硝酸 B.铁粉 C.氯气 D.烧碱 E.浓氨水
需要用到的试剂除盐酸外还需要___________ (填字母)。
(5)高铁酸钠( )是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,
)是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么, 、
、 、
、 三种消毒杀菌剂的消毒效率最高的是
三种消毒杀菌剂的消毒效率最高的是___________ 。
(6)近年来, 作为制备锂离子电池正极材料
作为制备锂离子电池正极材料 的重要原料而成为研究热点。一种以
的重要原料而成为研究热点。一种以 、
、 、氨水为主要原料制备
、氨水为主要原料制备 ,并测定产物样品中铁元素的质量分数,主要步骤如下:
,并测定产物样品中铁元素的质量分数,主要步骤如下:
i.取 样品,加入过量盐酸充分溶解,再滴加
样品,加入过量盐酸充分溶解,再滴加 (还原剂)至溶液呈浅黄色;
(还原剂)至溶液呈浅黄色;
ii.加入 ,恰好将i中残余的少量
,恰好将i中残余的少量 还原为
还原为 ;
;
iii.用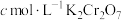 标准溶液滴定
标准溶液滴定 ,消耗
,消耗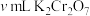 标准溶液。
标准溶液。
①步骤iii的离子方程式是:___________ 。
②产物中铁元素的质量分数为___________ 。
(1)
 的价层电子排布式为
的价层电子排布式为(2)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(3)工业上用黄铁矿制硫酸的第一步反应化学反应方程式为
(4)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为②欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:
溶液循环利用,现有下列试剂:A.浓硝酸 B.铁粉 C.氯气 D.烧碱 E.浓氨水
需要用到的试剂除盐酸外还需要
(5)高铁酸钠(
 )是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,
)是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么, 、
、 、
、 三种消毒杀菌剂的消毒效率最高的是
三种消毒杀菌剂的消毒效率最高的是(6)近年来,
 作为制备锂离子电池正极材料
作为制备锂离子电池正极材料 的重要原料而成为研究热点。一种以
的重要原料而成为研究热点。一种以 、
、 、氨水为主要原料制备
、氨水为主要原料制备 ,并测定产物样品中铁元素的质量分数,主要步骤如下:
,并测定产物样品中铁元素的质量分数,主要步骤如下:i.取
 样品,加入过量盐酸充分溶解,再滴加
样品,加入过量盐酸充分溶解,再滴加 (还原剂)至溶液呈浅黄色;
(还原剂)至溶液呈浅黄色;ii.加入
 ,恰好将i中残余的少量
,恰好将i中残余的少量 还原为
还原为 ;
;iii.用
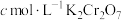 标准溶液滴定
标准溶液滴定 ,消耗
,消耗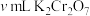 标准溶液。
标准溶液。①步骤iii的离子方程式是:
②产物中铁元素的质量分数为
您最近半年使用:0次
名校
解题方法
7 . 氧化还原反应在日常生活和工业生产中有重要应用。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:
(1)用“双线桥”标明该反应中电子转移的方向和数目。__________

(2)该反应中被氧化的元素是___________ ,还原产物是___________ 。
(3)该反应中氧化剂与还原剂的微粒个数比为___________ 。
Ⅱ.阅读下面一段材料并回答问题。
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为___________ 。
(5)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐 b.固体保存需要防潮
b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式___________ 。
(7)将K2FeO4与水反应的化学方程式补充完整并配平:____________
___________ +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为___________ 个
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为___________ g。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:

(1)用“双线桥”标明该反应中电子转移的方向和数目。

(2)该反应中被氧化的元素是
(3)该反应中氧化剂与还原剂的微粒个数比为
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
 b.固体保存需要防潮
b.固体保存需要防潮c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式
(7)将K2FeO4与水反应的化学方程式补充完整并配平:
___________
 +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为
您最近半年使用:0次
名校
8 . 氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产、生活、科研具有重要意义。
(1) 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。
①一氯胺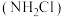 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式___________ 。
②二氧化氯 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
③等物质的量下列物质消毒效率最高的是___________ (填序号;已知:消毒效率可用单位物质的量的消毒剂的氧化能力衡量)。
a. b.
b. c.
c. d.
d.
(2) 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式:___________ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(3) 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为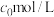 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为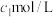 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。
①写出溶液中 分解生成
分解生成 的化学方程式:
的化学方程式:___________ 。
② 时刻溶液中
时刻溶液中
___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)
 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。①一氯胺
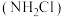 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式②二氧化氯
 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为③等物质的量下列物质消毒效率最高的是
a.
 b.
b. c.
c. d.
d.
(2)
 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(3)
 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为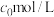 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为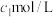 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。①写出溶液中
 分解生成
分解生成 的化学方程式:
的化学方程式:②
 时刻溶液中
时刻溶液中
 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
名校
9 . 铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(2)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①发生反应的离子方程式为___________ 。
②为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为_________
③欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要___________ (选填字母)。
(3)纳米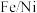 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:

①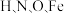 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是___________ 。
②反应ⅱ的离子方程式为___________ 。
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为___________ 。
(4)在 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。
已知:
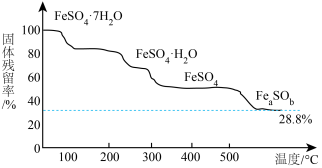
通过计算后,写出 受热分解的化学方程式
受热分解的化学方程式___________ 。
(1)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(2)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①发生反应的离子方程式为
②为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为③欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要(3)纳米
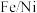 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:
①
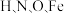 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是②反应ⅱ的离子方程式为
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为
(4)在
 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。已知:


通过计算后,写出
 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
2023-09-17更新
|
75次组卷
|
2卷引用:重庆市第十一中学校2024届高三第一次测试化学试题
名校
解题方法
10 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体 ,回答下列问题:
,回答下列问题: 的溶解度数据表
的溶解度数据表
(1)仪器A右侧玻璃导管的作用为___________ ,仪器A中使用饱和食盐水代替蒸馏水的目的是___________ 。
(2)装置乙的作用是除杂,写出 被除去的离子方程式
被除去的离子方程式___________ 。
(3)在装置丙中已加入催化剂,请写出生成 的化学方程式
的化学方程式___________ ,研究表明当硝酸的质量分数超过 或温度高于
或温度高于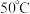 ,草酸的产率开始下降,其原因是
,草酸的产率开始下降,其原因是___________ 。
(4)装置丁的作用是___________ 。
(5)待反应结束后,从装置丙中分离出 晶体的操作为
晶体的操作为___________ 、___________ 、过滤、洗涤、低温干燥。
(6)草酸纯度的测定(杂质不与空气反应)
步骤1:称取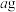 产品放置于管式炉中。
产品放置于管式炉中。
步骤2:将纯化后的空气 (已换算为标况)通入管式炉中与产品充分反应。
(已换算为标况)通入管式炉中与产品充分反应。
步骤3:测出混合气体中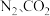 的体积分数分别为
的体积分数分别为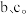
产品中草酸的质量分数为___________ ( 的摩尔质量为
的摩尔质量为 ,化为最简式)。
,化为最简式)。
 ,回答下列问题:
,回答下列问题:
 的溶解度数据表
的溶解度数据表温度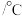 | 20 | 40 | 60 | 80 |
溶解度 | 9.52 | 21.5 | 44.3 | 84.5 |
(1)仪器A右侧玻璃导管的作用为
(2)装置乙的作用是除杂,写出
 被除去的离子方程式
被除去的离子方程式(3)在装置丙中已加入催化剂,请写出生成
 的化学方程式
的化学方程式 或温度高于
或温度高于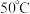 ,草酸的产率开始下降,其原因是
,草酸的产率开始下降,其原因是(4)装置丁的作用是
(5)待反应结束后,从装置丙中分离出
 晶体的操作为
晶体的操作为(6)草酸纯度的测定(杂质不与空气反应)
步骤1:称取
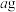 产品放置于管式炉中。
产品放置于管式炉中。步骤2:将纯化后的空气
 (已换算为标况)通入管式炉中与产品充分反应。
(已换算为标况)通入管式炉中与产品充分反应。步骤3:测出混合气体中
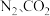 的体积分数分别为
的体积分数分别为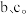
产品中草酸的质量分数为
 的摩尔质量为
的摩尔质量为 ,化为最简式)。
,化为最简式)。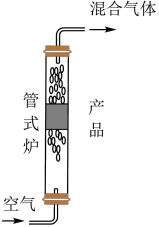
您最近半年使用:0次



