名校
解题方法
1 . 工业上利用石煤矿粉(主要含 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:

已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为 、
、 、
、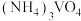 ;
;
②不同pH下,V(V)在溶液中的主要存在形式见下表:
③25℃时, 。
。
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)滤液Ⅰ的成分为_______ (填化学式);先“转沉”后“转化”的目的是_______ 。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到_______ 操作单元中循环使用。
(4)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①_______ 。②_______ ;25℃时,测得“转化”后,滤液中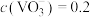 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少_______ mol·L 。
。
(5)“煅烧”时, 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为_______ 。
 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:
已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为
 、
、 、
、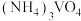 ;
;②不同pH下,V(V)在溶液中的主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 。
。回答下列问题:
(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ的成分为
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到
(4)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①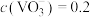 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少 。
。(5)“煅烧”时,
 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
您最近一年使用:0次
2023-02-08更新
|
2140次组卷
|
4卷引用:山东省济南市2023届高三下学期学情检测(一模)化学试题
22-23高三上·河北邯郸·期末
名校
解题方法
2 . 用软锰矿(主要成分是MnO2)制备纯净MnO2的工艺流程如下:
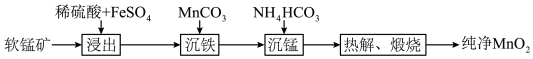
| A.“浸出”过程中参与反应的n(FeSO4):n(MnO2)为1:2 |
B.“沉锰”过程涉及:2HCO +Mn2+=MnCO3↓+H2O+CO2↑ +Mn2+=MnCO3↓+H2O+CO2↑ |
| C.“沉锰”过程中产物过滤后所得滤液可制造化肥 |
| D.“沉锰”和“热解、煅烧”过程生成的CO2可用来制备NH4HCO3 |
您最近一年使用:0次
2023-02-04更新
|
489次组卷
|
8卷引用:山东省济南市2022届高三3月高考模拟考试(一模)(不定项选择题)
(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(不定项选择题)河北省邯郸市2022-2023学年高三上学期期末考试化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题6-10)江苏省镇江第一中学2023-2024学年高三上学期期初阶段学情检测化学试题湖北省武汉市武钢三中2023-2024学年高三上学期8月月考化学试题吉林省郭尔罗斯蒙古族自治县第五高级中学2023-2024学年高三上学期10月月考化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题福建省厦门市国祺中学2023-2024学年高三上学期第三次月考化学试题
3 . 资料表明,氧化性:浓硝酸 稀硝酸,基于以下事实:
稀硝酸,基于以下事实:
I.稀硝酸不能氧化 ,而浓硝酸能将
,而浓硝酸能将 氧化成
氧化成 。
。
II.稀硝酸与磷化物反应时,只能将磷元素氧化成单质磷,而浓硝酸与磷化物反应时,能将磷元素氧化成 。
。
III.稀硝酸只能将 氧化成单质碘,而浓硝酸则能把
氧化成单质碘,而浓硝酸则能把 氧化成
氧化成
回答下列问题:
(1)某同学通过实验验证事实I,所用实验装置(夹持装置略)如图(实验前用 将装置中空气排尽):
将装置中空气排尽):

已知:氢氧化钠溶液不与 反应,能与
反应,能与 反应生成
反应生成 和
和 。
。
① 的作用是
的作用是_______ , 中反应的离子方程式为
中反应的离子方程式为_______ 。
②实验时,首先将 和
和 相连接,
相连接, 中的试剂为
中的试剂为_______ , 中观察到的现象是
中观察到的现象是_______ 。然后将 与
与 相连接,其目的是
相连接,其目的是_______ , 中观察到的现象是
中观察到的现象是_______ 。
(2)根据事实II,写出稀硝酸与磷化亚铜 反应的化学方程式为
反应的化学方程式为 稀
稀 ;被氧化的元素是
;被氧化的元素是_______ 。
(3)根据事实III,将 气体通入浓
气体通入浓 溶液中至过量,一段时间后溶液由无色变为黄褐色,写出生成使溶液显黄褐色的物质的离子方程式
溶液中至过量,一段时间后溶液由无色变为黄褐色,写出生成使溶液显黄褐色的物质的离子方程式_______ 。
(4)请说明浓硝酸、稀硝酸分别和铜反应时的最大区别_______ 。
 稀硝酸,基于以下事实:
稀硝酸,基于以下事实:I.稀硝酸不能氧化
 ,而浓硝酸能将
,而浓硝酸能将 氧化成
氧化成 。
。II.稀硝酸与磷化物反应时,只能将磷元素氧化成单质磷,而浓硝酸与磷化物反应时,能将磷元素氧化成
 。
。III.稀硝酸只能将
 氧化成单质碘,而浓硝酸则能把
氧化成单质碘,而浓硝酸则能把 氧化成
氧化成
回答下列问题:
(1)某同学通过实验验证事实I,所用实验装置(夹持装置略)如图(实验前用
 将装置中空气排尽):
将装置中空气排尽):
已知:氢氧化钠溶液不与
 反应,能与
反应,能与 反应生成
反应生成 和
和 。
。①
 的作用是
的作用是 中反应的离子方程式为
中反应的离子方程式为②实验时,首先将
 和
和 相连接,
相连接, 中的试剂为
中的试剂为 中观察到的现象是
中观察到的现象是 与
与 相连接,其目的是
相连接,其目的是 中观察到的现象是
中观察到的现象是(2)根据事实II,写出稀硝酸与磷化亚铜
 反应的化学方程式为
反应的化学方程式为 稀
稀 ;被氧化的元素是
;被氧化的元素是(3)根据事实III,将
 气体通入浓
气体通入浓 溶液中至过量,一段时间后溶液由无色变为黄褐色,写出生成使溶液显黄褐色的物质的离子方程式
溶液中至过量,一段时间后溶液由无色变为黄褐色,写出生成使溶液显黄褐色的物质的离子方程式(4)请说明浓硝酸、稀硝酸分别和铜反应时的最大区别
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 草酸(H2C2O4)及其盐类化合物在化学工业中有重要作用。请回答下列问题:
(1)实验室中可以在 用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
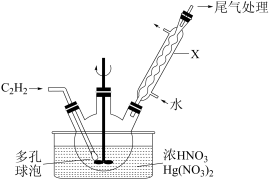
 的电子式为
的电子式为_______ ;仪器X的名称为_______ ;装置中浓硝酸的还原产物为 ,生成草酸的化学方程式为
,生成草酸的化学方程式为_______ ,若反应温度高于 ,生成草酸的速率会减慢,主要原因是
,生成草酸的速率会减慢,主要原因是_______ 。
(2)三草酸合铁酸钾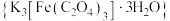 为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用
为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用 为原料制备三草酸合铁酸钾的步骤如下:
为原料制备三草酸合铁酸钾的步骤如下:
①称取 晶体,溶解,加硫酸酸化,边搅拌边加入
晶体,溶解,加硫酸酸化,边搅拌边加入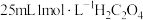 溶液,静置,析出黄色的
溶液,静置,析出黄色的 沉淀,过滤并洗涤沉淀
沉淀,过滤并洗涤沉淀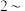 3次。
3次。
②将上述 沉淀溶解在
沉淀溶解在 饱和草酸钾溶液中,再加入
饱和草酸钾溶液中,再加入 饱和
饱和 溶液,保持溶液温度为
溶液,保持溶液温度为 ,缓慢滴加
,缓慢滴加 溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾
溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾 ,再加入
,再加入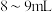 草酸溶液,控制
草酸溶液,控制 为
为 ,变为绿色透明的三草酸合铁酸钾溶液。
,变为绿色透明的三草酸合铁酸钾溶液。
③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体 次,干燥、称量。
次,干燥、称量。
其中生成 的化学方程式为
的化学方程式为_______ ;保持溶液温度为 所采用的加热方式是
所采用的加热方式是_______ ,加热至沸腾 的目的是
的目的是_______ ;洗涤晶体所用试剂为_______ 。
(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定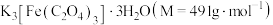 的纯度,进行如下实验:
的纯度,进行如下实验:
称取样品 ,加稀硫酸溶解后配成
,加稀硫酸溶解后配成 溶液。取
溶液。取 配制的溶液,用浓度为
配制的溶液,用浓度为 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 溶液
溶液 ,已知:
,已知: ,样品中
,样品中 的质量分数为
的质量分数为_______ (结果保留三位有效数字)。
(1)实验室中可以在
 用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如图所示。
 的电子式为
的电子式为 ,生成草酸的化学方程式为
,生成草酸的化学方程式为 ,生成草酸的速率会减慢,主要原因是
,生成草酸的速率会减慢,主要原因是(2)三草酸合铁酸钾
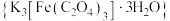 为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用
为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用 为原料制备三草酸合铁酸钾的步骤如下:
为原料制备三草酸合铁酸钾的步骤如下:①称取
 晶体,溶解,加硫酸酸化,边搅拌边加入
晶体,溶解,加硫酸酸化,边搅拌边加入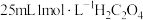 溶液,静置,析出黄色的
溶液,静置,析出黄色的 沉淀,过滤并洗涤沉淀
沉淀,过滤并洗涤沉淀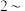 3次。
3次。②将上述
 沉淀溶解在
沉淀溶解在 饱和草酸钾溶液中,再加入
饱和草酸钾溶液中,再加入 饱和
饱和 溶液,保持溶液温度为
溶液,保持溶液温度为 ,缓慢滴加
,缓慢滴加 溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾
溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾 ,再加入
,再加入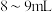 草酸溶液,控制
草酸溶液,控制 为
为 ,变为绿色透明的三草酸合铁酸钾溶液。
,变为绿色透明的三草酸合铁酸钾溶液。③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体
 次,干燥、称量。
次,干燥、称量。其中生成
 的化学方程式为
的化学方程式为 所采用的加热方式是
所采用的加热方式是 的目的是
的目的是(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定
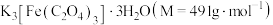 的纯度,进行如下实验:
的纯度,进行如下实验:称取样品
 ,加稀硫酸溶解后配成
,加稀硫酸溶解后配成 溶液。取
溶液。取 配制的溶液,用浓度为
配制的溶液,用浓度为 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 溶液
溶液 ,已知:
,已知: ,样品中
,样品中 的质量分数为
的质量分数为
您最近一年使用:0次
2023-01-20更新
|
438次组卷
|
4卷引用:山东省济南市2022届高三3月高考模拟考试(一模)(实验探究题)
22-23高三上·山东菏泽·期末
名校
解题方法
5 . 钌 粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料(废料中钌主要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制备高纯钌粉的流程如下:
粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料(废料中钌主要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制备高纯钌粉的流程如下:
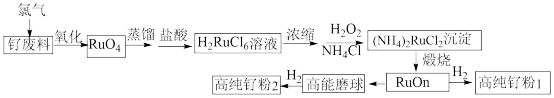
已知:i.钌在碱性条件下被氯气氧化为 ,
, 是有毒的挥发性物质,用盐酸吸收得到红色
是有毒的挥发性物质,用盐酸吸收得到红色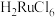 溶液,其中还含有少量
溶液,其中还含有少量 ;
;
ii.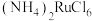 易溶于水,微溶于酒精。
易溶于水,微溶于酒精。
回答下列问题:
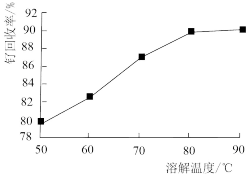
(1)钌废料在碱性条件下被氯气氧化的离子方程式为_______ ;钌废料氧化时,随着温度的升高,钌的回收率变化如图所示。综合考虑,确定氧化时的温度以_______ ℃为宜。
(2)用盐酸吸收蒸馏产物时发生主要反应的化学方程式是_______ 。
(3)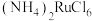 沉淀用乙醇洗涤而不用水洗涤的优点是
沉淀用乙醇洗涤而不用水洗涤的优点是_______ 。
(4)加入 的主要作用是
的主要作用是_______ ,同时又调节了溶液的 ,有利于沉淀反应的发生。流程中可以循环利用的物质
,有利于沉淀反应的发生。流程中可以循环利用的物质_______ 。
(5)煅烧的过程分为两步:第1步是氯钌酸铵分解生成钌单质和一种无毒的气体单质,同时有两种化合物生成;第2步是钌单质与氧气反应生成钌的氧化物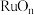 (
(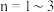 )。第1步的化学方程式是
)。第1步的化学方程式是_______ 。
 粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料(废料中钌主要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制备高纯钌粉的流程如下:
粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以钌废料(废料中钌主要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制备高纯钌粉的流程如下: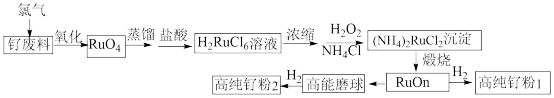
已知:i.钌在碱性条件下被氯气氧化为
 ,
, 是有毒的挥发性物质,用盐酸吸收得到红色
是有毒的挥发性物质,用盐酸吸收得到红色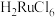 溶液,其中还含有少量
溶液,其中还含有少量 ;
;ii.
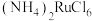 易溶于水,微溶于酒精。
易溶于水,微溶于酒精。回答下列问题:
(1)钌废料在碱性条件下被氯气氧化的离子方程式为

(2)用盐酸吸收蒸馏产物时发生主要反应的化学方程式是
(3)
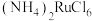 沉淀用乙醇洗涤而不用水洗涤的优点是
沉淀用乙醇洗涤而不用水洗涤的优点是(4)加入
 的主要作用是
的主要作用是 ,有利于沉淀反应的发生。流程中可以循环利用的物质
,有利于沉淀反应的发生。流程中可以循环利用的物质(5)煅烧的过程分为两步:第1步是氯钌酸铵分解生成钌单质和一种无毒的气体单质,同时有两种化合物生成;第2步是钌单质与氧气反应生成钌的氧化物
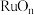 (
(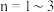 )。第1步的化学方程式是
)。第1步的化学方程式是
您最近一年使用:0次
2023-01-16更新
|
275次组卷
|
5卷引用:山东省济南市2022届高三3月高考模拟考试(一模)(工业流程题)
(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(工业流程题)山东省鄄城县第一中学2022-2023学年高三上学期期末考试化学试题山东省菏泽市郓城县实验中学2022-2023学年高三上学期期末考试化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(工业流程题)河南省南阳市新野县第一高级中学校2023-2024学年高三上学期12月月考化学试题
名校
6 . 亚氯酸钠( )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:① 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 ;
;
②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1) 发生器中反应的离子方程式为
发生器中反应的离子方程式为_______ 。
(2)通入空气的作用可能是_______ 。
(3)吸收塔内发生反应的离子方程式为_______ ;吸收塔内的温度不能超过20℃,其目的是_______ 。
(4)240g/LNaOH溶液的物质的量浓度为_______ mol/L。
(5)从滤液中得到 粗晶体的实验操作依次是
粗晶体的实验操作依次是_______ (填序号)。
A.蒸发浓缩 B.蒸馏 C.过滤 D.灼烧 E.冷却结晶
 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
已知:①
 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 ;
;②纯
 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
易分解爆炸,一般用稀有气体或空气稀释到10%以下。(1)
 发生器中反应的离子方程式为
发生器中反应的离子方程式为(2)通入空气的作用可能是
(3)吸收塔内发生反应的离子方程式为
(4)240g/LNaOH溶液的物质的量浓度为
(5)从滤液中得到
 粗晶体的实验操作依次是
粗晶体的实验操作依次是A.蒸发浓缩 B.蒸馏 C.过滤 D.灼烧 E.冷却结晶
您最近一年使用:0次
2023-01-14更新
|
481次组卷
|
2卷引用:山东省实验中学2022-2023学年高一上学期期末考试化学试题
名校
7 . 已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。
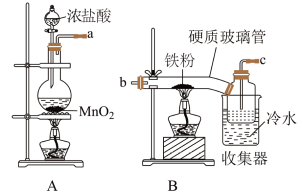
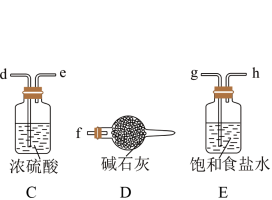
(1)反应开始时,应先点燃_______ 装置的酒精灯(填“A”或“B”)。
(2)碱石灰的作用是_______ 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

淡红色溶液中加入过量 后溶液红色加深的原因请用离子方程式表达
后溶液红色加深的原因请用离子方程式表达_______ 。
(4)已知红色褪去的同时有气体生成,经检验为 。该小组同学对红色褪去的原因进行探究。通过查阅资料获知:
。该小组同学对红色褪去的原因进行探究。通过查阅资料获知: 在
在 催化作用下可分解;
催化作用下可分解; 可被氧化剂氧化。据此进行了如下实验:
可被氧化剂氧化。据此进行了如下实验:
①取褪色后溶液三份,第一份滴加 溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和
溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和 溶液,产生白色沉淀。
溶液,产生白色沉淀。
②另取同物质的量浓度的 溶液滴加2滴试剂X,溶液变红,再通入
溶液滴加2滴试剂X,溶液变红,再通入 ,无明显变化。
,无明显变化。
实验①说明_______ (填离子符号)发生了反应;实验②的目的是排除_______ ;得出结论:红色褪去的原因是_______ 。


(1)反应开始时,应先点燃
(2)碱石灰的作用是
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

淡红色溶液中加入过量
 后溶液红色加深的原因请用离子方程式表达
后溶液红色加深的原因请用离子方程式表达(4)已知红色褪去的同时有气体生成,经检验为
 。该小组同学对红色褪去的原因进行探究。通过查阅资料获知:
。该小组同学对红色褪去的原因进行探究。通过查阅资料获知: 在
在 催化作用下可分解;
催化作用下可分解; 可被氧化剂氧化。据此进行了如下实验:
可被氧化剂氧化。据此进行了如下实验:①取褪色后溶液三份,第一份滴加
 溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和
溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和 溶液,产生白色沉淀。
溶液,产生白色沉淀。②另取同物质的量浓度的
 溶液滴加2滴试剂X,溶液变红,再通入
溶液滴加2滴试剂X,溶液变红,再通入 ,无明显变化。
,无明显变化。实验①说明
您最近一年使用:0次
2023-01-14更新
|
571次组卷
|
3卷引用:山东省实验中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4) 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2∶1时,则表现酸性与表现氧化性的
和NO的个数之比为2∶1时,则表现酸性与表现氧化性的 的个数之比为
的个数之比为_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)
 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2∶1时,则表现酸性与表现氧化性的
和NO的个数之比为2∶1时,则表现酸性与表现氧化性的 的个数之比为
的个数之比为
您最近一年使用:0次
2023-01-14更新
|
435次组卷
|
2卷引用:山东省实验中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 水体中存在的 、
、 等致癌阴离子对人体健康构成严重威胁。采用
等致癌阴离子对人体健康构成严重威胁。采用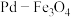 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的
消除酸性废水中的 、
、 。
。 中含有
中含有 、
、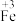 ,分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
,分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
 、
、 等致癌阴离子对人体健康构成严重威胁。采用
等致癌阴离子对人体健康构成严重威胁。采用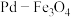 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的
消除酸性废水中的 、
、 。
。 中含有
中含有 、
、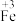 ,分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
,分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
| A.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用 |
B.过程③发生的反应为 |
C.过程④每生成 ,转移3mol电子 ,转移3mol电子 |
| D.用该法处理后水体的酸性增强 |
您最近一年使用:0次
2023-01-14更新
|
410次组卷
|
2卷引用:山东省实验中学2022-2023学年高一上学期期末考试化学试题
名校
10 . 以硫酸渣(主要含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如图:

已知:SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应。
(1)“酸溶”中加快溶解的方法可采取加热、_______ 、适当增大硫酸浓度或粉碎硫酸渣等方法。
(2)“酸溶”过程中的主要反应的离子方程式为_______ ;“还原”过程中的离子方程式为_______ 。
(3)“沉铁”过程中生成Fe(OH)2的化学方程式为_______ 。
(4)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,虽然能缩短氧化时间,缺点可能是_______ 。

已知:SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应。
(1)“酸溶”中加快溶解的方法可采取加热、
(2)“酸溶”过程中的主要反应的离子方程式为
(3)“沉铁”过程中生成Fe(OH)2的化学方程式为
(4)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,虽然能缩短氧化时间,缺点可能是
您最近一年使用:0次



