名校
解题方法
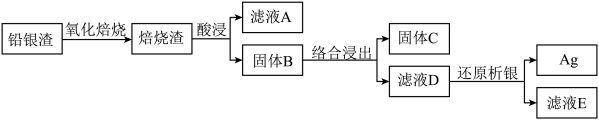
1 . 从铅银渣(含Pb、Ag、Cu等金属元素)中提取银的流程如下: 形成[Ag(SO3)2]3−。
形成[Ag(SO3)2]3−。
(1)“酸浸”时,使用H2SO4、NaCl和NaNO3的混合液作为浸出剂。
①加入NaNO3的作用___________ 。
②固体B含有___________ 。
(2)用氨水和水合肼(N2H4·H2O)进行“络合浸出”和“还原析银”。
①氨水“络合浸出”的化学方程式是___________ 。
②将水合肼“还原析银”反应的离子方程式补充完整:___________ 。
□ ___________+ N2H4·H2O =N2↑ + H2O + □ ___________ + □ ___________ + □ NH3↑
(3)用Na2SO3和甲醛进行“络合浸出”和“还原析银”。
①亚硫酸钠“络合浸出”时,银浸出率和溶液pH、浸出时间的关系分别如下图所示,解释银浸出率随溶液pH增大先升高后降低的原因___________ ;分析浸出时间超过4 h,银浸出率降低的原因___________ 。___________ 。
 形成[Ag(SO3)2]3−。
形成[Ag(SO3)2]3−。(1)“酸浸”时,使用H2SO4、NaCl和NaNO3的混合液作为浸出剂。
①加入NaNO3的作用
②固体B含有
(2)用氨水和水合肼(N2H4·H2O)进行“络合浸出”和“还原析银”。
①氨水“络合浸出”的化学方程式是
②将水合肼“还原析银”反应的离子方程式补充完整:
□ ___________+ N2H4·H2O =N2↑ + H2O + □ ___________ + □ ___________ + □ NH3↑
(3)用Na2SO3和甲醛进行“络合浸出”和“还原析银”。
①亚硫酸钠“络合浸出”时,银浸出率和溶液pH、浸出时间的关系分别如下图所示,解释银浸出率随溶液pH增大先升高后降低的原因

您最近一年使用:0次
2024-04-01更新
|
655次组卷
|
5卷引用:北京市石景山区2024届高三期中考试(一模)化学试卷
北京市石景山区2024届高三期中考试(一模)化学试卷(已下线)提升练07 工艺流程综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)北京市西城区2024届高三下学期第三次模拟测试化学试题北京市第一六六中学2023-2024学年高三下学期高考模拟测试(三模)化学试题
名校
2 . 下列反应对应的离子方程式正确的是
A.乙酰胺与盐酸混合共热: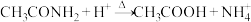 |
B.硫化钠溶液在空气中氧化变质: |
C.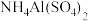 溶液与足量 溶液与足量 溶液反应: 溶液反应: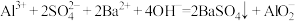 |
D.证明 、 、 、 、 三者的酸性强弱: 三者的酸性强弱: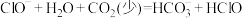 |
您最近一年使用:0次
2024-04-22更新
|
680次组卷
|
4卷引用:2024届河北省邢台市部分高中高三下学期二模化学试题
2024届河北省邢台市部分高中高三下学期二模化学试题福建省福州市八县市一中2024届高三下学期模拟联考化学试题河北衡水中学2023-2024学年高三下学期自我提升中期测试化学试题(已下线)专题1 物质及其变化-离子反应、离子方程式
2023高三·全国·专题练习
名校
解题方法
3 . 以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备NixOy和碳酸亚钴(CoCO3)的工艺流程如图。

| A.“滤渣1”的主要成分是H2SiO3、BaSO4 |
B.“氧化”时的离子反应为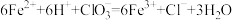 |
| C.“调pH"过程中形成黄钠铁矾渣,Na2CO3必须过量 |
D.“沉钴”过程发生的反应为 |
您最近一年使用:0次
2023-02-01更新
|
681次组卷
|
3卷引用:专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)河南省实验中学2023~2024学年高一上学期开学考试化学试题湖南省岳阳市岳阳县第一中学2024-2025学年高一上学期开学考试化学试题
解题方法
4 . 某学习小组对 与
与 的反应进行了研究。
的反应进行了研究。___________ 。
(2)利用如图装置完成 与
与 制取氮氧化物的反应。实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体。
制取氮氧化物的反应。实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体。
①为排尽整套装置内的空气,先打开弹簧夹,通入_______ (填化学式),一段时间后关闭弹簧夹。
②C中液面上方为红棕色气体,其原因是________ (用化学方程式表示)。
(3)学习小组在做铜与硝酸反应的实验时观察到了以下现象:实验Ⅰ中蓝色溶液A遇铜片立即产生气泡,而相同条件下实验Ⅱ中 硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
①假设1:___________ (填化学式)对该反应有催化作用。
实验验证:向 硝酸中加入少量硝酸铜固体,溶液呈蓝色,放入铜片,无明显变化。
硝酸中加入少量硝酸铜固体,溶液呈蓝色,放入铜片,无明显变化。
结论:假设1不成立。
②假设2: 对该反应有催化作用。
对该反应有催化作用。
向A中鼓入 数分钟得溶液C,相同条件下,铜片与A、C溶液的反应速率:
数分钟得溶液C,相同条件下,铜片与A、C溶液的反应速率: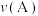
______ 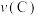 (填“
(填“ ”“
”“ ”“
”“ ”)。实验证明假设2成立。
”)。实验证明假设2成立。
③经检验,蓝色溶液A中还含有少量亚硝酸 。
。
设计实验证明 也对该反应有催化作用。操作和预期的现象是:
也对该反应有催化作用。操作和预期的现象是:___________ 。向含有铜片的溶液B中___________ 。
实验总结: 和
和 对铜与硝酸的反应都有催化作用。
对铜与硝酸的反应都有催化作用。
(4)请推测 与浓硝酸反应中
与浓硝酸反应中 和
和 参与的可能的催化过程:
参与的可能的催化过程:
①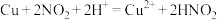 ②
②___________ 。
 与
与 的反应进行了研究。
的反应进行了研究。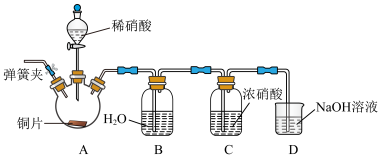
(2)利用如图装置完成
 与
与 制取氮氧化物的反应。实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体。
制取氮氧化物的反应。实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体。①为排尽整套装置内的空气,先打开弹簧夹,通入
②C中液面上方为红棕色气体,其原因是
(3)学习小组在做铜与硝酸反应的实验时观察到了以下现象:实验Ⅰ中蓝色溶液A遇铜片立即产生气泡,而相同条件下实验Ⅱ中
 硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:实验Ⅰ: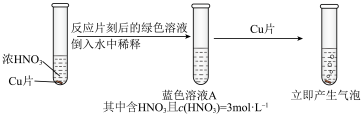
实验Ⅱ: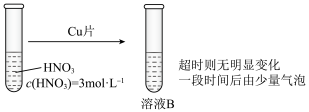
①假设1:
实验验证:向
 硝酸中加入少量硝酸铜固体,溶液呈蓝色,放入铜片,无明显变化。
硝酸中加入少量硝酸铜固体,溶液呈蓝色,放入铜片,无明显变化。结论:假设1不成立。
②假设2:
 对该反应有催化作用。
对该反应有催化作用。向A中鼓入
 数分钟得溶液C,相同条件下,铜片与A、C溶液的反应速率:
数分钟得溶液C,相同条件下,铜片与A、C溶液的反应速率: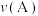
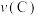 (填“
(填“ ”“
”“ ”“
”“ ”)。实验证明假设2成立。
”)。实验证明假设2成立。③经检验,蓝色溶液A中还含有少量亚硝酸
 。
。设计实验证明
 也对该反应有催化作用。操作和预期的现象是:
也对该反应有催化作用。操作和预期的现象是:实验总结:
 和
和 对铜与硝酸的反应都有催化作用。
对铜与硝酸的反应都有催化作用。(4)请推测
 与浓硝酸反应中
与浓硝酸反应中 和
和 参与的可能的催化过程:
参与的可能的催化过程:①
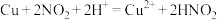 ②
②
您最近一年使用:0次
2024-01-22更新
|
632次组卷
|
3卷引用:北京房山区2023-2024学年高三上学期期末化学试题
北京房山区2023-2024学年高三上学期期末化学试题(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)北京市房山区2023-2024学年高三上学期期末检测化学试题
解题方法
5 . 全钒液流电池正极废液中含有的离子是 。以该废液为原料经过氧化、调
。以该废液为原料经过氧化、调 、沉钒、煅烧可以制取
、沉钒、煅烧可以制取 。
。
(1)氧化:向正极废液中加入 将
将 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:________ 。
(2)调 :向氧化后的溶液中加入
:向氧化后的溶液中加入 调节溶液
调节溶液 ,溶液中V(
,溶液中V( 价)会以
价)会以 等形式存在。随pH的升高,溶液中
等形式存在。随pH的升高,溶液中 的值将
的值将________ (填“增大”“减小”或“保持不变”),判断的方法是________ 。
(3)沉钒:不同 时,向溶液中加入
时,向溶液中加入 ,可得到不同类型的含钒沉淀。
,可得到不同类型的含钒沉淀。
①其他条件一定,控制溶液 在2~5之间,向溶液中加入
在2~5之间,向溶液中加入 ,沉钒率和沉淀的X射线衍射图分别如图1和图2所示。
,沉钒率和沉淀的X射线衍射图分别如图1和图2所示。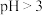 时,
时, 越大,溶液的沉钒率越低的原因是
越大,溶液的沉钒率越低的原因是________ 。
②向 的溶液中(此时
的溶液中(此时 主要以
主要以 存在)加入过量
存在)加入过量 溶液,生成
溶液,生成 沉淀。加入过量
沉淀。加入过量 溶液的目的是。已知:
溶液的目的是。已知: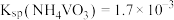 。
。 固体制取
固体制取 时,需在有氧条件下进行,原因是
时,需在有氧条件下进行,原因是________ 。
(5) 是一种相变材料,其一种晶胞(部分
是一种相变材料,其一种晶胞(部分 原子未标出)的结构如图3所示,在图中合适位置补充其余
原子未标出)的结构如图3所示,在图中合适位置补充其余 原子
原子________ 。
 。以该废液为原料经过氧化、调
。以该废液为原料经过氧化、调 、沉钒、煅烧可以制取
、沉钒、煅烧可以制取 。
。(1)氧化:向正极废液中加入
 将
将 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(2)调
 :向氧化后的溶液中加入
:向氧化后的溶液中加入 调节溶液
调节溶液 ,溶液中V(
,溶液中V( 价)会以
价)会以 等形式存在。随pH的升高,溶液中
等形式存在。随pH的升高,溶液中 的值将
的值将(3)沉钒:不同
 时,向溶液中加入
时,向溶液中加入 ,可得到不同类型的含钒沉淀。
,可得到不同类型的含钒沉淀。①其他条件一定,控制溶液
 在2~5之间,向溶液中加入
在2~5之间,向溶液中加入 ,沉钒率和沉淀的X射线衍射图分别如图1和图2所示。
,沉钒率和沉淀的X射线衍射图分别如图1和图2所示。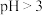 时,
时, 越大,溶液的沉钒率越低的原因是
越大,溶液的沉钒率越低的原因是②向
 的溶液中(此时
的溶液中(此时 主要以
主要以 存在)加入过量
存在)加入过量 溶液,生成
溶液,生成 沉淀。加入过量
沉淀。加入过量 溶液的目的是。已知:
溶液的目的是。已知: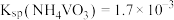 。
。
 固体制取
固体制取 时,需在有氧条件下进行,原因是
时,需在有氧条件下进行,原因是(5)
 是一种相变材料,其一种晶胞(部分
是一种相变材料,其一种晶胞(部分 原子未标出)的结构如图3所示,在图中合适位置补充其余
原子未标出)的结构如图3所示,在图中合适位置补充其余 原子
原子
您最近一年使用:0次
2024-03-12更新
|
612次组卷
|
2卷引用:江苏省南通市如皋市2023-2024学年高三下学期2月适应性考试(一)化学试题
名校
6 . 以高硫铝土矿(主要成分为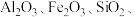 少量
少量 )为原料,生产
)为原料,生产 的部分工艺流程如下:
的部分工艺流程如下: 是一种难溶于水的酸性氧化物,
是一种难溶于水的酸性氧化物, 酸性比碳酸弱,难溶于水。下列说法
酸性比碳酸弱,难溶于水。下列说法不正确 的是
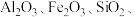 少量
少量 )为原料,生产
)为原料,生产 的部分工艺流程如下:
的部分工艺流程如下: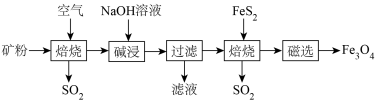
 是一种难溶于水的酸性氧化物,
是一种难溶于水的酸性氧化物, 酸性比碳酸弱,难溶于水。下列说法
酸性比碳酸弱,难溶于水。下列说法| A.高硫铝土矿加工成粉状,可以加快焙烧速率,又能提高原料利用率 |
B.碱浸过程 发生的反应: 发生的反应: |
C.向过滤后得到的滤液中通入过量 ,得到的沉淀为 ,得到的沉淀为 |
D.若由 与 与 在无氧条件下焙烧制得 在无氧条件下焙烧制得 ,则两者物质的量之比为 ,则两者物质的量之比为 |
您最近一年使用:0次
2023-06-27更新
|
703次组卷
|
4卷引用:江苏省连云港市2022-2023学年高一下学期6月期末考试化学试题
江苏省连云港市2022-2023学年高一下学期6月期末考试化学试题江西省赣州市全南中学2023-2024学年高二上学期开学考试化学试题(已下线)重难点05 铁及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)河南省新乡市原阳县第一高级中学2023-2024学年高一下学期5月月考化学试题
名校
解题方法
7 . 宏观辨识与微观探析是化学学科核心素养之一、下列反应方程式书写正确的是
A.将少量 通入 通入 溶液中: 溶液中: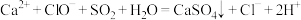 |
B.向甲醛溶液中加入足量的银氨溶液并加热: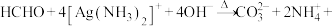  |
C.向摩尔盐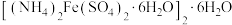 溶液中加入NaOH溶液至 溶液中加入NaOH溶液至 刚好反应完全: 刚好反应完全: |
D.往酸性 溶液中加入难溶于水的 溶液中加入难溶于水的 固体,溶液出现紫红色: 固体,溶液出现紫红色: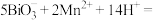 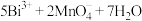 |
您最近一年使用:0次
2024-05-09更新
|
639次组卷
|
5卷引用:辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷
辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷湖北省十堰市2023-2024学年高三下学期4月调研考试化学试题2024届南昌市第十九中学高三下学期模拟预测化学试题(已下线)第02讲 离子反应、离子方程式(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)(已下线)专题1 物质及其变化-离子反应、离子方程式
8 . 以软锰矿(主要成分为 ,含少量
,含少量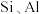 等的氧化物)为原料,某研究所设计由软锰矿制备
等的氧化物)为原料,某研究所设计由软锰矿制备 的生产流程如下:
的生产流程如下: 固体和溶液的颜色均为墨绿色。
固体和溶液的颜色均为墨绿色。
回答下列问题:
(1)“熔融、煅烧”时, 参与反应的化学方程式为
参与反应的化学方程式为___________ 。
(2)向“浸取”液中通入 调节其
调节其 ,经“过滤”得滤渣Ⅰ,滤渣Ⅰ的成分为
,经“过滤”得滤渣Ⅰ,滤渣Ⅰ的成分为_______ (填化学式)。
(3)锰元素的氧化态-吉布斯自由能图如图所示,该图具有多方面的应用。 是锰的最稳定态,则在碱性溶液中
是锰的最稳定态,则在碱性溶液中___________ (填化学式)是锰的最稳定态。
②可预测歧化反应发生的可能性。若某氧化态位于它相邻两氧化态连线的上方,则该氧化态不稳定,能发生歧化反应,生成其相邻两氧化态。反之,若某氧化态位于它相邻两氧化态连线的下方,则该氧化态是相对稳定的。由图可知, 在
在________ (填“酸性”或“碱性”)环境中更易发生歧化反应,由此可知,“歧化”时加入冰醋酸的目的是___________ (结合化学平衡移动原理解释)。“歧化”时,下列酸可以用来代替冰醋酸的是___________ (填字母)。
a.稀硫酸 b.亚硫酸 c.氢溴酸 d.乙二酸
(4)“结晶”时,当___________ (填现象)时,停止加热,待自然冷却后,过滤即可获得紫黑色 晶体。
晶体。
(5)实验室用草酸标准溶液测定产品中高锰酸钾的纯度(已知:杂质不参与反应),进行了如下操作:
步骤ⅰ.配制 的标准氢氧化钠溶液;
的标准氢氧化钠溶液;
步骤ⅱ.取草酸溶液 ,加入几滴酚酞溶液,用
,加入几滴酚酞溶液,用 的标准氢氧化钠溶液标定,消耗氢氧化钠溶液
的标准氢氧化钠溶液标定,消耗氢氧化钠溶液 ;
;
步骤ⅲ.取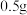 样品溶于水,滴入几滴稀硫酸酸化,用已标定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液
样品溶于水,滴入几滴稀硫酸酸化,用已标定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液 。
。
①样品中高锰酸钾的纯度为___________ 。
②高锰酸钾和草酸反应接近滴定终点时速率较慢,需用水浴加热。若不加热,测定出的高锰酸钾的纯度会偏___________ (填“大”或“小”)。
 ,含少量
,含少量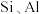 等的氧化物)为原料,某研究所设计由软锰矿制备
等的氧化物)为原料,某研究所设计由软锰矿制备 的生产流程如下:
的生产流程如下: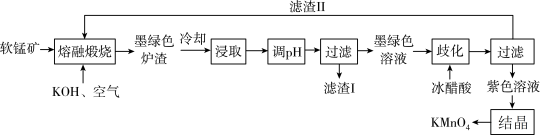
 固体和溶液的颜色均为墨绿色。
固体和溶液的颜色均为墨绿色。回答下列问题:
(1)“熔融、煅烧”时,
 参与反应的化学方程式为
参与反应的化学方程式为(2)向“浸取”液中通入
 调节其
调节其 ,经“过滤”得滤渣Ⅰ,滤渣Ⅰ的成分为
,经“过滤”得滤渣Ⅰ,滤渣Ⅰ的成分为(3)锰元素的氧化态-吉布斯自由能图如图所示,该图具有多方面的应用。
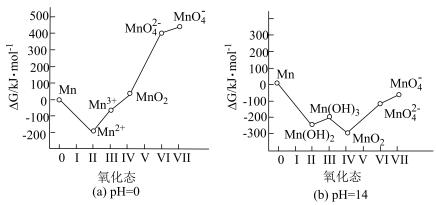
 是锰的最稳定态,则在碱性溶液中
是锰的最稳定态,则在碱性溶液中②可预测歧化反应发生的可能性。若某氧化态位于它相邻两氧化态连线的上方,则该氧化态不稳定,能发生歧化反应,生成其相邻两氧化态。反之,若某氧化态位于它相邻两氧化态连线的下方,则该氧化态是相对稳定的。由图可知,
 在
在a.稀硫酸 b.亚硫酸 c.氢溴酸 d.乙二酸
(4)“结晶”时,当
 晶体。
晶体。(5)实验室用草酸标准溶液测定产品中高锰酸钾的纯度(已知:杂质不参与反应),进行了如下操作:
步骤ⅰ.配制
 的标准氢氧化钠溶液;
的标准氢氧化钠溶液;步骤ⅱ.取草酸溶液
 ,加入几滴酚酞溶液,用
,加入几滴酚酞溶液,用 的标准氢氧化钠溶液标定,消耗氢氧化钠溶液
的标准氢氧化钠溶液标定,消耗氢氧化钠溶液 ;
;步骤ⅲ.取
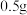 样品溶于水,滴入几滴稀硫酸酸化,用已标定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液
样品溶于水,滴入几滴稀硫酸酸化,用已标定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液 。
。①样品中高锰酸钾的纯度为
②高锰酸钾和草酸反应接近滴定终点时速率较慢,需用水浴加热。若不加热,测定出的高锰酸钾的纯度会偏
您最近一年使用:0次
2023-12-15更新
|
604次组卷
|
5卷引用:四川省成都市石室中学2024届高三上学期一诊模拟考试理科综合化学试题
名校
解题方法
9 . 向仅含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法错误的是
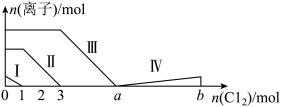
| A.线段Ⅰ、Ⅱ、Ⅲ、Ⅳ分别代表I-、Fe2+、Br-、HIO3的变化情况 |
| B.Fe2+、I-和Br-的物质的量之比为1∶2∶3 |
| C.根据图像可计算b=11 |
| D.线段Ⅳ对应的反应中氧化剂和还原剂的物质的量之比是5∶1 |
您最近一年使用:0次
2023-08-14更新
|
811次组卷
|
6卷引用:河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题
河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题 山东省日照市五莲县第一中学2024届高三上学期阶段性测试化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)第04讲 氧化还原反应的基本概念和规律考点专练第10讲 铁及其重要化合物考点专练
解题方法
10 . 钛酸钡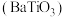 是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为
是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为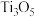 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备 的工业流程如下:
的工业流程如下: 在溶液中呈绿色;
在溶液中呈绿色; 是强电解质;
是强电解质;
②部分金属离子开始沉淀的 如下表:
如下表:
回答下列问题:
(1)“碱浸”操作过程中除去的杂质为_______ 。
(2)“水洗”过程中 与水发生离子交换反应:
与水发生离子交换反应: ,滤液2呈绿色,经除杂处理后可在
,滤液2呈绿色,经除杂处理后可在_______ (操作单元名称)循环利用,“熔盐反应”过程中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)“酸溶”过程中 (
( 溶液质量浓度)及F(
溶液质量浓度)及F( 溶液酸度)与w(
溶液酸度)与w( 质量分数)之间的关系如图所示。当
质量分数)之间的关系如图所示。当 值恒定时,随
值恒定时,随 溶液质量浓度增大,所需硫酸的质量分数
溶液质量浓度增大,所需硫酸的质量分数_______ (填“增大”“减小”或“不变”)。 目的是调节溶液
目的是调节溶液 ,可适当提高水解速率。已知:
,可适当提高水解速率。已知: ,水解反应
,水解反应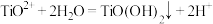 的平衡常数
的平衡常数
_______ ;“转化”过程加入铁粉的目的是_______ ,滤液3中含有的金属阳离子有_______ 。
(5)“共沉淀”过程发生反应: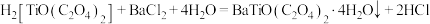 ,“灼烧”时隔绝空气,发生反应的化学方程式为
,“灼烧”时隔绝空气,发生反应的化学方程式为_______ 。
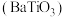 是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为
是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。用高钛渣(主要成分为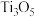 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备 的工业流程如下:
的工业流程如下: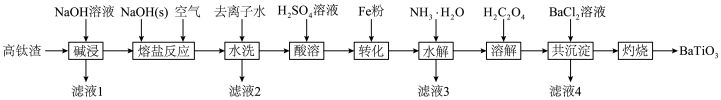
 在溶液中呈绿色;
在溶液中呈绿色; 是强电解质;
是强电解质;②部分金属离子开始沉淀的
 如下表:
如下表:| 金属离子 |  |  |  |
开始沉淀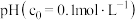 | 1.9 | 7.0 | 9.1 |
(1)“碱浸”操作过程中除去的杂质为
(2)“水洗”过程中
 与水发生离子交换反应:
与水发生离子交换反应: ,滤液2呈绿色,经除杂处理后可在
,滤液2呈绿色,经除杂处理后可在 发生反应的离子方程式为
发生反应的离子方程式为(3)“酸溶”过程中
 (
( 溶液质量浓度)及F(
溶液质量浓度)及F( 溶液酸度)与w(
溶液酸度)与w( 质量分数)之间的关系如图所示。当
质量分数)之间的关系如图所示。当 值恒定时,随
值恒定时,随 溶液质量浓度增大,所需硫酸的质量分数
溶液质量浓度增大,所需硫酸的质量分数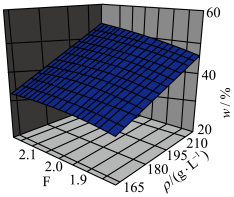
 目的是调节溶液
目的是调节溶液 ,可适当提高水解速率。已知:
,可适当提高水解速率。已知: ,水解反应
,水解反应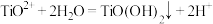 的平衡常数
的平衡常数
(5)“共沉淀”过程发生反应:
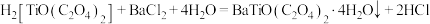 ,“灼烧”时隔绝空气,发生反应的化学方程式为
,“灼烧”时隔绝空气,发生反应的化学方程式为
您最近一年使用:0次
2024-03-23更新
|
568次组卷
|
2卷引用:山东省潍坊市2023-2024学年高三下学期一模化学试题



