名校
1 . 白硼钙石的主要成分是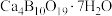 (含有少量
(含有少量 、FeO、
、FeO、 和
和 等杂质),利用白硼钙石制取强还原剂
等杂质),利用白硼钙石制取强还原剂 的工艺流程如下:
的工艺流程如下: 微溶于水,易溶于乙醇;偏硼酸钠(
微溶于水,易溶于乙醇;偏硼酸钠( )易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。
)易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。
(1) 中H的化合价为
中H的化合价为_________ ,该物质所含的化学键类型有_________________ 。
(2)写出“酸浸过滤”中发生的主要化学反应方程式______________________________ 。
(3)“气体”的主要成分为________________ 。“滤渣1”的主要成分是___________________ 。
(4)“操作X”为____________________________ 。
(5)写出“反应Y”的化学方程式________________________________________ 。
(6)“有效氢含量”(即:每克含氢还原剂的还原能力相当于多少克 的还原能力)可用衡量含氢还原剂的还原能力,则
的还原能力)可用衡量含氢还原剂的还原能力,则 的有效氢含量为
的有效氢含量为__________ (保留2位有效数字)。
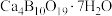 (含有少量
(含有少量 、FeO、
、FeO、 和
和 等杂质),利用白硼钙石制取强还原剂
等杂质),利用白硼钙石制取强还原剂 的工艺流程如下:
的工艺流程如下:
 微溶于水,易溶于乙醇;偏硼酸钠(
微溶于水,易溶于乙醇;偏硼酸钠( )易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。
)易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。(1)
 中H的化合价为
中H的化合价为(2)写出“酸浸过滤”中发生的主要化学反应方程式
(3)“气体”的主要成分为
(4)“操作X”为
(5)写出“反应Y”的化学方程式
(6)“有效氢含量”(即:每克含氢还原剂的还原能力相当于多少克
 的还原能力)可用衡量含氢还原剂的还原能力,则
的还原能力)可用衡量含氢还原剂的还原能力,则 的有效氢含量为
的有效氢含量为
您最近一年使用:0次
名校
2 . 二氧化氯( )是一种黄绿色到橙黄色的气体,极易溶于水,体积分数大于10%时,易发生爆炸,是一种无毒的绿色消毒剂。实验室可用下图所示装置(夹持仪器已省略)制备
)是一种黄绿色到橙黄色的气体,极易溶于水,体积分数大于10%时,易发生爆炸,是一种无毒的绿色消毒剂。实验室可用下图所示装置(夹持仪器已省略)制备 水溶液。下列说法错误的是
水溶液。下列说法错误的是
 )是一种黄绿色到橙黄色的气体,极易溶于水,体积分数大于10%时,易发生爆炸,是一种无毒的绿色消毒剂。实验室可用下图所示装置(夹持仪器已省略)制备
)是一种黄绿色到橙黄色的气体,极易溶于水,体积分数大于10%时,易发生爆炸,是一种无毒的绿色消毒剂。实验室可用下图所示装置(夹持仪器已省略)制备 水溶液。下列说法错误的是
水溶液。下列说法错误的是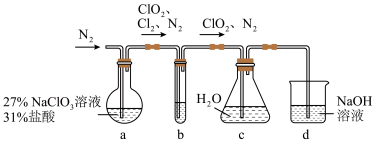
A.装置a的反应产物中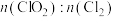 的比值一定为2:1 的比值一定为2:1 |
| B.装置b的主要作用是除去混合气体中的HCl |
C.通入氮气的目的为稀释装置a中产生的 并使其中产生的气体全部进入后续装置 并使其中产生的气体全部进入后续装置 |
D.装置d可除去多余的 |
您最近一年使用:0次
名校
解题方法
3 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
(1)汽车尾气主要含有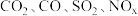 等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的
等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的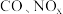 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为_______ 。
(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。_______ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为发生装置→_______ 。(按从左到右的气流方向,用小写字母 和箭头表示)_______ (填字母)。
A. B.
B. C.
C. D.
D.
③丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与 按物质的量
按物质的量 恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式_______ 。
(3)海洋生物参与氮循环的过程如图所示(其它含氨物质不参与反应)。_______ 种价态。反应③和⑤中,若生成等物质的量的 ,则转移的电子数之比为
,则转移的电子数之比为_____ 。
(1)汽车尾气主要含有
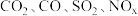 等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的
等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的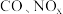 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

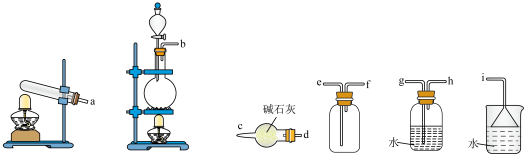
A.
 B.
B. C.
C. D.
D.
③丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与
 按物质的量
按物质的量 恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式(3)海洋生物参与氮循环的过程如图所示(其它含氨物质不参与反应)。
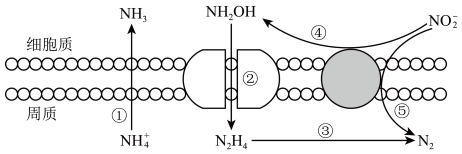
 ,则转移的电子数之比为
,则转移的电子数之比为
您最近一年使用:0次
名校
解题方法
4 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一)碘含量的测定
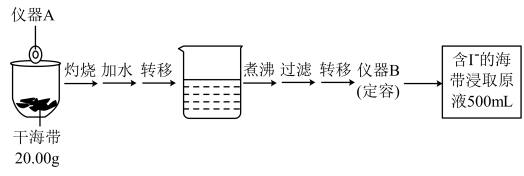
取100.00mL海带浸取原液于锥形瓶中,用 的
的 标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
(1)仪器A的名称为_____ ;仪器B的名称为:_____ 。
(2)计算海带中碘的百分含量为_____ %。
实验(二)碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知: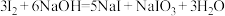 ;酸性条件下,
;酸性条件下, 在水溶液中的溶解度很小。
在水溶液中的溶解度很小。
(3)“适量 ”中能代替
”中能代替 的最佳物质的电子式为
的最佳物质的电子式为_____ 。
(4)下列有关步骤Y的说法,正确的是_____。
(5)方案乙中,上层液体加入 溶液,反应的离子方程式为:
溶液,反应的离子方程式为:_____ ,其中操作Z的名称是_____ 。
实验(一)碘含量的测定

取100.00mL海带浸取原液于锥形瓶中,用
 的
的 标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。
标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00mL。(1)仪器A的名称为
(2)计算海带中碘的百分含量为
实验(二)碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:
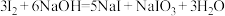 ;酸性条件下,
;酸性条件下, 在水溶液中的溶解度很小。
在水溶液中的溶解度很小。(3)“适量
 ”中能代替
”中能代替 的最佳物质的电子式为
的最佳物质的电子式为(4)下列有关步骤Y的说法,正确的是_____。
A.应控制 溶液的浓度和体积 溶液的浓度和体积 |
| B.将碘转化成离子进入水层 |
| C.主要是除浸取原液中的有机杂质 |
D. 溶液可由乙醇代替 溶液可由乙醇代替 |
(5)方案乙中,上层液体加入
 溶液,反应的离子方程式为:
溶液,反应的离子方程式为:
您最近一年使用:0次
名校
5 . 物质类别和元素化合价是研究物质性质的两个重要角度。
Ⅰ.硫在不同价态之间的转化: 溶液
溶液 溶液
溶液
(1)反应①的转化说明
 的类别属于
的类别属于 溶液,从化合价的角度分析,反应②合理的是
溶液,从化合价的角度分析,反应②合理的是a. b.
b. c.
c.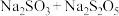
Ⅱ.某兴趣小组模拟工业制取 的装置(夹持和加热装置略)如图所示。
的装置(夹持和加热装置略)如图所示。
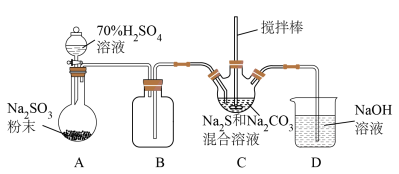
(2)装置A中发生反应的化学方程式为
(3)装置C发生的反应有①
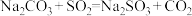 ;②……;③
;②……;③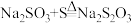 ,反应②的离子方程式为
,反应②的离子方程式为 ,应使三颈烧瓶中
,应使三颈烧瓶中 和
和 恰好完全反应,则三颈烧瓶中
恰好完全反应,则三颈烧瓶中 和
和 物质的量之比应为
物质的量之比应为(4)工业上常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 ,发生反应的离子方程式为
,发生反应的离子方程式为 可用于氰化物解毒,解毒原理为
可用于氰化物解毒,解毒原理为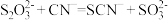 。体外模拟该解毒实验,检验该转化有
。体外模拟该解毒实验,检验该转化有 生成的实验操作是
生成的实验操作是
您最近一年使用:0次
名校
6 . 大连理工大学课题组通过CuO/ 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是
 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是A.标准状况下,1.12L NO中含有电子数为1.5 |
B.将 个 个 溶于100mL水中,所得溶液的质量分数约为29.9% 溶于100mL水中,所得溶液的质量分数约为29.9% |
C.生成22g  能消除NO的数目为0.2 能消除NO的数目为0.2 |
D.若NO和CO混合气体的平均相对分子质量为29,则含有CO的数目为0.5 |
您最近一年使用:0次
2024-03-13更新
|
280次组卷
|
3卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
名校
解题方法
7 . 雌黄 和雄黄
和雄黄 都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是

 和雄黄
和雄黄 都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
| A.反应Ⅰ、Ⅱ、Ⅲ、Ⅳ均为氧化还原反应 |
B.反应Ⅱ中,若物质a为 ,当 ,当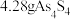 参与反应时转移 参与反应时转移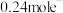 |
| C.反应过程中的尾气用硫酸铜溶液吸收 |
D.反应Ⅰ的离子方程式为 |
您最近一年使用:0次
2024-01-24更新
|
340次组卷
|
3卷引用:山东省名校考试联盟2023-2024学年高三上学期12月份联盟考试化学试题
名校
8 . 工业生产中除去电石渣浆(含 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是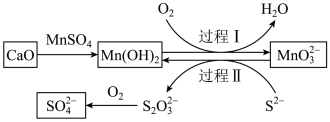
A.碱性条件下,氧化性: |
B.过程Ⅱ中,反应的离子方程式为 |
C.将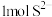 转化为 转化为 理论上需要 理论上需要 的体积为 的体积为 (标准状况) (标准状况) |
| D.该过程中涉及的化学反应均是氧化还原反应 |
您最近一年使用:0次
2024-01-14更新
|
921次组卷
|
3卷引用:山东省淄博第十一中学2023-2024学年高一下学期4月阶段性考试化学试卷
名校
解题方法
9 . 下列离子方程式正确的是
A. 溶液与少量 溶液与少量 溶液反应: 溶液反应: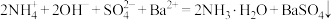 |
B.用热的NaOH溶液溶解S: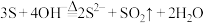 |
C.用 溶液吸收废气中的 溶液吸收废气中的 : :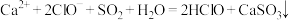 |
D.向 稀溶液中加入盐酸: 稀溶液中加入盐酸: |
您最近一年使用:0次
2024-01-10更新
|
649次组卷
|
2卷引用:山东省淄博第十一中学2023-2024学年高一下学期4月阶段性考试化学试卷
名校
10 . 肼(N2H4)是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实验小组拟用NH3和NaClO溶液反应制备肼,装置如图所示,并探究肼的性质。

回答下列问题:
(1)装置A中的化学方程式为___________ 。装置C中滴入浓盐酸时使用恒压滴液漏斗的优点是___________ 。
(2)装置B中制备肼的化学方程式为___________ 。
(3)图示装置存在的两处缺陷是___________ 。
(4)探究性质:已知N2H4为二元弱碱,在水中的电离与NH3相似。请写出N2H4在水溶液中的第二步电离方程式:___________ ,肼与硫酸反应生成酸式盐的化学式为___________ ,反应后的水溶液中含有多种阳离子,其中阳离子N2H 的电子式为
的电子式为___________ 。
(5)常温下,向N2H4的水溶液中滴加盐酸,溶液的pH与离子浓度的变化关系如图所示,下列说法正确的是___________(填标号)。


回答下列问题:
(1)装置A中的化学方程式为
(2)装置B中制备肼的化学方程式为
(3)图示装置存在的两处缺陷是
(4)探究性质:已知N2H4为二元弱碱,在水中的电离与NH3相似。请写出N2H4在水溶液中的第二步电离方程式:
 的电子式为
的电子式为(5)常温下,向N2H4的水溶液中滴加盐酸,溶液的pH与离子浓度的变化关系如图所示,下列说法正确的是___________(填标号)。

| A.N2H4在水溶液中的第一步电离平衡常数为1.0×10-8 |
| B.N2H5Cl溶液显酸性 |
C.N2H +N2H4 +N2H4 2N2H5+的平衡常数为1.0×109 2N2H5+的平衡常数为1.0×109 |
D.N2H6Cl2溶液中:c(Cl-)=2c(N2H )+2c(N2H )+2c(N2H ) ) |
您最近一年使用:0次
2024-01-02更新
|
402次组卷
|
2卷引用:山东省高中名校2023-2024学年高三上学期12月统一调研考试化学试题



