解题方法
1 . 将氧化铁还原为铁的技术在人类文明的进步中占有十分重要的地位。炼铁高炉中发生的关键反应如下:
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
CO2(g)+C(s)=2CO(g) ΔH=+172.46 kJ/mol
Fe2O3+CO→Fe+CO2
若已知:2Fe(s)+ O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
根据上面三个热化学方程式,回答下列问题:
(1)CO的摩尔燃烧焓为_______ ;写出其热化学方程式:_______ 。
(2)高炉内Fe2O3被CO还原为Fe的热化学方程式为_______ 。
(3)炼制1吨含铁96%的生铁所需焦炭的理论用量是_______ 吨,实际生产中所需焦炭远高于理论用量,其原因是_______ 。
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
CO2(g)+C(s)=2CO(g) ΔH=+172.46 kJ/mol
Fe2O3+CO→Fe+CO2
若已知:2Fe(s)+
 O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol根据上面三个热化学方程式,回答下列问题:
(1)CO的摩尔燃烧焓为
(2)高炉内Fe2O3被CO还原为Fe的热化学方程式为
(3)炼制1吨含铁96%的生铁所需焦炭的理论用量是
您最近半年使用:0次
2 . 配平下列方程式。
① S+ KOH K2S+ K2SO3+ H2O
K2S+ K2SO3+ H2O_____ 。
② KClO3 KCl+ O2↑
KCl+ O2↑_____ 。
③ Cl2+ NaOH NaCl+ NaClO3+ H2O
NaCl+ NaClO3+ H2O_____ 。
④ (NH4)2SO4= NH3↑+ SO2↑+ N2↑+ H2O_____ 。
⑤ Fe+ HNO3(浓) Fe(NO3)3+ NO2↑+ H2O
Fe(NO3)3+ NO2↑+ H2O_____ 。
① S+ KOH
 K2S+ K2SO3+ H2O
K2S+ K2SO3+ H2O② KClO3
 KCl+ O2↑
KCl+ O2↑③ Cl2+ NaOH
 NaCl+ NaClO3+ H2O
NaCl+ NaClO3+ H2O④ (NH4)2SO4= NH3↑+ SO2↑+ N2↑+ H2O
⑤ Fe+ HNO3(浓)
 Fe(NO3)3+ NO2↑+ H2O
Fe(NO3)3+ NO2↑+ H2O
您最近半年使用:0次
3 . 配平下列离子方程式。
① Fe3++ SO2+ H2O= Fe2++ SO + H+
+ H+_____ 。
② C2O + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O_____ 。
① Fe3++ SO2+ H2O= Fe2++ SO
 + H+
+ H+② C2O
 + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O
您最近半年使用:0次
解题方法
4 . 配平下列氧化还原反应的方程式。
① HCl(浓)+ MnO2 Cl2↑+ MnCl2+ H2O
Cl2↑+ MnCl2+ H2O_____ 。
② KMnO4+ FeSO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O_____ 。
③ Na2SO3+ KIO3+ H2SO4= Na2SO4+ K2SO4+ I2+ H2O_____ 。
④ Au2O3+ Na2S2O3+ NaOH= Au2O+ Na2SO4+ H2O_____ 。
⑤ FeS+ O2= Fe2O3+ SO2_____ 。
⑥ KI+ KIO3+ H2SO4= I2+ K2SO4+ H2O_____ 。
① HCl(浓)+ MnO2
 Cl2↑+ MnCl2+ H2O
Cl2↑+ MnCl2+ H2O② KMnO4+ FeSO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
③ Na2SO3+ KIO3+ H2SO4= Na2SO4+ K2SO4+ I2+ H2O
④ Au2O3+ Na2S2O3+ NaOH= Au2O+ Na2SO4+ H2O
⑤ FeS+ O2= Fe2O3+ SO2
⑥ KI+ KIO3+ H2SO4= I2+ K2SO4+ H2O
您最近半年使用:0次
解题方法
5 . 检验加“碘”盐含“KIO3”可通过在酸性条件下,加入碘化钾溶液和淀粉来实现。反应原理如下:KIO3+KI+HCl―→I2+KCl+H2O(未配平)。下列有关说法正确的是
| A.KI是还原剂 |
| B.KIO3被氧化 |
| C.该反应配平后化学计量数依次为:1、5、6、3、6、3 |
| D.每生成3个I2分子,转移6个电子 |
您最近半年使用:0次
6 . 在离子方程式xR2++yH++O2=mR3++nH2O中,对系数m和R3+的判断正确的是
| A.m=4;R2+是氧化剂 |
| B.m=y;R3+是氧化产物 |
| C.m=2;R2+是氧化剂 |
| D.m=y;R3+是还原产物 |
您最近半年使用:0次
2023-08-25更新
|
310次组卷
|
2卷引用:微专题(五) 氧化还原反应方程式的配平及计算
7 . 等个数的下列化合物与足量浓盐酸反应,得到氯气的量最多的是
已知:
 +H++Cl-―→Mn2++Cl2↑+H2O(未配平)
+H++Cl-―→Mn2++Cl2↑+H2O(未配平)
 +H++Cl-―→Cl2↑+H2O(未配平)
+H++Cl-―→Cl2↑+H2O(未配平)
ClO-+H++Cl-―→Cl2↑+H2O(未配平)
MnO2+H++Cl-―→Cl2↑+H2O(未配平)
已知:
 +H++Cl-―→Mn2++Cl2↑+H2O(未配平)
+H++Cl-―→Mn2++Cl2↑+H2O(未配平) +H++Cl-―→Cl2↑+H2O(未配平)
+H++Cl-―→Cl2↑+H2O(未配平)ClO-+H++Cl-―→Cl2↑+H2O(未配平)
MnO2+H++Cl-―→Cl2↑+H2O(未配平)
| A.KClO3 | B.KMnO4 |
| C.MnO2 | D.Ca(ClO)2 |
您最近半年使用:0次
8 . CaO2和Na2O2在结构和性质上有很多相似的地方。请回答下列问题:
(1)CaO2属于___________ (填“离子化合物”或“共价化合物”),其电子式为___________ ,其阴、阳离子个数比为___________ 。
(2)CaO2与水反应的化学方程式为___________ ,生成1 mol单质气体,转移的电子数为___________ 。
(3)CaO2与二氧化碳反应的化学方程式为___________ ,该反应属于___________ (填字母)。
A.置换反应 B.氧化还原反应 C.复分解反应
(1)CaO2属于
(2)CaO2与水反应的化学方程式为
(3)CaO2与二氧化碳反应的化学方程式为
A.置换反应 B.氧化还原反应 C.复分解反应
您最近半年使用:0次
9 . 高铁酸钾(K2FeO4)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,可用于饮用水处理。实验室中可通过如图方法制备K2FeO4。
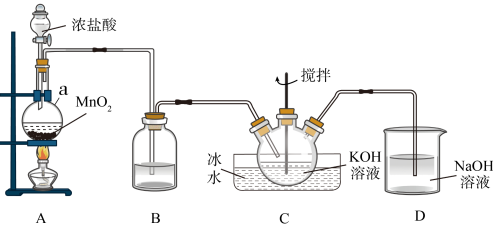
回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为________ ;装置B中试剂的名称是________ ;装置B的作用是___ 。
(2)装置C中Cl2与KOH反应的离子方程式为____________ 。
(3)若无装置D,可能产生的危害是_______ 。
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为______ 。

回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为
(2)装置C中Cl2与KOH反应的离子方程式为
(3)若无装置D,可能产生的危害是
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为
您最近半年使用:0次
10 . 下列实验装置可用于实验室制备少量无水FeCl3,已知FeCl3遇水会强烈反应。

(1)为达到实验目的,各装置的正确连接顺序是:a→________→________→________→________→h→i→c→b→g→f(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。_____ 。
(2)请写出装置⑤圆底烧瓶中制备氯气的离子方程式_______________________ 。
(3)装置②的目的除了降低Cl2在溶液中的溶解度外,还有_______________________ 。
(4)请写出④制备FeCl3的化学方程式______________ 。
(5)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃________ (填装置序号)处酒精灯,后点燃________ (填装置序号)处酒精灯。

(1)为达到实验目的,各装置的正确连接顺序是:a→________→________→________→________→h→i→c→b→g→f(填接口的字母,箭头的方向即气流的方向,部分装置可重复使用)。
(2)请写出装置⑤圆底烧瓶中制备氯气的离子方程式
(3)装置②的目的除了降低Cl2在溶液中的溶解度外,还有
(4)请写出④制备FeCl3的化学方程式
(5)本实验装置④⑤两处均有酒精灯,实验开始前应先点燃
您最近半年使用:0次



