1 . 在三支试管中分别加入 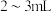
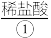 ,
, 溶液、
溶液、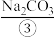 溶液,然后各滴入几滴
溶液,然后各滴入几滴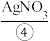 溶液,观察现象;再分别滴入少量
溶液,观察现象;再分别滴入少量 ,观察现象。回答下列问题:
,观察现象。回答下列问题:
(1)AgNO3 在水中电离的电离方程式为_______ 。
(2)①中分散质粒子直径为_______ (填“<1 nm”或“>100 nm”)。
(3)常温下,饱和②溶液_______ (填“能”或“不能”)发生丁达尔效应。
(4)从物质的组成来看,④属于_______ (填“酸”、“碱”、“盐”或“氧化物”),将其加入稀盐酸中,发生反应的化学方程式为_______ 。
(5)查阅资料可知,硝酸具有强氧化性,其浓度越小,氧化能力越弱。对于反应
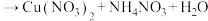 (未配平),该反应的化学方程式为
(未配平),该反应的化学方程式为_______ ,该反应中,每生成0.8gNH4NO3,转移的电子数为_______ NA。
 ,
, 溶液、
溶液、 溶液,然后各滴入几滴
溶液,然后各滴入几滴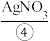 溶液,观察现象;再分别滴入少量
溶液,观察现象;再分别滴入少量 ,观察现象。回答下列问题:
,观察现象。回答下列问题:(1)AgNO3 在水中电离的电离方程式为
(2)①中分散质粒子直径为
(3)常温下,饱和②溶液
(4)从物质的组成来看,④属于
(5)查阅资料可知,硝酸具有强氧化性,其浓度越小,氧化能力越弱。对于反应

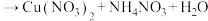 (未配平),该反应的化学方程式为
(未配平),该反应的化学方程式为
您最近一年使用:0次
2023-11-03更新
|
77次组卷
|
2卷引用:辽宁省辽阳市2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
2 . 青铜是人类历史上一项伟大的发明,它是红铜和锡、铅的合金,也是金属冶铸史上最早的合金。铜及其合金在日常生活中应用广泛。回答下列问题:
(1)西汉刘安在《淮南万毕术》中介绍了我国在西汉时期发明的湿法冶金技术,即“曾青得铁则化为铜”,其含义是铜的可溶性化合物的水溶液与铁反应生成铜。例如:将适量的铁粉加入硫酸铜溶液中,发生反应CuSO4+Fe=Cu+FeSO4。
①该反应发生时,溶液的颜色变化为_______ 。
②用双线桥法标出该反应中电子转移的方向和数目:_______ 。
③每生成6.4 g Cu,消耗的CuSO4的质量为_______ g。
(2)工业冶炼铜的原理主要是:
i.2Cu2S+3O2 2Cu2O+2SO2
2Cu2O+2SO2
ii.2Cu2O+Cu2S 6Cu+SO2↑
6Cu+SO2↑
①Cu2S中Cu元素的化合价为_______ 价。
②反应i中,生成的SO2属于_______ (填“氧化”、“还原”或“氧化和还原”)产物,将其通入足量的NaOH溶液中,发生反应的化学方程式为2NaOH+SO2=Na2SO3+H2O,该反应的离子方程式为_______ 。
③将Cu2O固体加入稀HNO3中,发生反应_______Cu2O+_______ HNO3=_______Cu(NO3)2+_______ NO↑+_______H2O,配平该化学方程式_________ 。
(1)西汉刘安在《淮南万毕术》中介绍了我国在西汉时期发明的湿法冶金技术,即“曾青得铁则化为铜”,其含义是铜的可溶性化合物的水溶液与铁反应生成铜。例如:将适量的铁粉加入硫酸铜溶液中,发生反应CuSO4+Fe=Cu+FeSO4。
①该反应发生时,溶液的颜色变化为
②用双线桥法标出该反应中电子转移的方向和数目:
③每生成6.4 g Cu,消耗的CuSO4的质量为
(2)工业冶炼铜的原理主要是:
i.2Cu2S+3O2
 2Cu2O+2SO2
2Cu2O+2SO2ii.2Cu2O+Cu2S
 6Cu+SO2↑
6Cu+SO2↑①Cu2S中Cu元素的化合价为
②反应i中,生成的SO2属于
③将Cu2O固体加入稀HNO3中,发生反应_______Cu2O+_______ HNO3=_______Cu(NO3)2+_______ NO↑+_______H2O,配平该化学方程式
您最近一年使用:0次
2022-10-10更新
|
302次组卷
|
5卷引用:辽宁省辽阳市2022-2023学年高一上学期期中考试化学试题
3 . 氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中均有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦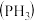 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:___________ 。
(2)羟基磷灰石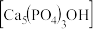 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
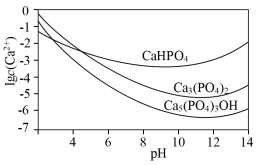
①图中所示3种钙盐,其中在人体中最稳定的存在形式是___________ (填化学式)。
②实验室制备羟基磷灰石时,应将___________ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到___________ 中。
(3)氮的氧化物对大气污染比较严重,一定条件下可用 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ ,该反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为___________ ,每消耗1mol ,同时转移
,同时转移___________ mol电子。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦
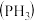 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:(2)羟基磷灰石
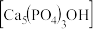 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
(3)氮的氧化物对大气污染比较严重,一定条件下可用
 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式: ,同时转移
,同时转移
您最近一年使用:0次
4 . 过氧化氢的水溶液俗称双氧水,它的用途很广泛,常用于消毒、杀菌、漂白等。回答下列问题:
(1)过氧化氢的性质
①酸性条件下H2O2可将Fe2+转化成Fe3+,说明H2O2具有__ 性。
②常温下,H2O2显弱酸性(Ka1=2.40×10-12、Ka2=1.05×10-25),不能使甲基橙指示剂褪色,则向4.0mol•L-1的H2O2溶液中滴加甲基橙,溶液显__ 色。(甲基橙在pH小于3.1时显红色,3.1~4.4时显橙色,大于4.4时显黄色)
(2)过氧化氢含量的测定实验
某兴趣小组同学用0.1mol•L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2MnO +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①滴定达到终点的现象是__ 。
②用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如下表:
试样中过氧化氢的浓度为__ mol•L-1。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上。实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛(HCHO)溶液依次加入质量分数为30%~70%的过氧化氢溶液中。该反应的化学方程式为__ 。
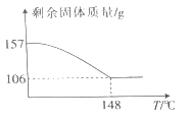
(4)过氧化氢与碳酸钠的加合物Na2CO3•xH2O2比较稳定,方便储存,可用于消毒、漂白。现称取157gNa2CO3•xH2O2晶体加热,实验结果如图所示,则该晶体的组成为__ (x精确到0.1)
(1)过氧化氢的性质
①酸性条件下H2O2可将Fe2+转化成Fe3+,说明H2O2具有
②常温下,H2O2显弱酸性(Ka1=2.40×10-12、Ka2=1.05×10-25),不能使甲基橙指示剂褪色,则向4.0mol•L-1的H2O2溶液中滴加甲基橙,溶液显
(2)过氧化氢含量的测定实验
某兴趣小组同学用0.1mol•L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2MnO
 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。①滴定达到终点的现象是
②用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如下表:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| V(酸性KMnO4标准溶液)/mL | 17.10 | 18.10 | 18.00 | 17.90 |
试样中过氧化氢的浓度为
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上。实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛(HCHO)溶液依次加入质量分数为30%~70%的过氧化氢溶液中。该反应的化学方程式为
(4)过氧化氢与碳酸钠的加合物Na2CO3•xH2O2比较稳定,方便储存,可用于消毒、漂白。现称取157gNa2CO3•xH2O2晶体加热,实验结果如图所示,则该晶体的组成为

您最近一年使用:0次
5 . 已知铅(Pb)与硅同主族且Pb比Si多3个电子层。
(1)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb[(CH3COO)2Pb易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是______ (填“强”或“弱”)电解质。
(2)将PbO2加入硝酸酸化的Mn(NO3)2溶液中搅拌后溶液显紫红色;则每反应1 mol Mn(NO3)2转移____________ mol电子。
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成两种无污染的气体,该反应的化学方程式为:___________________________________ 。
(4)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液呈碱性,发生反应的离子方程式是______________ 。
②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠溶液,发现蓝色逐渐消失,写出发生反应的离子方程式是______________ 。
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为______________ ,其中氨水转化Cr3+为Cr(OH)3的离子方程式为____________________________________________ ;该方案处理后的废水中因含有大量________ 元素,直接排放会导致水体富营养化。
(1)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb[(CH3COO)2Pb易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是
(2)将PbO2加入硝酸酸化的Mn(NO3)2溶液中搅拌后溶液显紫红色;则每反应1 mol Mn(NO3)2转移
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成两种无污染的气体,该反应的化学方程式为:
(4)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液呈碱性,发生反应的离子方程式是
②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠溶液,发现蓝色逐渐消失,写出发生反应的离子方程式是
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为
您最近一年使用:0次



