1 . 浓硝酸可以氧化非金属单质,如加热条件下可将C氧化为CO2,同时生成红棕色气体,反应的化学方程式为________________________ ,体现浓硝酸的________ 性。
您最近一年使用:0次
2 . 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:
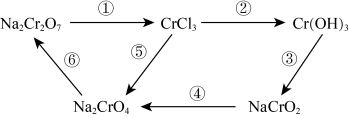
(1)Na2Cr2O7中Cr元素的化合价是______ ,该物质属于_____ (填序号)。
①酸 ②碱 ③盐 ④氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是______ (填序号)。
(3)反应①为: (未配平)。其中还原产物为
(未配平)。其中还原产物为______ ,Na2Cr2O7与Cl2的化学计量数比为_____ 。
(4)完成反应④的配平,并用单线桥标出电子转移的方向和数目。(系数若为1也请写出)_____
反应④为:

(1)Na2Cr2O7中Cr元素的化合价是
①酸 ②碱 ③盐 ④氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是
(3)反应①为:
 (未配平)。其中还原产物为
(未配平)。其中还原产物为(4)完成反应④的配平,并用单线桥标出电子转移的方向和数目。(系数若为1也请写出)
反应④为:

您最近一年使用:0次
3 . 金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为___________ ,采用空气和Na为原料可直接制备Na2O2.空气与熔融的金属Na反应前需依次通过的试剂为___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)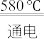 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是___________ 。
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
①配平上述离子方程式___________ 。
②该反应说明Na2O2具有___________ (选填“氧化性”“还原性"或“漂白性”)。
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为___________ 。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
A.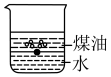 | B.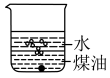 |
C. | D. |
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)
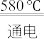 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O①配平上述离子方程式
②该反应说明Na2O2具有
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为
您最近一年使用:0次
名校
4 . 按要求完成下列问题:
(1)Na久置空气中最终都是变为________ (填化学式);漂白粉有效成分的化学式________ 。
(2)纯净的H2在Cl2中安静地燃烧,发出________ 色火焰。胆矾的化学式为________ 。
(3)写出金属钠投入水中发生反应的离子方程式是________ 。
(4)在一定量的稀盐酸中,加入少量高铜酸钠(NaCuO2)固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是________ 。
(1)Na久置空气中最终都是变为
(2)纯净的H2在Cl2中安静地燃烧,发出
(3)写出金属钠投入水中发生反应的离子方程式是
(4)在一定量的稀盐酸中,加入少量高铜酸钠(NaCuO2)固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是
您最近一年使用:0次
解题方法
5 . 利用绿矾(FeSO4·7H2O)对某工厂废水(含有强氧化性离子Cr2O )进行处理。
)进行处理。
(1)工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取FeSO4。已知该反应除生成硫酸亚铁外,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:_______________________ 。
(2)请配平下列离子方程式:______ 。
Fe2++ Cr2O +
+  = Fe3++ Cr3++ H2O
= Fe3++ Cr3++ H2O
 )进行处理。
)进行处理。(1)工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取FeSO4。已知该反应除生成硫酸亚铁外,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
(2)请配平下列离子方程式:
Fe2++ Cr2O
 +
+  = Fe3++ Cr3++ H2O
= Fe3++ Cr3++ H2O
您最近一年使用:0次
6 . 配平下列离子方程式。
① Fe3++ SO2+ H2O= Fe2++ SO + H+
+ H+_____ 。
② C2O + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O_____ 。
① Fe3++ SO2+ H2O= Fe2++ SO
 + H+
+ H+② C2O
 + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O
您最近一年使用:0次
7 . 化学与人类生产、生活密切相关,按要求回答下列问题。
(1)工业上制造光导纤维的基本原料是_______ (填化学式)。
(2)钠的化合物中,可用作潜水艇中供氧剂的是_______ ,其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是_______ (填化学式)。
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目_______ 。若反应中共转移 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为_______ L(标准状况下)。
(1)工业上制造光导纤维的基本原料是
(2)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
A. | B. | C. | D. |
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为
您最近一年使用:0次
2023-07-31更新
|
360次组卷
|
4卷引用:陕西省汉中市2020-2021学年高一上学期期末考试化学试题
陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)结构与性质(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)
8 . 根据要求,写出化学方程式或者离子方程式。
(1)氯气和石灰乳反应制取漂白粉的化学方程式___________ ;
(2)过氧化钠和水反应的化学方程式___________ ;
(3)写出 和足量
和足量 反应的离子方程式
反应的离子方程式___________ ;
(4)碘盐中的 和
和 在酸性溶液中发生反应的离子方程式
在酸性溶液中发生反应的离子方程式___________ ;
(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式___________ ;
(6)红热的炭块放入浓硫酸中发生反应的化学方程式___________ 。
(1)氯气和石灰乳反应制取漂白粉的化学方程式
(2)过氧化钠和水反应的化学方程式
(3)写出
 和足量
和足量 反应的离子方程式
反应的离子方程式(4)碘盐中的
 和
和 在酸性溶液中发生反应的离子方程式
在酸性溶液中发生反应的离子方程式(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式
(6)红热的炭块放入浓硫酸中发生反应的化学方程式
您最近一年使用:0次
解题方法
9 . 消毒剂在生活中应用广泛, 、
、 、
、 、
、 、
、 是生活中不同领域的消毒剂。根据下列反应回答问题:
是生活中不同领域的消毒剂。根据下列反应回答问题:
①
②
③ (未配平)
(未配平)
④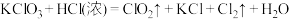 (未配平)
(未配平)
(1)储存过氧化氢的试剂瓶上最适合贴上的标签是_____(填字母)。
(2)反应①中,氧化剂与还原剂的物质的量之比为_____ 。
(3)反应②中,当有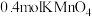 参加反应时,做酸性介质的
参加反应时,做酸性介质的 的物质的量为
的物质的量为_____  。
。
(4)配平并用双线桥法表示反应③中电子转移的方向和数目_____ 。
(5)若反应④中有 (标准状况下)氯气生成,则转移的电子数为
(标准状况下)氯气生成,则转移的电子数为_____
(6)某强酸反应体系中会发生氧化还原反应,反应物和生成物共六种微粒: 、
、 、
、 、
、 、
、 、
、 ,已知该反应中
,已知该反应中 只发生过程
只发生过程 。
。
i.该反应体系选择的酸是_____ (填字母)。
A盐酸 B.稀硫酸 C.醋酸
ii.该反应的离子方程式为_____ 。
 、
、 、
、 、
、 、
、 是生活中不同领域的消毒剂。根据下列反应回答问题:
是生活中不同领域的消毒剂。根据下列反应回答问题:①

②

③
 (未配平)
(未配平)④
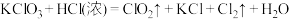 (未配平)
(未配平)(1)储存过氧化氢的试剂瓶上最适合贴上的标签是_____(填字母)。
A. | B. |
C. | D. |
(3)反应②中,当有
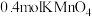 参加反应时,做酸性介质的
参加反应时,做酸性介质的 的物质的量为
的物质的量为 。
。(4)配平并用双线桥法表示反应③中电子转移的方向和数目
(5)若反应④中有
 (标准状况下)氯气生成,则转移的电子数为
(标准状况下)氯气生成,则转移的电子数为(6)某强酸反应体系中会发生氧化还原反应,反应物和生成物共六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,已知该反应中
,已知该反应中 只发生过程
只发生过程 。
。i.该反应体系选择的酸是
A盐酸 B.稀硫酸 C.醋酸
ii.该反应的离子方程式为
您最近一年使用:0次
名校
10 . 下列是中学阶段常见的重要化学物质:
a.氢氧化铁胶体 b.氢氧化钠 c.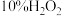 溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
请完成下列各题:
(1)属于氧化物的有___________ (填序号,下同),能净水的有___________ ,属于盐的有___________ 。
(2)g的有效成分是___________ (填化学式)。
(3)向f中滴加几滴c,观察到的现象是___________ ,发生反应的离子方程式为___________ 。
(4)向d溶液中加入过量b溶液,发生反应的离子方程式为___________ 。
a.氢氧化铁胶体 b.氢氧化钠 c.
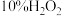 溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠
溶液 d.明矾 e.氧化铝 f.稀硫酸酸化的硫酸亚铁溶液 g.84消毒液 h.稀盐酸 i.二氧化硅 j.偏铝酸钠请完成下列各题:
(1)属于氧化物的有
(2)g的有效成分是
(3)向f中滴加几滴c,观察到的现象是
(4)向d溶液中加入过量b溶液,发生反应的离子方程式为
您最近一年使用:0次



