名校
解题方法
1 . 不能 正确表示下列反应的离子方程式是
| A.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
B.0.1 mol/L NH4Al(SO4)2溶液与0.2 mol/L Ba(OH)2溶液等体积混合:Al3++2SO +2Ba2++4OH-=2BaSO4↓+[(AlOH)4]- +2Ba2++4OH-=2BaSO4↓+[(AlOH)4]- |
C.用稀硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO +6H++5H2O2=2Mn2++5O2↑+8H2O +6H++5H2O2=2Mn2++5O2↑+8H2O |
| D.向FeBr2溶液(含溶质amol)中通入amol氯气:2Fe2++ 2Br-+2Cl2 =2Fe3++ Br2+ 4Cl- |
您最近一年使用:0次
2021-09-17更新
|
964次组卷
|
4卷引用:河南省南阳市第一中学校2021-2022学年高三上学期第三次月考化学试题
10-11高三上·河南·阶段练习
2 . 下列实验设计及其对应的离子方程式均正确的是
| A.石灰石与硫酸反应制CO2:CaCO3+2H+=Ca2++CO2↑+ H2O |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2+ H2O=2H++Cl-+ClO- |
| D.用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
您最近一年使用:0次
名校
解题方法
3 . 海水提碘实验中,得到碘的四氯化碳溶液后可用“反萃取法”萃取、富集碘单质,实验步骤如下(已知:3I2+6NaOH=5NaI+NaIO3+3H2O)。下列说法错误的是
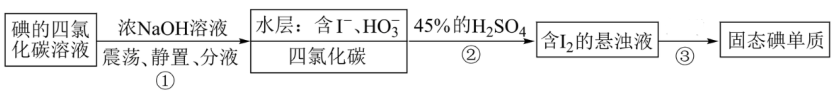
| A.步骤①还可以用酒精做萃取剂 |
| B.分液时水层从分液漏斗上口放出 |
C.步骤②中发生反应的离子方程式为6H++5I-+ =3I2↓+3H2O =3I2↓+3H2O |
| D.步骤③操作中需要的玻璃仪器为漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-04-23更新
|
146次组卷
|
2卷引用:河南省安阳市林州市第一中学2023-2024学年高一下学期4月月考化学试题
名校
4 . 黄铁矿在潮湿的环境中会被缓慢氧化,其中发生的反应之一为 (未配平),下列说法错误的是
(未配平),下列说法错误的是
A. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
B.根据该反应判断 的氧化性大于 的氧化性大于 |
C.氧化剂与还原剂的物质的量之比为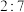 |
| D.随反应进行,体系的酸性逐渐增强 |
您最近一年使用:0次
5 . 硫化氢的转化是资源利用和环境保护的重要研究课题.将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收
的混合溶液中回收 ,其转化如图所示(
,其转化如图所示( 不溶于水).下列说法中,不正确的是
不溶于水).下列说法中,不正确的是

 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收
的混合溶液中回收 ,其转化如图所示(
,其转化如图所示( 不溶于水).下列说法中,不正确的是
不溶于水).下列说法中,不正确的是
A.过程①中,生成 的反应为 的反应为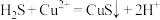 |
B.过程②中, 作氧化剂 作氧化剂 |
C.每生成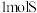 ,整个过程转移电子数为 ,整个过程转移电子数为 |
D.回收 的总反应为 的总反应为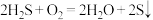 |
您最近一年使用:0次
名校
解题方法
6 . 利用硫铁矿烧渣(主要成分为 和
和 等)制备
等)制备 的工艺流程如图所示:
的工艺流程如图所示:
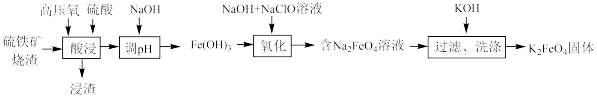
下列说法错误的是
A.“酸浸”时,充入高压氧的目的是增大溶解氧的量,使 充分被氧化 充分被氧化 |
B.浸渣的主要成分为硅酸,若酸浸时不进行过滤,其将会导致 产品纯度降低 产品纯度降低 |
C.“氧化”时,发生反应的离子方程式为 |
D.根据流程可知 的溶解度小于 的溶解度小于 ,洗涤 ,洗涤 固体时可选择 固体时可选择 溶液 溶液 |
您最近一年使用:0次
2024-02-26更新
|
357次组卷
|
3卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题
7 . 微生物法炼铜是在反应釜中加入黄铜矿( ,其中Cu为+2价)、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,各物质的转化关系如图所示,下列说法错误的是
,其中Cu为+2价)、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,各物质的转化关系如图所示,下列说法错误的是
 ,其中Cu为+2价)、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,各物质的转化关系如图所示,下列说法错误的是
,其中Cu为+2价)、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,各物质的转化关系如图所示,下列说法错误的是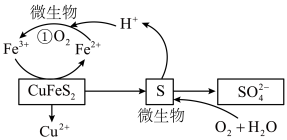
| A.反应釜中保持高温不利于反应进行 |
B.整个转化过程中,可以循环利用的物质有 和 和 |
C.反应①的离子方程式为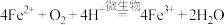 |
D.当黄铜矿中的铁元素全部转化为 时,生成 时,生成 共消耗 共消耗 |
您最近一年使用:0次
2024-02-14更新
|
505次组卷
|
3卷引用:河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题
名校
解题方法
8 . 从干海带中提取碘的实验流程如下:
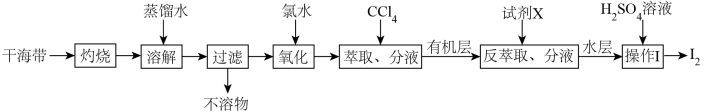
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: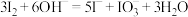 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-01-28更新
|
573次组卷
|
6卷引用:河南省郑州市中牟县第一高级中学2023-2024学年高一下学期3月月考化学试题
9 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如图1所示:
的一种制备方法如图1所示: 可将
可将 氧化成
氧化成 。下列说法错误的是
。下列说法错误的是
 的一种制备方法如图1所示:
的一种制备方法如图1所示: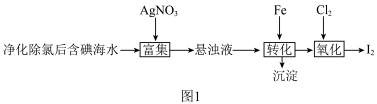
 可将
可将 氧化成
氧化成 。下列说法错误的是
。下列说法错误的是A.“转化”反应的离子方程式为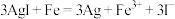 |
B.“转化”产生的沉淀可用 处理后循环使用 处理后循环使用 |
C.“氧化”时,应控制 的量,过多或过少,都会降低单质碘的收率 的量,过多或过少,都会降低单质碘的收率 |
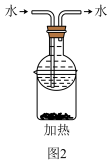
| D.获得的粗碘可采用图2装置进行纯化 |
您最近一年使用:0次
2024-01-10更新
|
95次组卷
|
2卷引用:河南省周口市项城市2023-2024学年上学期高三1月阶段测试理综试题
名校
10 . 去除废水中含氮离子是目前水质改善的热点研究课题,常见的化学方法是用 将含氮离子还原为氮气或先用臭氧、双氧水、次氯酸钠等氧化
将含氮离子还原为氮气或先用臭氧、双氧水、次氯酸钠等氧化 ,再用还原剂除去。去除废水中含有的
,再用还原剂除去。去除废水中含有的 、
、 的一种原理如下:
的一种原理如下: (Ⅰ),
(Ⅰ), (Ⅱ)。下列说法不正确的是
(Ⅱ)。下列说法不正确的是
 将含氮离子还原为氮气或先用臭氧、双氧水、次氯酸钠等氧化
将含氮离子还原为氮气或先用臭氧、双氧水、次氯酸钠等氧化 ,再用还原剂除去。去除废水中含有的
,再用还原剂除去。去除废水中含有的 、
、 的一种原理如下:
的一种原理如下: (Ⅰ),
(Ⅰ), (Ⅱ)。下列说法不正确的是
(Ⅱ)。下列说法不正确的是A.氧化性由强至弱的顺序为 |
B.用镁将水中的 还原成 还原成 的离子方程式为 的离子方程式为 |
C.根据上述资料可知 与 与 不共存,反应为 不共存,反应为 |
D.等物质的量 分别与臭氧、双氧水、次氯酸钠完全反应转移电子数之比为3∶1∶1 分别与臭氧、双氧水、次氯酸钠完全反应转移电子数之比为3∶1∶1 |
您最近一年使用:0次
2023-12-06更新
|
343次组卷
|
2卷引用:河南省洛阳市宜阳县第一高级中学2023-2024学年高一上学期(研学班)期末考试化学试卷



