名校
解题方法
1 . 不能 正确表示下列反应的离子方程式是
| A.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
B.0.1 mol/L NH4Al(SO4)2溶液与0.2 mol/L Ba(OH)2溶液等体积混合:Al3++2SO +2Ba2++4OH-=2BaSO4↓+[(AlOH)4]- +2Ba2++4OH-=2BaSO4↓+[(AlOH)4]- |
C.用稀硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO +6H++5H2O2=2Mn2++5O2↑+8H2O +6H++5H2O2=2Mn2++5O2↑+8H2O |
| D.向FeBr2溶液(含溶质amol)中通入amol氯气:2Fe2++ 2Br-+2Cl2 =2Fe3++ Br2+ 4Cl- |
您最近一年使用:0次
2021-09-17更新
|
963次组卷
|
4卷引用:山东省新泰市新泰中学2022届高三第一次阶段性考试化学试题
名校
2 . 某铜冶炼厂烟气净化工序含砷废水中主要含有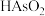 和硫酸及少量
和硫酸及少量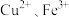 等,以其为原料制备
等,以其为原料制备 的工艺流程如图:
的工艺流程如图: 范围:
范围:
下列说法错误的是
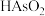 和硫酸及少量
和硫酸及少量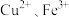 等,以其为原料制备
等,以其为原料制备 的工艺流程如图:
的工艺流程如图: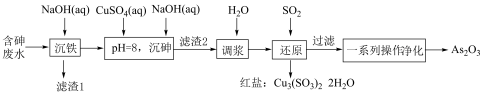
 范围:
范围:金属离子 |
|
|
开始沉淀的 | 1.5 | 4.7 |
沉淀完全的 | 3.7 | 6.6 |
A.“沉铁”调 的范围是 的范围是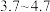 |
B.“滤渣2”成分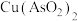 和 和 |
C.“还原”过程中生成红盐的化学方程式: |
| D.“一系列操作”仅涉及物理变化 |
您最近一年使用:0次
2024-05-21更新
|
79次组卷
|
2卷引用:2024届山东省高三下学期联合模拟考试模拟预测化学试题
名校
3 . 利用锌灰(主要成分为ZnO,含有CuO、PbO、SiO2、FeO、Fe2O3等杂质)制备高纯ZnO的工艺流程如图:(已知PbSO4为难溶物)
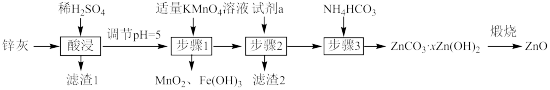
| A.滤渣1的成分只有H2SiO3和PbSO4 |
| B.加入的试剂a可为Zn,目的是除去Cu2+ |
C.步骤1中发生反应的离子方程式为MnO +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ |
| D.若取步骤3后的干燥滤饼11.2g煅烧,得到产品8.1g,则x=2 |
您最近一年使用:0次
名校
4 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中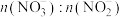 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中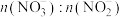 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是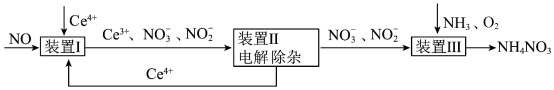
| A.装置江中若有5.6L(标准状况)NO参与反应,则转移1mol电子 |
B.装置Ⅰ中反应为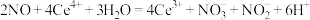 |
| C.装置Ⅲ中氧化剂和还原剂的物质的量之比为1∶2 |
D.装置Ⅲ中 和 和 的体积比3∶1时,可实现原子利用率最大化 的体积比3∶1时,可实现原子利用率最大化 |
您最近一年使用:0次
2024-04-10更新
|
98次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
5 . 用过量的盐酸和 溶液的混合液作为浸取剂,浸取黄铜矿(
溶液的混合液作为浸取剂,浸取黄铜矿( )的流程示意图如下。
)的流程示意图如下。
 溶液的混合液作为浸取剂,浸取黄铜矿(
溶液的混合液作为浸取剂,浸取黄铜矿( )的流程示意图如下。
)的流程示意图如下。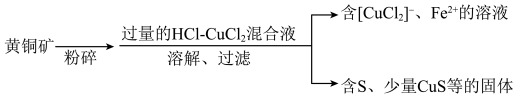
A.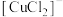 的中心离子是 的中心离子是 ,配体是 ,配体是 |
B.参与反应的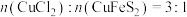 |
C.浸取剂中的 有助于 有助于 固体的溶解 固体的溶解 |
D.用浓盐酸和 溶液的混合液也可能使黄铜矿溶解 溶液的混合液也可能使黄铜矿溶解 |
您最近一年使用:0次
解题方法
6 . 利用镍铂靶材废料(主要成分为Ni、Pt以及微量Fe、Al的单质)回收铂的一种工艺流程如下。

已知:①隔绝空气“煅烧”时有两种单质生成,其中一种是
②室温: 、
、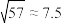
下列说法错误的是

已知:①隔绝空气“煅烧”时有两种单质生成,其中一种是

②室温:
 、
、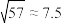
下列说法错误的是
A.“溶解”时发生反应的离子方程式为 |
B.“沉铂”中,若向 的溶液里加入等体积的 的溶液里加入等体积的 溶液,使 溶液,使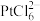 沉淀完全,则 沉淀完全,则 溶液的最小浓度为 溶液的最小浓度为 (忽略溶液混合后体积的变化) (忽略溶液混合后体积的变化) |
C.“操作1”中包括过滤及沉淀的洗涤,洗涤沉淀时最好选用饱和 溶液 溶液 |
D.隔绝空气“煅烧”时每生成 ,理论上产生标准状况下 ,理论上产生标准状况下 |
您最近一年使用:0次
解题方法
7 . 常温常压下,利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应机理如图.下列说法错误的是:
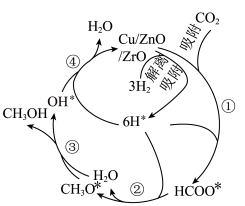

| A.Cu/ZnO/ZrO能加快反应速率,但不能改变反应热 | B.②为 |
C.转移电子数为 时消耗标准状况下 时消耗标准状况下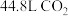 | D.总反应为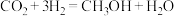 |
您最近一年使用:0次
名校
解题方法
8 . 硝酸厂烟气中的大量NO经还原法可转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是
 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是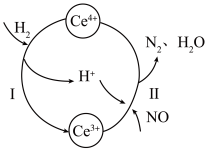
A.该转化过程的实质为NO被 还原 还原 |
| B.反应I中氧化剂与还原剂的物质的量之比为1∶2 |
C.反应II的离子反应方程式为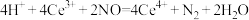 |
D.反应过程中混合溶液内 和 和 的总数不变 的总数不变 |
您最近一年使用:0次
2023-11-29更新
|
669次组卷
|
5卷引用: 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末考试化学模拟卷(二)
名校
9 . 某工厂废液中含有大量的 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下:
称取m g产品溶解于大量较浓盐酸中,在 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。
已知:①氧化性 ;
;
②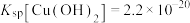 ,
, ;
;
③当溶液中离子浓度小于等于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。
根据上述产品含量测定的实验原理,下列说法错误的是
 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下: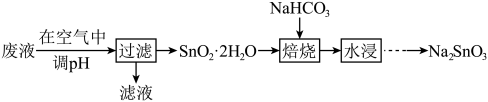
称取m g产品溶解于大量较浓盐酸中,在
 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。已知:①氧化性
 ;
;②
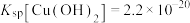 ,
, ;
;③当溶液中离子浓度小于等于
 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。根据上述产品含量测定的实验原理,下列说法错误的是
A.实验室配制 溶液时需加入盐酸和锡粉 溶液时需加入盐酸和锡粉 |
| B.若加入的还原剂不足,则测定结果偏小 |
C.滴定时选用淀粉作指示剂,产生 的离子方程式: 的离子方程式: |
D.则产品中Sn的质量分数为 % % |
您最近一年使用:0次
解题方法
10 . 过二硫酸钠(Na2S2O8)和铋酸钠(NaBiO3)都是工业上常用的强氧化剂。下列分别是 与过二硫酸钠和铋酸钠反应的离子方程式(未配平)。
与过二硫酸钠和铋酸钠反应的离子方程式(未配平)。
Ⅰ.
Ⅱ.
下列说法错误的是
 与过二硫酸钠和铋酸钠反应的离子方程式(未配平)。
与过二硫酸钠和铋酸钠反应的离子方程式(未配平)。Ⅰ.

Ⅱ.

下列说法错误的是
| A.过二硫酸钠中O(-2价)和O(-1价)含量之比为3∶1 |
| B.反应Ⅰ中氧化剂和还原剂的物质的量之比是5∶2 |
C.反应Ⅱ生成 转移电子的物质的量为5mol 转移电子的物质的量为5mol |
D.若反应Ⅰ和反应Ⅱ消耗等量的 ,则Ⅰ和Ⅱ中还原产物的物质的量之比为1∶1 ,则Ⅰ和Ⅱ中还原产物的物质的量之比为1∶1 |
您最近一年使用:0次




