名校
1 . 工业上由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备高纯碳酸锰。其主要工艺流程如图:
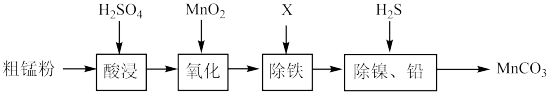
下列有关说法不正确 的是

下列有关说法
| A.可以通过搅拌的方式提高“酸浸”时粗锰粉的浸取率 |
| B.向酸浸后的滤液中加入MnO2,反应的离子方程式为:Mn4++2Fe2+=2Fe3++Mn2+ |
| C.除铁时加入的物质X作用是调节溶液的pH值,使Fe3+转化为Fe(OH)3沉淀而除去 |
| D.取除铁后的滤液,加入几滴KSCN溶液,无明显现象证明Fe3+已除尽 |
您最近一年使用:0次
2022-04-15更新
|
850次组卷
|
5卷引用:江苏省盐城市阜宁中学等四校2021-2022学年高一下学期期中考试化学试题
江苏省盐城市阜宁中学等四校2021-2022学年高一下学期期中考试化学试题江苏省海州高级中学2021-2022学年高一下学期期中考试化学试题江苏省常熟市海虞高级中学2021-2022学年高一下学期线上期中考试化学试题(已下线)微专题17 热点金属及其化合物制备流程(V、Cr、Mn、Co、Ni)-备战2023年高考化学一轮复习考点微专题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
2 . 以废旧铅蓄电池中的含铅废料( 、
、 、
、 、
、 及炭黑等)和
及炭黑等)和 为原料,可以制备高纯
为原料,可以制备高纯 ,实现铅的再生利用,其工艺流程如下:
,实现铅的再生利用,其工艺流程如下:
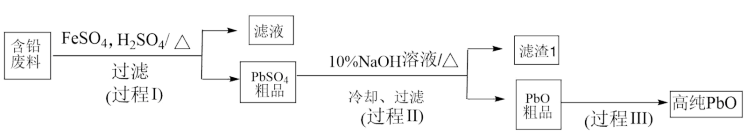
在过程Ⅰ涉及两个反应:
①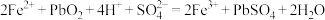 ;
;
②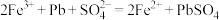 。下列说法错误的是
。下列说法错误的是
 、
、 、
、 、
、 及炭黑等)和
及炭黑等)和 为原料,可以制备高纯
为原料,可以制备高纯 ,实现铅的再生利用,其工艺流程如下:
,实现铅的再生利用,其工艺流程如下:
在过程Ⅰ涉及两个反应:
①
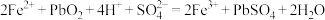 ;
;②
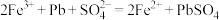 。下列说法错误的是
。下列说法错误的是A.在过程Ⅰ中, 起催化作用 起催化作用 |
B.在过程Ⅰ中生成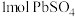 时,转移的电子数为 时,转移的电子数为 个 个 |
C.在过程Ⅰ中若改为加入 也能起到催化作用 也能起到催化作用 |
D.要证明过程Ⅰ中 起催化作用,加入 起催化作用,加入 溶液,溶液不变红色即可 溶液,溶液不变红色即可 |
您最近一年使用:0次
2022-01-20更新
|
149次组卷
|
4卷引用:江苏省响水中学2021-2022学年高二下学期开学测试化学试题
解题方法
3 . 碱金属和碱土金属元素分别位于元素周期表的ⅠA族和ⅡA族,它们的化合物应用广泛。历史上曾以NaCl为原料生产NaOH作为化学工业开端的标志。 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。
碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
A.侯氏制碱法中的物质转化: |
B.由 制备乙酸的物质转化: 制备乙酸的物质转化: |
C.电解饱和NaCl溶液的阴极反应: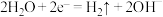 |
D. 与 与 共熔的反应: 共熔的反应: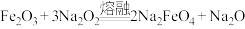 |
您最近一年使用:0次
名校
解题方法
4 . 高铁酸钾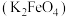 是一种环保、高效的饮用水处理剂。
是一种环保、高效的饮用水处理剂。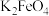 能溶于水,微溶于浓
能溶于水,微溶于浓 溶液,难溶于无水乙醇,在水处理时可转化为
溶液,难溶于无水乙醇,在水处理时可转化为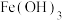 胶体。制备
胶体。制备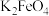 的流程如图所示,下列说法不正确的是
的流程如图所示,下列说法不正确的是
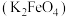 是一种环保、高效的饮用水处理剂。
是一种环保、高效的饮用水处理剂。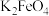 能溶于水,微溶于浓
能溶于水,微溶于浓 溶液,难溶于无水乙醇,在水处理时可转化为
溶液,难溶于无水乙醇,在水处理时可转化为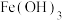 胶体。制备
胶体。制备 的流程如图所示,下列说法不正确的是
的流程如图所示,下列说法不正确的是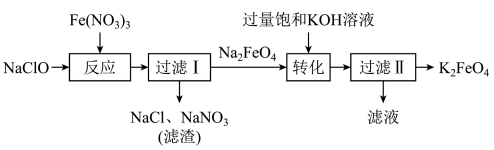
A.可以用滤纸分离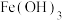 胶体和 胶体和 溶液 溶液 |
B.“反应”中,氧化剂和还原剂的物质的量之比为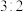 |
C.“转化”说明,该条件下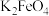 的溶解度小于 的溶解度小于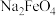 |
D.“过滤Ⅱ”所得的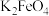 晶体可用无水乙醇洗涤 晶体可用无水乙醇洗涤 |
您最近一年使用:0次
名校
解题方法
5 . 将 通入
通入 溶液时,
溶液时, 与水生成
与水生成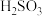 ,
,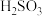 和
和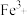 形成配合物后,通过配合物中“
形成配合物后,通过配合物中“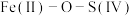 ”氧桥将
”氧桥将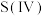 的电子传递给
的电子传递给 发生“配位体对金属的荷移”,其反应机理图示如下:
发生“配位体对金属的荷移”,其反应机理图示如下:
 通入
通入 溶液时,
溶液时, 与水生成
与水生成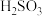 ,
,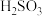 和
和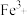 形成配合物后,通过配合物中“
形成配合物后,通过配合物中“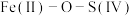 ”氧桥将
”氧桥将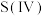 的电子传递给
的电子传递给 发生“配位体对金属的荷移”,其反应机理图示如下:
发生“配位体对金属的荷移”,其反应机理图示如下: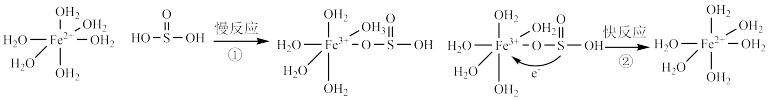
A. 分子和 分子和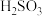 分子的硫原子杂化方式相同 分子的硫原子杂化方式相同 |
B. 与 与 溶液反应的离子方程式为 溶液反应的离子方程式为 |
C.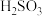 中的O与 中的O与 的配位反应决定图中总反应的速率 的配位反应决定图中总反应的速率 |
D. 中含有 中含有 键 键 |
您最近一年使用:0次
6 .  与砂糖混用可以作补血剂,实验室制备
与砂糖混用可以作补血剂,实验室制备 的流程如图所示.下列说法
的流程如图所示.下列说法不正确 的是

 与砂糖混用可以作补血剂,实验室制备
与砂糖混用可以作补血剂,实验室制备 的流程如图所示.下列说法
的流程如图所示.下列说法
A.可利用 溶液检验 溶液检验 溶液是否变质 溶液是否变质 |
B.沉淀过程发生反应的离子方程式为: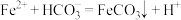 |
| C.可利用盐酸酸化的氯化钡溶液检验沉淀是否洗涤干净 |
D. 在空气中高温分解不能得到纯净的 在空气中高温分解不能得到纯净的 |
您最近一年使用:0次
7 . 由铁及其化合物可制得铁红(Fe2O3)、氧化铁、绿矾(FeSO4•7H2O)、高铁酸钾(K2FeO4)、铁黄(FeOOH)等物质。高铁酸钾是一种既能杀菌、消毒,又能絮凝净水的水处理剂,能与水反应生成氢氧化铁和氧气。铁黄可用作生产磁性材料、颜料的原料。工业制备K2FeO4的离子方程式为Fe(OH)3+ClO-+OH-→FeO +Cl-+H2O(未配平)。下列有关说法
+Cl-+H2O(未配平)。下列有关说法不正确 的是
 +Cl-+H2O(未配平)。下列有关说法
+Cl-+H2O(未配平)。下列有关说法| A.K2FeO4中Fe显+6价 |
B.ClO-的氧化性大于FeO |
| C.上述反应中氧化剂和还原剂的物质的量之比为3:2 |
| D.每1molK2FeO4与水反应,产生0.5molO2 |
您最近一年使用:0次
名校
解题方法
8 . 土壤中的 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法不正确 的是
 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法A. 被氧化为 被氧化为 的过程中, 的过程中, 与 与 的物质的量之比为 的物质的量之比为 |
B.在反硝化过程中,土壤 降低 降低 |
C. 与 与 反应时,每生成 反应时,每生成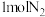 ,转移电子数为 ,转移电子数为 |
| D.适当疏松土壤,有利于提高铵态氮肥的肥效 |
您最近一年使用:0次
9 . 周期表第ⅤA族元素及其化合物用途广泛。 在强碱性条件下能被NaClO氧化生成肼(
在强碱性条件下能被NaClO氧化生成肼( ),常温下
),常温下 呈液态,是常用的火箭燃料。
呈液态,是常用的火箭燃料。 的燃烧热为624kJ/mol,
的燃烧热为624kJ/mol, 可被NaClO氧化生成
可被NaClO氧化生成 ,也可被
,也可被 氧化生成
氧化生成 ,
, 是一种弱酸,酸性与醋酸相当。
是一种弱酸,酸性与醋酸相当。 与
与 高温条件下可制备半导体材料砷化镓,
高温条件下可制备半导体材料砷化镓, 的沸点为55℃。下列化学反应或说法不正确的是
的沸点为55℃。下列化学反应或说法不正确的是
 在强碱性条件下能被NaClO氧化生成肼(
在强碱性条件下能被NaClO氧化生成肼( ),常温下
),常温下 呈液态,是常用的火箭燃料。
呈液态,是常用的火箭燃料。 的燃烧热为624kJ/mol,
的燃烧热为624kJ/mol, 可被NaClO氧化生成
可被NaClO氧化生成 ,也可被
,也可被 氧化生成
氧化生成 ,
, 是一种弱酸,酸性与醋酸相当。
是一种弱酸,酸性与醋酸相当。 与
与 高温条件下可制备半导体材料砷化镓,
高温条件下可制备半导体材料砷化镓, 的沸点为55℃。下列化学反应或说法不正确的是
的沸点为55℃。下列化学反应或说法不正确的是A.制备 时,应将 时,应将 缓缓通入NaClO溶液中 缓缓通入NaClO溶液中 |
B. 与 与 反应方程式为 反应方程式为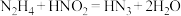 |
C.向 溶液中通入HCl可以制得 溶液中通入HCl可以制得 |
D. 燃烧的热化学方程式为: 燃烧的热化学方程式为: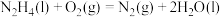  |
您最近一年使用:0次
名校
10 . 工业上用生物法处理H2S的原理如下:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2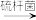 2Fe(SO4)3+2H2O
2Fe(SO4)3+2H2O
以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2
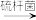 2Fe(SO4)3+2H2O
2Fe(SO4)3+2H2O以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

| A.上述总反应方程式为:2H2S+O2=2S↓+2H2O,Fe2(SO4)3是该反应的催化剂 |
| B.当反应温度过高时,Fe2+氧化速率下降的原因可能是硫杆菌失去活性 |
| C.由图-1、图-2可得出结论:使用硫杆菌作催化剂的最佳条件为30℃、pH=2.0 |
| D.当反应1中转移0.1mol电子时,反应1中消耗的H2S在标准状况下的体积为2.24L |
您最近一年使用:0次
2024-02-14更新
|
143次组卷
|
2卷引用:江苏省镇江市2023-2024学年高一上学期期末考试化学试题



