解题方法
1 . 钯是航天航空高科技领域的重要材料。工业用粗钯制备高纯度钯的流程如图:
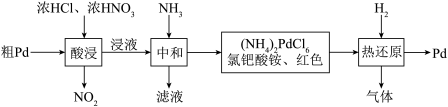
下列说法正确的是

下列说法正确的是
A.酸浸时反应的化学方程式是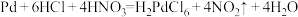 |
| B.“热还原”中每生成1mol Pd同时生成的气体的物质的量为4mol |
C.化学实验中可利用氯钯酸根离子检验溶液中是否含有 |
| D.在“酸浸”过程中为加快反应速率可用浓硫酸代替浓盐酸 |
您最近一年使用:0次
2 . 黄铁矿(主要成分 ),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是
),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是
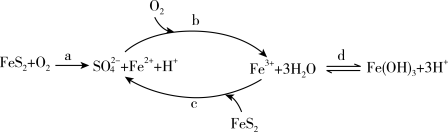
 ),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是
),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是
| A.发生反应a时,0.05molFeS2被氧化时消耗标准状况下空气的体积大约19.6L |
| B.为了验证b过程反应后溶液中含Fe2+,可选用KSCN溶液和氯水 |
C.c发生反应的离子方程式为: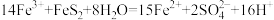 |
| D.总反应中氧化剂是O2 与Fe3+ |
您最近一年使用:0次
解题方法
3 . 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
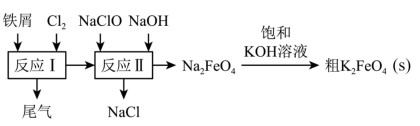
下列叙述不正确的是

下列叙述不正确的是
| A.反应I产生的尾气可通入碱液中吸收 |
| B.反应I生成的FeCl2,在碱性条件下会被NaClO氧化成Na2FeO4 |
| C.反应II中每转移6mol电子会生成166gNa2FeO4 |
| D.Na2FeO4转化成K2FeO4的化学方程式为Na2FeO4+2KOH=K2FeO4↓+2NaOH |
您最近一年使用:0次
名校
解题方法
4 . 硫酸亚铁铵是一种重要的化工原料,用途十分广泛。实验室可用如图所示流程制备硫酸亚铁铵,下列说法错误的是


| A.步骤①中用Na2CO3溶液处理的目的是去除废铁屑表面的油污 |
| B.为了提高产率,步骤②中硫酸一定要过量 |
| C.步骤②中发生的氧化还原反应主要有Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+ |
| D.步骤③的操作为蒸发结晶 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验的反应原理用离子方程式表示正确的是
A.水玻璃中通入少量 : : |
B.用稀硫酸酸化的KMnO溶液与少量 反应: 反应: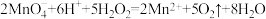 |
C.新制氯水中加入少量 : : |
D. 溶液中滴加 溶液中滴加 溶液至 溶液至 恰好完全沉淀: 恰好完全沉淀: |
您最近一年使用:0次
名校
解题方法
6 . 以废锌电池预处理物(主要成分为 ,另含少量
,另含少量 等)为原料可生产草酸锌晶体
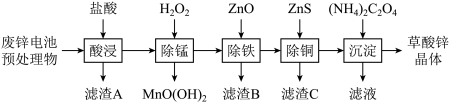
等)为原料可生产草酸锌晶体 ,生产工艺如下图所示。下列关于草酸锌晶体生产工艺,说法正确的是
,生产工艺如下图所示。下列关于草酸锌晶体生产工艺,说法正确的是
 ,另含少量
,另含少量 等)为原料可生产草酸锌晶体
等)为原料可生产草酸锌晶体 ,生产工艺如下图所示。下列关于草酸锌晶体生产工艺,说法正确的是
,生产工艺如下图所示。下列关于草酸锌晶体生产工艺,说法正确的是
A.“滤渣A”主要成分为 |
B.“除锰”的离子方程式: |
C.“除锰”后的溶液中主要存在的阳离子有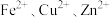 |
D.“除铁”过程中,可以用 代替 代替 |
您最近一年使用:0次
2022-10-07更新
|
389次组卷
|
3卷引用:湖南省长沙市长郡中学2023届高三上学期第二次月考化学试题
7 . 在特定碱性条件下,过量H2O2可将Cr(Ⅲ)完全氧化成Cr(Ⅵ),其反应为H2O2+CrO +W→CrO
+W→CrO +Y(未配平),下列有关说法正确的是
+Y(未配平),下列有关说法正确的是
 +W→CrO
+W→CrO +Y(未配平),下列有关说法正确的是
+Y(未配平),下列有关说法正确的是| A.Y为OH- |
| B.上述反应中氧化剂和还原剂的物质的量之比为3∶2 |
| C.1 mol H2O2参加反应时,转移电子的物质的量为6 mol |
D.在酸性条件下CrO 可以转化为Cr2O 可以转化为Cr2O |
您最近一年使用:0次
2022-10-04更新
|
142次组卷
|
2卷引用:湖南省邵阳市新宁县崀山培英学校2022届高三下学期第三次模拟考试化学试题
名校
解题方法
8 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示。下列说法正确的是
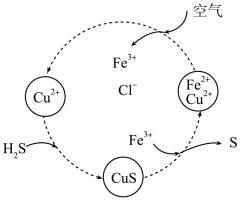

| A.可通过点燃的方法除去尾气中的H2S |
| B.H2S具有还原性 |
| C.在图示转化过程中,只有两种元素的化合价不变 |
| D.回收S的总反应为2H2S+O2= 2H2O+S↓ |
您最近一年使用:0次
名校
解题方法
9 . 磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]是常用的电极材料,其制备流程如下:
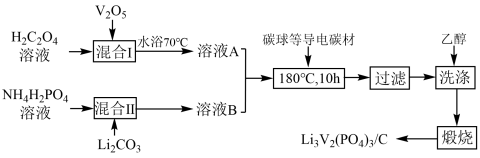
已知: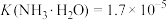 ,H3PO4的电离常数
,H3PO4的电离常数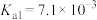 、
、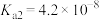 、
、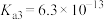 ,下列说法正确的是
,下列说法正确的是

已知:
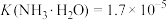 ,H3PO4的电离常数
,H3PO4的电离常数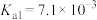 、
、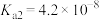 、
、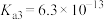 ,下列说法正确的是
,下列说法正确的是| A.NH4H2PO4溶液显碱性 |
| B.复合材料中V的化合价为+3 |
| C.“洗涤”时用乙醇而不用水的目的是减少产品损耗 |
D.“混合Ⅰ”时发生反应的化学方程式为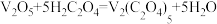 |
您最近一年使用:0次
解题方法
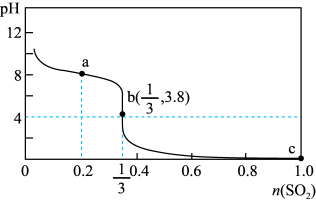
10 . 常温下,向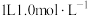 的NaClO溶液中缓慢通入
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
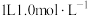 的NaClO溶液中缓慢通入
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
A.常温下,HClO电离平衡常数的数量级为 |
| B.水的电离程度:a<b<c |
C.b点溶液中: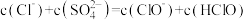 |
D.c点溶液中: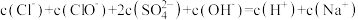 |
您最近一年使用:0次



