1 . 焦锑酸钠 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。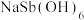 难溶于水。
难溶于水。
②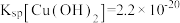 ,
, 。
。
回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是_______ ,“浸渣”的主要成分是_______ (填“ ”或“CuS”)。
”或“CuS”)。
(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为_______ 。
(3)“氧化”时,溶液中的 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式_______ 。
(4)“滤液”的主要成分是_______ 。
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定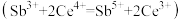 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。
①硫酸肼的作用是_______ 。
②产品的纯度为_______ [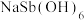 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。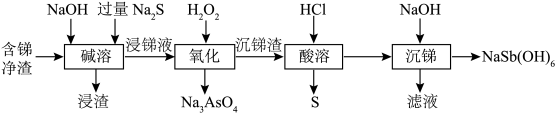
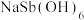 难溶于水。
难溶于水。②
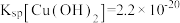 ,
, 。
。回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是
 ”或“CuS”)。
”或“CuS”)。(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为
(3)“氧化”时,溶液中的
 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式(4)“滤液”的主要成分是
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定
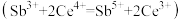 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。①硫酸肼的作用是
②产品的纯度为
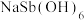 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
您最近一年使用:0次
名校
2 . 普鲁士蓝可用于氨氮废水的处理,利用柠檬酸铁铵和赤血盐可制备得到普鲁士蓝。
Ⅰ.柠檬酸铁铵的制备
实验步骤:向已加有铁粉的三颈烧瓶中滴加柠檬酸溶液并搅拌,控温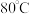 至生成柠檬酸亚铁白色沉淀。降温至
至生成柠檬酸亚铁白色沉淀。降温至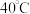 ,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温
,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温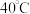 ,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。
,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。 的名称是
的名称是______ 。
(2)控温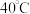 的原因
的原因______ 。
(3)“一系列操作”包括蒸发浓缩、冷却结晶、过滤、______ 、干燥。
Ⅱ.赤血盐的制备
用 在
在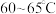 氧化黄血盐
氧化黄血盐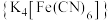 制备赤血盐
制备赤血盐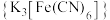 的装置如下图所示(夹持装置略)。
的装置如下图所示(夹持装置略)。______ ,装置B中试剂是______ 。
(5)反应结束后通入 一段时间的目的
一段时间的目的______ 。
(6)黄血盐会被酸性高锰酸钾彻底氧化为 和
和 ,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因
,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因______ 。
Ⅲ.普鲁士蓝的制备及应用
在紫外光作用下柠檬酸铁铵中的三价铁离子被还原为二价铁离子,再与赤血盐反应,进行电子转移后生成相对稳定的普鲁士蓝。酸化后的普鲁士蓝加双氧水可处理氨氮废水(主要含 ),原理如下:
),原理如下:
ⅰ.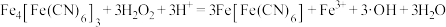
ⅱ. 将氨氮氧化为
将氨氮氧化为
(7)用实验制得的普鲁士蓝处理某氨氮废水,收集到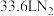 (已折成标准状况)。实验中消耗的
(已折成标准状况)。实验中消耗的 的质量至少为
的质量至少为______ g。
Ⅰ.柠檬酸铁铵的制备
实验步骤:向已加有铁粉的三颈烧瓶中滴加柠檬酸溶液并搅拌,控温
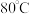 至生成柠檬酸亚铁白色沉淀。降温至
至生成柠檬酸亚铁白色沉淀。降温至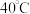 ,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温
,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温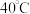 ,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。
,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。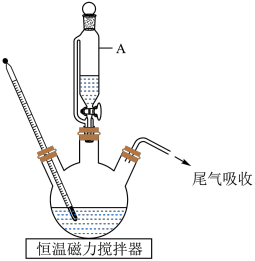
 的名称是
的名称是(2)控温
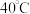 的原因
的原因(3)“一系列操作”包括蒸发浓缩、冷却结晶、过滤、
Ⅱ.赤血盐的制备
用
 在
在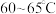 氧化黄血盐
氧化黄血盐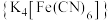 制备赤血盐
制备赤血盐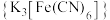 的装置如下图所示(夹持装置略)。
的装置如下图所示(夹持装置略)。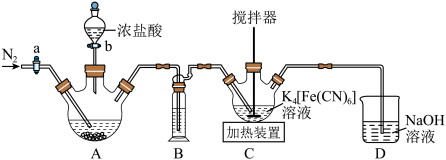
(5)反应结束后通入
 一段时间的目的
一段时间的目的(6)黄血盐会被酸性高锰酸钾彻底氧化为
 和
和 ,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因
,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因Ⅲ.普鲁士蓝的制备及应用
在紫外光作用下柠檬酸铁铵中的三价铁离子被还原为二价铁离子,再与赤血盐反应,进行电子转移后生成相对稳定的普鲁士蓝。酸化后的普鲁士蓝加双氧水可处理氨氮废水(主要含
 ),原理如下:
),原理如下:ⅰ.
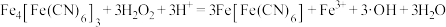
ⅱ.
 将氨氮氧化为
将氨氮氧化为
(7)用实验制得的普鲁士蓝处理某氨氮废水,收集到
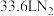 (已折成标准状况)。实验中消耗的
(已折成标准状况)。实验中消耗的 的质量至少为
的质量至少为
您最近一年使用:0次
2024-05-16更新
|
171次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
解题方法
3 . 氯化六氨合钴{ }是合成多种钴基功能材料和催化剂的中间体。已知:
}是合成多种钴基功能材料和催化剂的中间体。已知: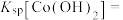
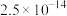 、
、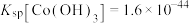 、
、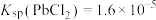 ;电对的标准电极电势(
;电对的标准电极电势( )越大,在水溶液中越容易发生还原反应,
)越大,在水溶液中越容易发生还原反应,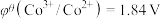 、
、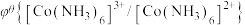
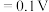 。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
步骤一:称取3.0g CoCl2·6H2O,研磨后与4.0g NH4Cl混匀后溶于适量蒸馏水中,加入1.5g活性炭,搅拌均匀并冷却至室温;
步骤二;继续加入7mL浓氨水充分反应,再冷却至10℃后逐滴加入7mL 6%的双氧水,控制温度55℃充分反应;
步骤三:将反应后所得体系迅速冷却至2℃,过滤、洗涤;所得沉淀转入烧杯,加入20mL 80℃蒸馏水和1mL浓盐酸,趁热过滤,收集滤液;
步骤四:将滤液浓缩后加入3.5mL浓盐酸,并迅速冷却至2℃,抽滤、乙醇洗涤、干燥,收集得1.9g产品。
回答下列问题:
(1)步骤一中,下列仪器不需要使用的是___________ (填仪器名称)。___________ ;控制反应温度在55℃的原因为___________ 。
(3)相同条件下,氯化六氨合钴在稀盐酸中的溶解度___________ (填“大于”“小于”或“等于”)在浓盐酸中的。
(4)与步骤三中过滤相比,步骤四中抽滤的优点为___________ 。
(5)制备产品的总反应方程式为___________ ;步骤二中双氧水可用PbO2或KMnO4代替,其中更适合选用___________ (填化学式)代替双氧水,原因为___________ 。
(6)本实验所得产品的产率为___________ (列出计算式)。
 }是合成多种钴基功能材料和催化剂的中间体。已知:
}是合成多种钴基功能材料和催化剂的中间体。已知: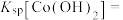
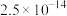 、
、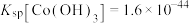 、
、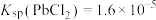 ;电对的标准电极电势(
;电对的标准电极电势( )越大,在水溶液中越容易发生还原反应,
)越大,在水溶液中越容易发生还原反应,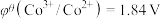 、
、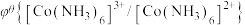
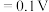 。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
。某学习小组在实验室中制备氯化六氨合钴的步骤如下:步骤一:称取3.0g CoCl2·6H2O,研磨后与4.0g NH4Cl混匀后溶于适量蒸馏水中,加入1.5g活性炭,搅拌均匀并冷却至室温;
步骤二;继续加入7mL浓氨水充分反应,再冷却至10℃后逐滴加入7mL 6%的双氧水,控制温度55℃充分反应;
步骤三:将反应后所得体系迅速冷却至2℃,过滤、洗涤;所得沉淀转入烧杯,加入20mL 80℃蒸馏水和1mL浓盐酸,趁热过滤,收集滤液;
步骤四:将滤液浓缩后加入3.5mL浓盐酸,并迅速冷却至2℃,抽滤、乙醇洗涤、干燥,收集得1.9g产品。
回答下列问题:
(1)步骤一中,下列仪器不需要使用的是
(3)相同条件下,氯化六氨合钴在稀盐酸中的溶解度
(4)与步骤三中过滤相比,步骤四中抽滤的优点为
(5)制备产品的总反应方程式为
(6)本实验所得产品的产率为
您最近一年使用:0次
2024-05-16更新
|
169次组卷
|
3卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高三下学期4月模拟测试化学试题
名校
4 . 某工业废催化剂主要成份为: 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:_______ (填化学式)。
(2)水浸渣的主要成份是_______ (填化学式)。
(3)“沉淀”的化学式_______ 。生成该沉淀的化学方程式_______ 。
(4)“沉钒”中需要加入过量的浓 ,结合离子方程式说明原因是
,结合离子方程式说明原因是_______ 。写出生成 的化学方程式
的化学方程式_______ 。
(5)淀粉水解液中_______ (填化学式)起还原作用,用焦亚硫酸钠( )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式_______ 。
(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时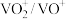 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。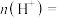
_______ mol。
 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示: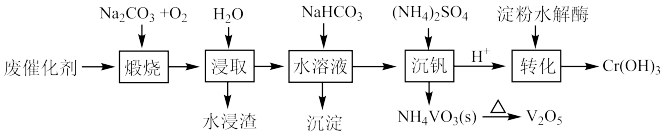
(2)水浸渣的主要成份是
(3)“沉淀”的化学式
(4)“沉钒”中需要加入过量的浓
 ,结合离子方程式说明原因是
,结合离子方程式说明原因是 的化学方程式
的化学方程式(5)淀粉水解液中
 )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时
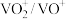 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。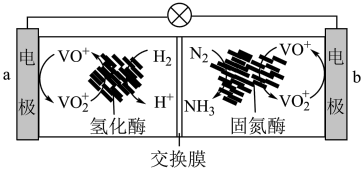
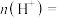
您最近一年使用:0次
5 . 锂电池的研发、使用及废电池的回收具有重要意义。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为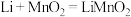 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是___________ (填序号)。
A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀 作电解质
作电解质
(2)钴酸锂( )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。
①钴酸锂电池放电时示意图如图1所示。放电时, 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式:___________ 。 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=___________ 。 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。___________ 。
②与 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:___________ 。
(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用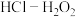 混合物作浸取剂。
混合物作浸取剂。
①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:___________ 。
②工业生产时在盐酸中加入 ,
, 的作用是
的作用是___________ 。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为
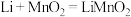 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀
 作电解质
作电解质(2)钴酸锂(
 )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。①钴酸锂电池放电时示意图如图1所示。放电时,
 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式: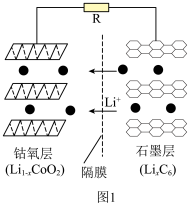
 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=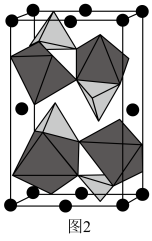
 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。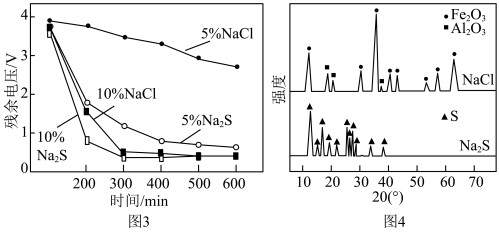
②与
 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为
 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用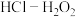 混合物作浸取剂。
混合物作浸取剂。①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:
②工业生产时在盐酸中加入
 ,
, 的作用是
的作用是
您最近一年使用:0次
解题方法
6 . 高纯二硫化钼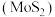 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量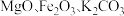 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)“焙烧”时生成 的化学方程式为
的化学方程式为___________ ;“水洗”的目的是___________ 。
(2)“转化”过程中,存在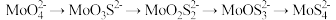 。
。
① 转化为
转化为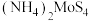 的化学方程式为
的化学方程式为___________ 。
②保持温度为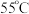 反应
反应 后,冷却至
后,冷却至 并静置
并静置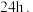 测得
测得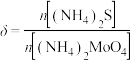 对
对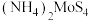 晶体产率的影响如图所示。
晶体产率的影响如图所示。 时,
时,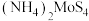 晶体产率为0的原因是
晶体产率为0的原因是___________ ; 时,
时,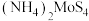 晶体产率继续增大的原因是
晶体产率继续增大的原因是___________ 。
(3)“酸浸”和“高温还原”中产生的气体可通入___________ (填操作单元的名称)中循环使用。
(4) 也可由
也可由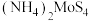 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为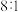 ,则硫单质的分子式为
,则硫单质的分子式为___________ 。
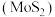 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量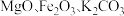 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。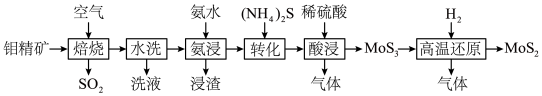
(1)“焙烧”时生成
 的化学方程式为
的化学方程式为(2)“转化”过程中,存在
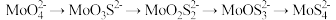 。
。①
 转化为
转化为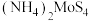 的化学方程式为
的化学方程式为②保持温度为
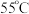 反应
反应 后,冷却至
后,冷却至 并静置
并静置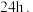 测得
测得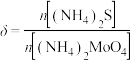 对
对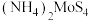 晶体产率的影响如图所示。
晶体产率的影响如图所示。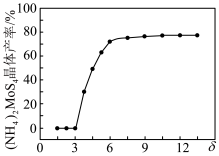
 时,
时,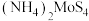 晶体产率为0的原因是
晶体产率为0的原因是 时,
时,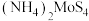 晶体产率继续增大的原因是
晶体产率继续增大的原因是(3)“酸浸”和“高温还原”中产生的气体可通入
(4)
 也可由
也可由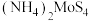 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为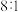 ,则硫单质的分子式为
,则硫单质的分子式为
您最近一年使用:0次
7 . 镍、钴均是一种重要的战略资源,广泛应用于飞机发动机、锂离子电池等领域。以红土镍矿常压盐酸浸液(含 、
、 、
、 、
、 、
、 和
和 )为原料提取Ni、Co。工艺流程如下:
)为原料提取Ni、Co。工艺流程如下:
回答下列问题:
(1)滤渣1的成分是 、
、___________ 。
(2)“调 ”时,发生反应的主要化学方程式为
”时,发生反应的主要化学方程式为___________ 。
(3)“碱性氧化”时,由 转化为
转化为 的离子方程式为
的离子方程式为___________ ,常温下,若pH控制为9,则溶液中 浓度最多为
浓度最多为___________ mol·L 。
。
(4)“析晶”时,通入的酸性气体A为___________ (化学式)。
(5)①“电解”时Ni在___________ (“阴”或“阳”)极析出。
②Ni可以进一步制备超导体 ,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为
,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为___________ (“顶点”“面心”或“体心”),晶体中一个C周围与其最近的Ni的个数为___________ 。
 、
、 、
、 、
、 、
、 和
和 )为原料提取Ni、Co。工艺流程如下:
)为原料提取Ni、Co。工艺流程如下: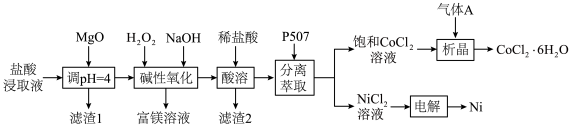
| 物质 |  |  |  |  |  |  |
 |  | 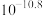 | 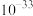 | 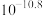 |  |  |
(1)滤渣1的成分是
 、
、(2)“调
 ”时,发生反应的主要化学方程式为
”时,发生反应的主要化学方程式为(3)“碱性氧化”时,由
 转化为
转化为 的离子方程式为
的离子方程式为 浓度最多为
浓度最多为 。
。(4)“析晶”时,通入的酸性气体A为
(5)①“电解”时Ni在
②Ni可以进一步制备超导体
 ,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为
,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为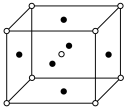
您最近一年使用:0次
解题方法
8 . 高砷烟尘(主要成分有 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下: 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为________ ,滤渣的主要成分为________ (填化学式)。 ,发生反应的离子方程式为
,发生反应的离子方程式为________ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
________ 。
(3)“还原”后溶液酸性增强,主要原因是________ (用离子方程式表示)。
(4)“结晶”操作为________ 、过滤、洗涤、干燥。
(5)“萃余液”中含有的金属阳离子为________ (填离子符号),将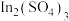 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为________ 。
 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下:
 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为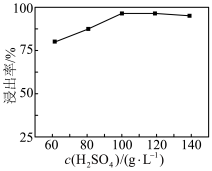
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(3)“还原”后溶液酸性增强,主要原因是
(4)“结晶”操作为
(5)“萃余液”中含有的金属阳离子为
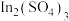 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . 二氯异氰尿酸钠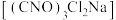 具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和
具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和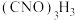 (氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(1)装置B中试剂为___________ 。
(2) 的制备步骤如下:
的制备步骤如下:
①检查装置气密性后加入药品。
②关闭K1,打开K2,向A中滴加足量的浓盐酸,关闭K2,当观察到___________ 时,滴入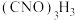 的吡啶溶液,写出
的吡啶溶液,写出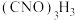 和NaClO发生反应的化学方程式
和NaClO发生反应的化学方程式___________ 。制备过程中要不断通入Cl2,其目的是___________ ,反应完成后需进行的操作为___________ 。
③取装置D中溶液,制得产品。操作为___________ 、过滤、冷水洗涤、低温干燥得到粗产品。
(3)粗产品中 纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量
纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量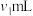
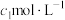 的AgNO3溶液,加入几滴稀
的AgNO3溶液,加入几滴稀 溶液,用
溶液,用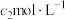 NH4SCN标准溶液滴定至终点,消耗
NH4SCN标准溶液滴定至终点,消耗 标准液。[已知:
标准液。[已知: (白色)]
(白色)]
① (摩尔质量为
(摩尔质量为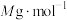 )的纯度为
)的纯度为___________ 。
②下列有关上述滴定操作的说法正确的是___________ 。
a.接近滴定终点时微微转动活塞,使溶液悬挂在尖嘴上,形成半滴,用锥形瓶内壁将其刮落
b.若盛放NH4SCN标准溶液的滴定管没有润洗,使测定结果偏大
c.锥形瓶洗涤后未干燥即加入所配待测溶液,使测定结果偏小
d.滴定前俯视读数,滴定后仰视读数,使测定结果偏小
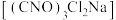 具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和
具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和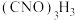 (氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(1)装置B中试剂为
(2)
 的制备步骤如下:
的制备步骤如下:①检查装置气密性后加入药品。
②关闭K1,打开K2,向A中滴加足量的浓盐酸,关闭K2,当观察到
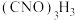 的吡啶溶液,写出
的吡啶溶液,写出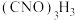 和NaClO发生反应的化学方程式
和NaClO发生反应的化学方程式③取装置D中溶液,制得产品。操作为
(3)粗产品中
 纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量
纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量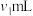
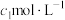 的AgNO3溶液,加入几滴稀
的AgNO3溶液,加入几滴稀 溶液,用
溶液,用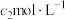 NH4SCN标准溶液滴定至终点,消耗
NH4SCN标准溶液滴定至终点,消耗 标准液。[已知:
标准液。[已知: (白色)]
(白色)]①
 (摩尔质量为
(摩尔质量为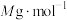 )的纯度为
)的纯度为②下列有关上述滴定操作的说法正确的是
a.接近滴定终点时微微转动活塞,使溶液悬挂在尖嘴上,形成半滴,用锥形瓶内壁将其刮落
b.若盛放NH4SCN标准溶液的滴定管没有润洗,使测定结果偏大
c.锥形瓶洗涤后未干燥即加入所配待测溶液,使测定结果偏小
d.滴定前俯视读数,滴定后仰视读数,使测定结果偏小
您最近一年使用:0次
解题方法
10 .  和
和 都具有广泛的用途。
都具有广泛的用途。
Ⅰ.工业上用软锰矿(主要含 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。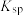
(1)为提高浸出速率,可采取的措施有_________________ (答出两条即可)。
(2)浸出过程中产生的 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。
ⅰ.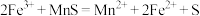 ;
;
ⅱ._________________ (离子方程式)。
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:_____________ 。
(4)滤渣2的主要成分是_________________ 。
Ⅱ.以 溶液为原料,用图1装置(
溶液为原料,用图1装置(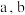 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。_________________ 。
(6)图1中 电极上
电极上 的电解效率
的电解效率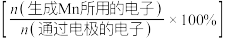 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是_________________ 。
 和
和 都具有广泛的用途。
都具有广泛的用途。Ⅰ.工业上用软锰矿(主要含
 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。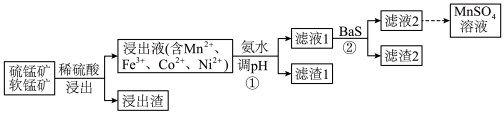
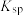
| 硫化物 |  |  |  |  (易溶) (易溶) |
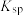 | 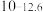 | 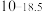 |  | |
| 氢氧化物 |  |  |  |  |
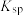 | 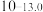 | 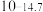 | 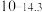 |  |
(1)为提高浸出速率,可采取的措施有
(2)浸出过程中产生的
 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。ⅰ.
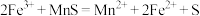 ;
;ⅱ.
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:
(4)滤渣2的主要成分是
Ⅱ.以
 溶液为原料,用图1装置(
溶液为原料,用图1装置( 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。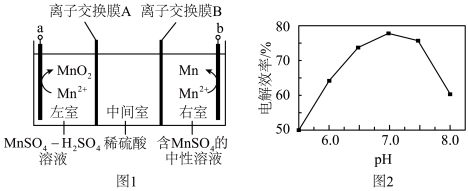
(6)图1中
 电极上
电极上 的电解效率
的电解效率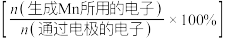 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是
您最近一年使用:0次



