名校
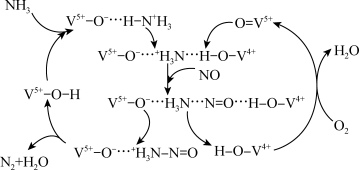
1 . 科学家研究了钒系 催化剂催化脱硝机理,部分反应机理如下图所示。有关该过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)
催化剂催化脱硝机理,部分反应机理如下图所示。有关该过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)
 催化剂催化脱硝机理,部分反应机理如下图所示。有关该过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)
催化剂催化脱硝机理,部分反应机理如下图所示。有关该过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)
A. 是反应中间体 是反应中间体 | B.反应过程中V的成键数目发生变化 |
C.反应过程中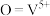 被还原 被还原 | D.脱硝反应为: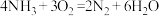 |
您最近一年使用:0次
2022-05-20更新
|
1275次组卷
|
4卷引用:宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题(尖子班)
宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题(尖子班)广东省2022届高三综合能力测试(三)化学试题(已下线)第二章 化学物质及其变化(测)-2023年高考化学一轮复习讲练测(全国通用)新疆维吾尔自治区乌鲁木齐市实验学校2023-2024学年高三上学期1月月考化学试题
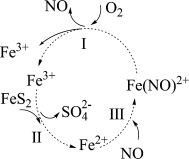
2 . 黄铁矿(主要成分为 )因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下
)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下 可发生如图所示的转化。下列分析错误的是
可发生如图所示的转化。下列分析错误的是
 )因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下
)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下 可发生如图所示的转化。下列分析错误的是
可发生如图所示的转化。下列分析错误的是 
| A.反应Ⅰ、Ⅱ为氧化还原反应 |
B.反应Ⅰ的离子方程式: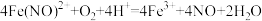 |
C.反应Ⅱ中,每消耗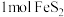 ,转移电子的物质的量为 ,转移电子的物质的量为 |
D.在酸性条件下,黄铁矿催化氧化中 和 和 均作催化剂 均作催化剂 |
您最近一年使用:0次
2022-04-20更新
|
371次组卷
|
5卷引用:宁夏固原市第一中学2023届高三上学期第二次月考化学试题
宁夏固原市第一中学2023届高三上学期第二次月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高三上学期期中考试化学试题辽宁省沈阳市同泽高级中学2020--2021 学年高一下学期4月月考化学试卷(已下线)第03练 氧化还原反应-2023年高考化学一轮复习小题多维练(全国通用)江西省宜春市丰城市东煌学校2022-2023学年高三上学期期中考试化学试卷
名校
3 . 一种海水提溴的部分工艺流程如图所示。下列说法错误的是
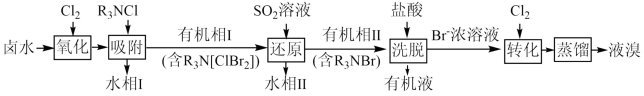

A.“氧化”和“转化”工序中 的主要作用相同 的主要作用相同 |
B.水相Ⅰ和水相Ⅱ中均含有 和 和 |
C.“洗脱”工序可完成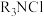 的再生 的再生 |
| D.保存液溴时加适量水的主要作用是防止溴单质被氧化 |
您最近一年使用:0次
2022-04-16更新
|
2360次组卷
|
9卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题湖南省隆回县第二中学2021-2022学年高三4月模拟考试化学试题(已下线)专题14 物质的反应和转化-三年(2020-2022)高考真题分项汇编(已下线)微专题02 化学与STSE-备战2023年高考化学一轮复习考点微专题(已下线)微专题19 海水资源的综合利用(提取溴和碘)-备战2023年高考化学一轮复习考点微专题江苏省扬州中学2022-2023学年高三上学期11月月考化学试题江苏省灌南高级中学2023-2024学年高三上学期暑期检测(二)化学试题江苏省靖江高级中学、华罗庚中学2023-2024学年高三上学期第一次阶段考试化学试题江苏省南京师范大学苏州实验学校2023-2024学年高三上学期零模考试热身练化学试题
名校
4 . 实验室用50mL浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为(未配平)KClO3+HCl—KCl+Cl2↑+H2O。
(1)配平上述反应化学方程式:______ 。
(2)若产生0.1molCl2,则转移电子的物质的量为_______ mol。
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是_____ mol,转移电子是______ mol。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是_____ 。
(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_____ 。
(1)配平上述反应化学方程式:
(2)若产生0.1molCl2,则转移电子的物质的量为
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与
 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题:
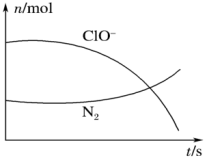
(1)某反应体系中有H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式_______ ,消耗1 mol还原剂,转移电子数为_______ 。
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是_______ ,相关反应的离子方程式是_______ 。
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为_______ ,生成的还原产物的质量为_______ g。
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式_____ 。
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
(1)某反应体系中有H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO
 + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
您最近一年使用:0次
名校
6 . 空气吹出法是工业规模海水提溴的常用方法,流程如下:

下列说法不正确的是

下列说法不正确的是
A.获得工业 的方法是过滤 的方法是过滤 |
| B.步骤②③的目的是富集溴元素 |
C.步骤①发生的主要反应为: |
D.步骤②发生的主要反应为: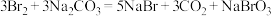 |
您最近一年使用:0次
2022-02-21更新
|
343次组卷
|
6卷引用:宁夏石嘴山市平罗中学2021-2022学年高一下学期第一次月考化学试题
宁夏石嘴山市平罗中学2021-2022学年高一下学期第一次月考化学试题陕西省渭南市临渭区2021-2022学年高一上学期期末教学质量检测化学试题(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)吉林省吉林市第一中学2022-2023学年高一6月月考(线上)化学试题黑龙江省大庆市大庆中学2022-2023学年高一下学期7月期末考试化学试题(已下线)第八章 化学与可持续发展【单元测试B卷】
名校
解题方法
7 . Ⅰ.明胶是水溶性蛋白质混合物,溶于水形成胶体。工业明胶含有重金属 ,对人体有害。
,对人体有害。
(1)已知 中
中 是一种酸根离子,则
是一种酸根离子,则 属于
属于___________ (填“酸”“碱”“盐”或“氧化物”), 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)明胶的水溶液和 溶液共同具有的性质是
溶液共同具有的性质是___________ (填字母)。
A.都不稳定,密封放置会产生沉淀 B.两者均有丁达尔效应 C.分散质粒子都可通过滤纸
Ⅱ. 是银白色金属,化学性质稳定,
是银白色金属,化学性质稳定, 价和
价和 价为常见价态。工业上以铬铁矿(主要成分为
价为常见价态。工业上以铬铁矿(主要成分为 ,含
,含
 等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠
等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠 ,其主要工艺流程如下。
,其主要工艺流程如下。

查阅资料:常温下, 不溶于水,有强氧化性,在碱性条件下,能将
不溶于水,有强氧化性,在碱性条件下,能将 转化为
转化为 。
。
(3)工业上常采用热还原法制备金属铬,写出以 为原料,利用铝热反应制取金属铬的化学方程式:
为原料,利用铝热反应制取金属铬的化学方程式:___________ 。
(4)酸化滤液D时,用硫酸而不用盐酸,可能的原因是___________ 。
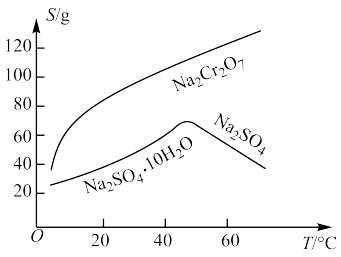
(5)固体E的主要成分是 ,根据下图分析操作a为
,根据下图分析操作a为___________ 、___________ 。
(6)电镀厂产生的镀铜废水中往往含有一定量的 ,处理该废水常用还原沉淀法,具体流程如下:
,处理该废水常用还原沉淀法,具体流程如下:

① 的化学性质与
的化学性质与 相似。在上述生产过程中加入
相似。在上述生产过程中加入 溶液时要控制溶液的
溶液时要控制溶液的 不能过高,是因为
不能过高,是因为___________ (用离子方程式表示)。
②下列溶液中可以代替上述流程中 溶液的是
溶液的是___________ (填字母)。
A.浓硫酸 B.酸性 溶液 C.
溶液 C. 溶液
溶液
③上述流程中,每消耗0.1mol 转移0.8mole-,则加入
转移0.8mole-,则加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为___________ 。
 ,对人体有害。
,对人体有害。(1)已知
 中
中 是一种酸根离子,则
是一种酸根离子,则 属于
属于 中铁元素的化合价为
中铁元素的化合价为(2)明胶的水溶液和
 溶液共同具有的性质是
溶液共同具有的性质是A.都不稳定,密封放置会产生沉淀 B.两者均有丁达尔效应 C.分散质粒子都可通过滤纸
Ⅱ.
 是银白色金属,化学性质稳定,
是银白色金属,化学性质稳定, 价和
价和 价为常见价态。工业上以铬铁矿(主要成分为
价为常见价态。工业上以铬铁矿(主要成分为 ,含
,含
 等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠
等杂质)为主要原料生产金属铬和强氧化剂重铬酸钠 ,其主要工艺流程如下。
,其主要工艺流程如下。
查阅资料:常温下,
 不溶于水,有强氧化性,在碱性条件下,能将
不溶于水,有强氧化性,在碱性条件下,能将 转化为
转化为 。
。(3)工业上常采用热还原法制备金属铬,写出以
 为原料,利用铝热反应制取金属铬的化学方程式:
为原料,利用铝热反应制取金属铬的化学方程式:(4)酸化滤液D时,用硫酸而不用盐酸,可能的原因是
(5)固体E的主要成分是
 ,根据下图分析操作a为
,根据下图分析操作a为
(6)电镀厂产生的镀铜废水中往往含有一定量的
 ,处理该废水常用还原沉淀法,具体流程如下:
,处理该废水常用还原沉淀法,具体流程如下:
①
 的化学性质与
的化学性质与 相似。在上述生产过程中加入
相似。在上述生产过程中加入 溶液时要控制溶液的
溶液时要控制溶液的 不能过高,是因为
不能过高,是因为②下列溶液中可以代替上述流程中
 溶液的是
溶液的是A.浓硫酸 B.酸性
 溶液 C.
溶液 C. 溶液
溶液③上述流程中,每消耗0.1mol
 转移0.8mole-,则加入
转移0.8mole-,则加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为
您最近一年使用:0次
2021-12-04更新
|
87次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2022-2023学年高三上学期第一次月考化学试题
8 . 水体中过量氨氮(以NH3表示)或总氮(溶液中所有可溶性的含氮化合物中氮元素总量)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如下图所示,下列说法正确的是
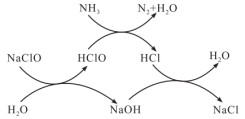

| A.NaClO除去氨氮的总反应化学方程式2NH3+3NaClO=N2+3NaCl+3H2O |
| B.整个过程中发生的反应都是氧化还原反应 |
| C.在较高温度下,氨氮去除率会升高 |
| D.NaClO投入过多,总氮去除率可能会升高 |
您最近一年使用:0次
2021-11-01更新
|
144次组卷
|
2卷引用:宁夏北方民族大学附属中学2022-2023学年高三上学期月考(一)理科综合化学试题
9 . 已知硫酸酸化的K2Cr2O7溶液能与KI反应:aH2SO4+bK2Cr2O7+cKI=mK2SO4+nI2+pCr2(SO4)3+qH2O,下列说法错误的是
| A.a=7 |
| B.K2Cr2O7也可用盐酸酸化 |
| C.每生成1molCr2(SO4)3,转移6mole- |
| D.由上述反应可知,I-的还原性强于Cr3+的还原性 |
您最近一年使用:0次
2021-10-01更新
|
274次组卷
|
4卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
名校
解题方法
10 . 已知某一反应体系反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是
| A.该反应的化学方程式为2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O |
| B.该反应中的氧化剂是H2O2,还原产物是O2 |
| C.氧化性:H2CrO4 > O2 |
| D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L |
您最近一年使用:0次
2020-11-07更新
|
192次组卷
|
9卷引用:宁夏银川一中2021-2022学年高一上学期期末考试化学试题



