1 . 下列说法错误的是
| A.已知电负性:Si<H<Cl,则SiHCl3水解时发生氧化还原反应 |
| B.已知Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,则氧化剂与还原剂物质的量之比为1:2 |
C.已知Na+KCl(熔融) K+NaCl,则可推知钠的还原性和金属性都强于钾 K+NaCl,则可推知钠的还原性和金属性都强于钾 |
| D.已知4KO2+2H2O=4KOH+3O2,则O2为氧化产物 |
您最近一年使用:0次
2024-05-11更新
|
135次组卷
|
2卷引用:天津市耀华中学2024届高三下学期第一次模拟考试化学试卷
名校
解题方法
2 . Ⅰ.如图为铁及其化合物的“价—类”二维图。

(1)填写二维图中缺失的类别①________ 和化学式②___________ 。
(2)从物质类别上看, 属于盐,可能与
属于盐,可能与_______ 发生反应(填序号);
从化合价角度看,体现 氧化性,可能与
氧化性,可能与______ 反应(填序号)。
① ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
Ⅱ.某工厂用 溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
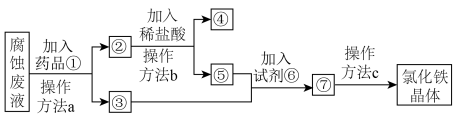
(3)腐蚀废液中加入药品①后,发生反应的离子方程式为___________ 。
(4)④代表的物质是___________ (用化学式表示)。
(5)操作方法a、b、c中是过滤的是________ (填序号)。
(6)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,_________ (补全现象),此过程设计氧化还原反应的方程式为________ 。
(7)工业中常用高铁酸钾( )作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒:
)作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制高铁酸钾的离子反应方程式:
。写出并配平湿法制高铁酸钾的离子反应方程式:___________ 。

(1)填写二维图中缺失的类别①
(2)从物质类别上看,
 属于盐,可能与
属于盐,可能与从化合价角度看,体现
 氧化性,可能与
氧化性,可能与①
 ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液Ⅱ.某工厂用
 溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
(3)腐蚀废液中加入药品①后,发生反应的离子方程式为
(4)④代表的物质是
(5)操作方法a、b、c中是过滤的是
(6)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(7)工业中常用高铁酸钾(
 )作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒:
)作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制高铁酸钾的离子反应方程式:
。写出并配平湿法制高铁酸钾的离子反应方程式:
您最近一年使用:0次
2024-02-12更新
|
120次组卷
|
2卷引用:天津市第四十二中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
3 . 回答下列问题
(1)呼吸面具中的供氧剂与二氧化碳反应的化学方程式_______ ,该反应与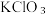 分解反应相比较,产生等分子数的气体,转移电子数目之比为
分解反应相比较,产生等分子数的气体,转移电子数目之比为_______ 。
(2) 溶于水,书写电离方程式
溶于水,书写电离方程式_______ ;检验该溶液中是否含有  ,所需试剂
,所需试剂_______ (填化学式),离子方程式_______ ;除去该溶液中的 杂质,涉及的离子方程式
杂质,涉及的离子方程式_______ ;检验 溶液中是否含有
溶液中是否含有 ,实验操作名称为
,实验操作名称为_______ 。
(3)分别取含等质量溶质的氢氧化钠溶液各 100mL,再分别通入一定量的 ,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
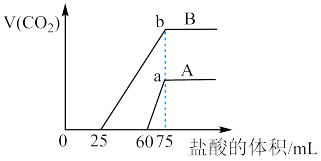
①在A情况下,加入盐酸0-60mL过程中,发生反应的离子方程式依次为_______ 、_______ 。
②图中a、b两点所示的溶液(加入盐酸均为75mL时)溶质分别为_______ 、_______ (生成的 全部逸出),所含溶质的质量大小关系
全部逸出),所含溶质的质量大小关系_______
A. 相等 B. b点质量大 C. a 点质量大
(4) (O为-l价)性质与
(O为-l价)性质与 类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性
类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性 溶液、酸化的KI溶液与
溶液、酸化的KI溶液与 溶液反应验证其性质。(已知:淀粉遇
溶液反应验证其性质。(已知:淀粉遇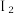 变蓝)
变蓝)

实验①利用了酸性高锰酸钾的_______ 性质,该实验中,证明 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有_______ 。
实验②是为了验证 的
的_______ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式_______ 。
(1)呼吸面具中的供氧剂与二氧化碳反应的化学方程式
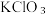 分解反应相比较,产生等分子数的气体,转移电子数目之比为
分解反应相比较,产生等分子数的气体,转移电子数目之比为(2)
 溶于水,书写电离方程式
溶于水,书写电离方程式 ,所需试剂
,所需试剂 杂质,涉及的离子方程式
杂质,涉及的离子方程式 溶液中是否含有
溶液中是否含有 ,实验操作名称为
,实验操作名称为(3)分别取含等质量溶质的氢氧化钠溶液各 100mL,再分别通入一定量的
 ,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
,随后分别各取 20mL 溶液,向其中逐滴滴入稀盐酸,在标准状况下产生(CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B 两种情况):
①在A情况下,加入盐酸0-60mL过程中,发生反应的离子方程式依次为
②图中a、b两点所示的溶液(加入盐酸均为75mL时)溶质分别为
 全部逸出),所含溶质的质量大小关系
全部逸出),所含溶质的质量大小关系A. 相等 B. b点质量大 C. a 点质量大
(4)
 (O为-l价)性质与
(O为-l价)性质与 类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性
类似,既具有氧化性,也具有还原性。某小组同学分别选用酸性 溶液、酸化的KI溶液与
溶液、酸化的KI溶液与 溶液反应验证其性质。(已知:淀粉遇
溶液反应验证其性质。(已知:淀粉遇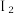 变蓝)
变蓝)
实验①利用了酸性高锰酸钾的
 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有实验②是为了验证
 的
的
您最近一年使用:0次
4 . 氮及其化合物的相互转化对生命、生产生活意义重大。 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化:

(1)写出氮元素在周期表的位置_________ ,写出氯元素的原子结构示意图________ 。
(2)写出 的电子式
的电子式___________ , 的结构式
的结构式___________ 。
(3)下列说法正确的是___________ (填序号)。
a.实验室可用浓氨水和生石灰反应,快速制取少量氨气
b. 分子中所有原子在同一平面上
分子中所有原子在同一平面上
c.用 处理硝酸工业排放的尾气
处理硝酸工业排放的尾气 ,利用了
,利用了 的还原性
的还原性
(4)写出过量 发生转化Ⅰ的化学反应方程式
发生转化Ⅰ的化学反应方程式___________
(5)反应Ⅱ在碱性条件下恰好完全反应,还原产物的阴离子是___________ ,检验该阴离子的方实验方法是___________
(6)反应Ⅲ中 与
与 的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式___________ 。
 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化:
(1)写出氮元素在周期表的位置
(2)写出
 的电子式
的电子式 的结构式
的结构式(3)下列说法正确的是
a.实验室可用浓氨水和生石灰反应,快速制取少量氨气
b.
 分子中所有原子在同一平面上
分子中所有原子在同一平面上c.用
 处理硝酸工业排放的尾气
处理硝酸工业排放的尾气 ,利用了
,利用了 的还原性
的还原性(4)写出过量
 发生转化Ⅰ的化学反应方程式
发生转化Ⅰ的化学反应方程式(5)反应Ⅱ在碱性条件下恰好完全反应,还原产物的阴离子是
(6)反应Ⅲ中
 与
与 的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
您最近一年使用:0次
5 . 近日,科学家开发的常压旋转滑行弧实现高效固氮取得进展,如图所示。
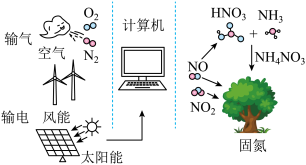
下列叙述错误的是

下列叙述错误的是
| A.该固氮过程均发生氧化还原反应 |
| B.太阳能、风能转化为电能 |
C.图中反应包括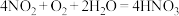 |
D. 和 和 中的N原子的杂化方式不同 中的N原子的杂化方式不同 |
您最近一年使用:0次
2023-04-09更新
|
609次组卷
|
3卷引用:天津市十二区重点学校2023届高三毕业班下学期第二次联考化学试题
天津市十二区重点学校2023届高三毕业班下学期第二次联考化学试题山东省聊城市部分学校2022-2023学年高三下学期第三次学业质量联合检测化学试题(已下线)化学-2023年高考押题预测卷02(江苏卷)(含考试版、全解全析、参考答案、答题卡)
6 . 为探究Na2SO3的性质,实验小组同学进行了如下实验:

| A.③和④中产生的气体成分完全相同 | B.②和⑥中沉淀的主要成分不同 |
| C.①→②和④→⑥均只发生了复分解反应 | D. 的还原性在酸性条件下增强 的还原性在酸性条件下增强 |
您最近一年使用:0次
2023-04-06更新
|
2564次组卷
|
11卷引用:天津市滨海新区2023-2024学年塘沽第一中学高三上学期第二次月考化学试题
天津市滨海新区2023-2024学年塘沽第一中学高三上学期第二次月考化学试题北京市海淀区2022-2023学年高三下学期期中练习化学试题山东省东营市第一中学2023届高三下学期二模化学试题浙江省杭州第四中学2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭四下沙】【高中化学】【罗梦宇收集】(已下线)题型35 微型成套装置实验流程(已下线)题型45 物质性质探究型综合实验山西省晋城一中2022-2023学年高一下学期第三次调研考试化学试题(已下线)热点19 化学微型实验北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷 北京市顺义区第二中学2023-2024学年高三下学期开学测化学试题
名校
7 . 非金属元素Si、N、S的单质及其化合物在生产生活中起到重要的作用。
I.氮化硅是一种高温陶瓷材料,它硬度大、熔点高,化学性质稳定,工业上普遍采用高纯硅与纯氮在1300℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是___________。(填序号)
II.
(2)为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置(尾气处理装置省略):

上述三套装置中,仅通过观察不能探究出“铜与浓硝酸反应是吸热反应还是放热反应”的是___________ (填“I”“II”或“III”)。
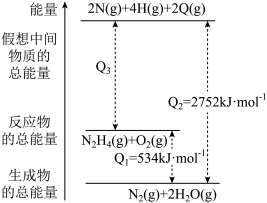
(3)已知化学反应 的能量变化如图所示,回答下列问题:
的能量变化如图所示,回答下列问题:
① 和
和 生成
生成 原子、
原子、 原子、
原子、 原子的过程中
原子的过程中___________ (填“吸收”或“放出”)___________  能量。
能量。
② 和
和 生成
生成 和
和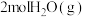 的反应中
的反应中___________ (填“吸收”或“放出”)___________  能量。
能量。
(4)下列性质的比较中,不能说明N的非金属性强于P的是___________ (填序号)。
A.熔沸点: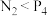 (白磷) B.稳定性:
(白磷) B.稳定性: C.酸性:
C.酸性:
III.
(5)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理: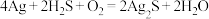 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。
(6)酸雨中的亚硫酸易被氧化,如:能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:___________ 。
I.氮化硅是一种高温陶瓷材料,它硬度大、熔点高,化学性质稳定,工业上普遍采用高纯硅与纯氮在1300℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是___________。(填序号)
| A.制汽轮机 | B.制有色玻璃 | C.制永久性模具 | D.制造柴油机 |
II.
(2)为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置(尾气处理装置省略):

上述三套装置中,仅通过观察不能探究出“铜与浓硝酸反应是吸热反应还是放热反应”的是
(3)已知化学反应
 的能量变化如图所示,回答下列问题:
的能量变化如图所示,回答下列问题:①
 和
和 生成
生成 原子、
原子、 原子、
原子、 原子的过程中
原子的过程中 能量。
能量。②
 和
和 生成
生成 和
和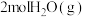 的反应中
的反应中 能量。
能量。
(4)下列性质的比较中,不能说明N的非金属性强于P的是
A.熔沸点:
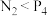 (白磷) B.稳定性:
(白磷) B.稳定性: C.酸性:
C.酸性:
III.
(5)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:
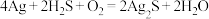 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:
您最近一年使用:0次
解题方法
8 . 联氨(N2H4)可用于处理水中的溶解氧,其反应机理如下图所示:
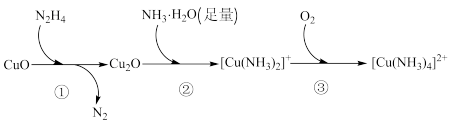
下列说法不正确 的是

下列说法
A. 分子的共价键只有 分子的共价键只有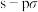 键 键 |
B. 具有还原性,在一定条件下可被 具有还原性,在一定条件下可被 氧化 氧化 |
C.②中反应产物是 而不是 而不是 ,说明 ,说明 相对较稳定 相对较稳定 |
D.③中发生反应: |
您最近一年使用:0次
2022-12-29更新
|
454次组卷
|
4卷引用:天津市南开区2022-2023学年高三下学期质量检测(一)化学试题
天津市南开区2022-2023学年高三下学期质量检测(一)化学试题北京市大兴区2022-2023学年高三上学期期末考试化学试题(已下线)专题12 化学反应机理(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)化学-2023年高考押题预测卷03(辽宁卷)(含考试版、全解全析、参考答案、答题卡)
解题方法
9 . 很多消毒剂都是利用其强氧化性进行消毒杀菌,如常见的“84”消毒液(有效成分是NaClO)、双氧水、二氧化氯、高铁酸钠等。回答下列问题。
(1)NaClO的电子式为____ 。某“84”消毒液的密度为1.49g•cm-3,NaClO的质量分数为10%;则c(NaClO)=____ 。“84”消毒液在存放过程中会变质,向淀粉碘化钾试纸上滴加1~2滴“84”消毒液,若试纸____ ,则说明“84”消毒液没有完全变质。
(2)双氧水有绿色消毒剂之称,这是因为____ 。“84”消毒液与双氧水混合会产生一种常见的无色无味气体,且消毒能力会严重降低,写出该反应的离子方程式____ 。
(3)二氧化氯(ClO2)是一种高效、低毒的消毒剂,其在消毒杀菌过程中会产生ClO ,需将其转化为Cl-除去,下列试剂可将ClO2转化为Cl-的是
,需将其转化为Cl-除去,下列试剂可将ClO2转化为Cl-的是____ (填标号)。
(4)高铁酸钠(Na2FeO4)不仅可以消毒,还可以净水,净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH,该反应中被氧化的元素是____ 。证明有胶体生成的简单方法是____ 。
(1)NaClO的电子式为
(2)双氧水有绿色消毒剂之称,这是因为
(3)二氧化氯(ClO2)是一种高效、低毒的消毒剂,其在消毒杀菌过程中会产生ClO
 ,需将其转化为Cl-除去,下列试剂可将ClO2转化为Cl-的是
,需将其转化为Cl-除去,下列试剂可将ClO2转化为Cl-的是| A.Cl2 | B.Na2CO3 | C.KMnO4 | D.FeSO4 |
您最近一年使用:0次
10 . 下列说法中,正确的是
A. 、 、 、 、 都是酸性氧化物,CaO、 都是酸性氧化物,CaO、 都是碱性氧化物 都是碱性氧化物 |
B.氧化镁与稀盐酸混合反应的离子方程式为: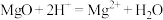 |
C.关于反应 中, 中, 是还原剂 是还原剂 |
D.盐酸、NaOH溶液、 溶液都能导电,它们都是电解质 溶液都能导电,它们都是电解质 |
您最近一年使用:0次



