1 . 某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用 酸化的
酸化的 的
的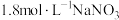 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的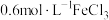 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的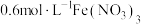 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含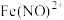 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是
 酸化的
酸化的 的
的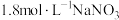 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的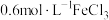 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的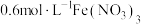 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含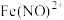 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是A.①说明 的 的 溶液不与铜粉反应 溶液不与铜粉反应 |
B.②证明氧化性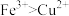 还原性 还原性 |
C.③中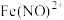 的生成速率一定小于 的生成速率一定小于 被还原的速率 被还原的速率 |
| D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色 |
您最近一年使用:0次
2 . 下列类比或推理结果正确的是
A.已知 和浓硫酸可发生归中反应,则 和浓硫酸可发生归中反应,则 和硝酸也可发生归中反应 和硝酸也可发生归中反应 |
B.已知加热时Cu与 反应生成 反应生成 ,则加热时Cu与S反应生成 ,则加热时Cu与S反应生成 |
C.已知C、Si形成的氧化物晶体类型不同,可推知等物质的量的 和 和 中σ键数目不相同 中σ键数目不相同 |
D.已知氧化性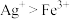 ,根据溶液中 ,根据溶液中 和 和 易发生氧化还原反应,推断溶液中 易发生氧化还原反应,推断溶液中 和 和 也易发生氧化还原反应 也易发生氧化还原反应 |
您最近一年使用:0次
名校
解题方法
3 . 我国某研究团队利用电解法处理富营养化河水的机理如图,下列说法正确的是
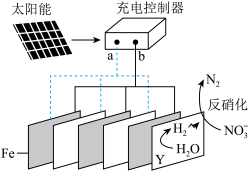

A. 极为电子流出极, 极为电子流出极, 极为电子流入极 极为电子流入极 |
B. 极发生的反应为 极发生的反应为 |
C.一段时间后,该河水的 增大 增大 |
D.反硝化过程中,还原剂与还原产物的物质的量之比为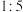 |
您最近一年使用:0次
解题方法
4 . N-羧基丙氨酸酸酐广泛用于生物领域,用碳酸二甲酯 和丙氨酸
和丙氨酸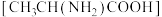 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
 和丙氨酸
和丙氨酸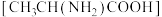 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
| A.在强酸性环境不利于反应进行 |
B.该过程中 元素的化合价发生改变 元素的化合价发生改变 |
C.反应过程中有 的断裂和形成 的断裂和形成 |
D.用甘氨酸 代替丙氨酸,可制得 代替丙氨酸,可制得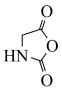 |
您最近一年使用:0次
2024-04-01更新
|
349次组卷
|
4卷引用:2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题
2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
名校
解题方法
5 . 从宏观现象探究微观本质是重要的化学学科素养。为研究FeCl3溶液的性质,某小组同学进行了如下探究实验。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是______ 。
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为______ 。
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为______ (填化学式)。两位同学实验如下:
(4)两位同学猜测实验a中的黑色沉淀可能是Fe2S3。继续实验:
根据实验b说明黑色沉淀是Fe2S3,写出实验b中Fe2S3与盐酸反应的化学方程式:______ 。
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为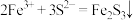 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于______ 。
②实验a中Fe2S3溶解时生成的黄色固体为______ ,乙同学推测是因为随着FeCl3溶液滴加至一定量, 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。
(6)已知: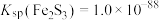 ,
,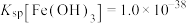 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:______ 。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为
| 实验a | 向稀Na2S溶液中逐滴加入FeCl3稀溶液,直至过量 |
| 实验现象 | 立即产生黑色沉淀并逐渐增加,无臭鸡蛋气味;FeCl3溶液过量后,黑色沉淀部分溶解,出现黄色沉淀 |
| 实验b | 将实验a中黑色沉淀过滤,并用CS2处理后洗净。向沉淀中加入6mol/L的盐酸,振荡试管 |
| 实验现象 | 加入盐酸后黑色沉淀溶解,转为乳黄色沉淀,并伴有臭鸡蛋气味 |
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为
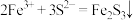 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于②实验a中Fe2S3溶解时生成的黄色固体为
 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。(6)已知:
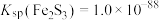 ,
,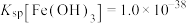 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
您最近一年使用:0次
6 . 已知转化Ⅰ: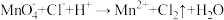 ;转化Ⅱ:
;转化Ⅱ: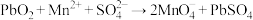 。下列说法错误的是
。下列说法错误的是
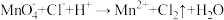 ;转化Ⅱ:
;转化Ⅱ: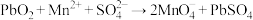 。下列说法错误的是
。下列说法错误的是A.氧化性:PbO2> >Cl2 >Cl2 |
B.转化Ⅰ、Ⅱ消耗或生成等物质的量的 ,转移电子数相同 ,转移电子数相同 |
C. 做氧化剂时,酸性越强,氧化性越强 做氧化剂时,酸性越强,氧化性越强 |
D.PbO2与FeSO4溶液反应: |
您最近一年使用:0次
2024-04-10更新
|
202次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷
7 . 氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)过氧化钠可用作潜水艇和消防员呼吸面具中的供氧剂,其主要原理为: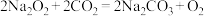 。其中Na2O2的阴、阳离子个数比为
。其中Na2O2的阴、阳离子个数比为________ 。每消耗2个CO2分子,转移电子的数目为________ 个。在下列选项中选择,上述反应中Na2O2是________ (填字母,下同),O2是________ .
A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
若要反应产生64.0gO2,同时消耗Na2O2的质量约为________ g。
(2)汽车尾气系统中均安装了催化转化器。汽车尾气中有毒的CO和NO在催化剂高温条件下发生反应,生成两种无毒气体。上述反应的化学方程式为: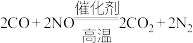 用单线桥标出反应中电子转移的方向和数目
用单线桥标出反应中电子转移的方向和数目________ 。
该反应中,氧化产物与还原产物的分子数之比为________ 。
(3)亚硝酸钠NaNO2像食盐一样有咸味,毒性很强,误食会导致血红蛋白中的Fe2+转化为Fe3+,可服用维生素C解毒。关于该过程的叙述,不正确的是________(填字母)。
(1)过氧化钠可用作潜水艇和消防员呼吸面具中的供氧剂,其主要原理为:
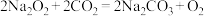 。其中Na2O2的阴、阳离子个数比为
。其中Na2O2的阴、阳离子个数比为A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
若要反应产生64.0gO2,同时消耗Na2O2的质量约为
(2)汽车尾气系统中均安装了催化转化器。汽车尾气中有毒的CO和NO在催化剂高温条件下发生反应,生成两种无毒气体。上述反应的化学方程式为:
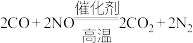 用单线桥标出反应中电子转移的方向和数目
用单线桥标出反应中电子转移的方向和数目该反应中,氧化产物与还原产物的分子数之比为
(3)亚硝酸钠NaNO2像食盐一样有咸味,毒性很强,误食会导致血红蛋白中的Fe2+转化为Fe3+,可服用维生素C解毒。关于该过程的叙述,不正确的是________(填字母)。
| A.亚硝酸钠的氧化性强于Fe3+ | B.维生素C是还原剂 |
| C.维生素C的还原性强于Fe2+ | D.亚硝酸钠是还原剂 |
您最近一年使用:0次
8 . 为增强铝合金的耐磨性与耐腐蚀性,常采用铬酸氧化法钝化铝合金表面。铬酸洗液(主要成分为重铬酸H2Cr2O7)与铝合金接触后发生如下反应 (反应未配平)。下列关于此反应的叙述不正确的是
(反应未配平)。下列关于此反应的叙述不正确的是
 (反应未配平)。下列关于此反应的叙述不正确的是
(反应未配平)。下列关于此反应的叙述不正确的是| A.钝化膜中的铬以+6价形式存在 | B.反应物中的铬元素只有 被还原 被还原 |
C.每消耗 转移6 mol电子 转移6 mol电子 | D.反应发生后铬酸洗液酸性减弱 |
您最近一年使用:0次
2023-12-23更新
|
64次组卷
|
2卷引用:湖南省长沙市名校联合体2023-2024学年高一上学期第二次联考化学试题
名校
9 . 一种含碘废水(I2和I-)制取单质碘的工艺流程如图:

下列有关分析错误的是

下列有关分析错误的是
| A.通入SO2的目的是将I2和Cu2+还原 |
| B.利用磁石可以将滤渣Ⅰ进一步分离 |
| C.滤渣Ⅱ放在潮湿的空气中能被氧化为红褐色物质 |
| D.操作X是萃取、分液 |
您最近一年使用:0次
2023-11-07更新
|
156次组卷
|
2卷引用:湖南省常德市第一中学2024届高三上学期第四次月考化学试题
名校
解题方法
10 . 某小组在验证反应“ ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。
向硝酸酸化的 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
(1)检测到滤液中含有 ,可以选用的试剂为
,可以选用的试剂为___________ (填化学式)溶液。 产生的原因可能有以下几种。
产生的原因可能有以下几种。
假设a:可能是铁粉表面有氧化层,能产生 。
。
假设b:空气中存在 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
假设c:酸性溶液中的 具有氧化性,可产生
具有氧化性,可产生 。
。
(2)某同学证明上面假设c不成立,向硝酸酸化的___________ 硝酸钠溶液中加入过量铁粉,搅拌后静置,一段时间后,上层清液未变黄色,经检验无 。
。
(3)取过滤后的黑色固体,洗涤后,___________ (填操作和现象),证明黑色固体中含有Ag。
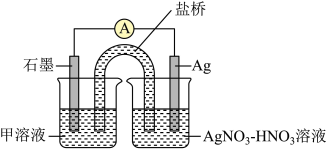
(4)某同学利用原电池证明 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为___________ 。写出石墨电极上发生的电极反应式:___________ 。电流表指针不再偏转后,向左侧烧杯中加入 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为___________ (填“正极”或“负极”),银电极的电极反应式为___________ 。
 ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。向硝酸酸化的
 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。(1)检测到滤液中含有
 ,可以选用的试剂为
,可以选用的试剂为 产生的原因可能有以下几种。
产生的原因可能有以下几种。假设a:可能是铁粉表面有氧化层,能产生
 。
。假设b:空气中存在
 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:假设c:酸性溶液中的
 具有氧化性,可产生
具有氧化性,可产生 。
。(2)某同学证明上面假设c不成立,向硝酸酸化的
 。
。(3)取过滤后的黑色固体,洗涤后,
(4)某同学利用原电池证明
 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为
您最近一年使用:0次
2023-10-26更新
|
610次组卷
|
7卷引用:湖南省娄底市新化县2023-2024学年高二上学期期末考试化学试题



