名校
1 . 二氧化铈( )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示:
(1)“焙烧”时,通入空气的主要目的是_________________ 。
(2)滤渣的主要成分是___________________ (填化学式)。
(3)“还原、脱氟”时,先加入硫脲(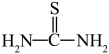 ),目的是将溶液中的
),目的是将溶液中的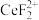 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_________________ [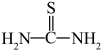 被氧化为
被氧化为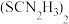 ,生成物还有HF和
,生成物还有HF和 ]。
]。
(4)“沉铈”时反应的离子方程式为__________________ 。若用 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是________________ 。
(5)若常温下,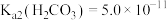 ,
,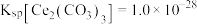 ,
, 恰好沉淀完全
恰好沉淀完全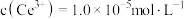 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中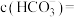
_____________  。
。
(6)二氧化铈作为一种SCR脱硝催化剂,能在 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物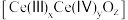 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为____________ 。
 )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示: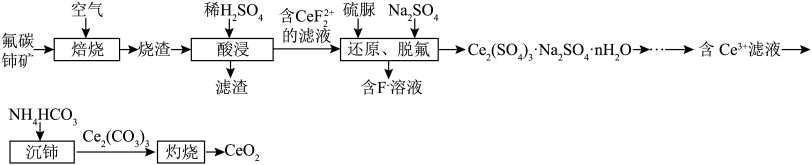
(1)“焙烧”时,通入空气的主要目的是
(2)滤渣的主要成分是
(3)“还原、脱氟”时,先加入硫脲(
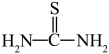 ),目的是将溶液中的
),目的是将溶液中的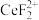 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: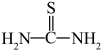 被氧化为
被氧化为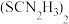 ,生成物还有HF和
,生成物还有HF和 ]。
]。(4)“沉铈”时反应的离子方程式为
 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是(5)若常温下,
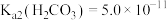 ,
,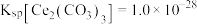 ,
, 恰好沉淀完全
恰好沉淀完全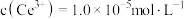 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中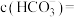
 。
。(6)二氧化铈作为一种SCR脱硝催化剂,能在
 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物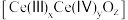 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为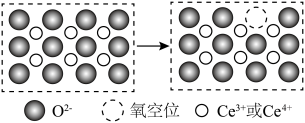
您最近一年使用:0次
7日内更新
|
98次组卷
|
3卷引用:江苏省部分学校2024届高三下学期全真模拟测化学试卷
2 . 锂电池的研发、使用及废电池的回收具有重要意义。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为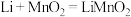 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是___________ (填序号)。
A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀 作电解质
作电解质
(2)钴酸锂( )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。
①钴酸锂电池放电时示意图如图1所示。放电时, 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式:___________ 。 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=___________ 。 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。___________ 。
②与 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:___________ 。
(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用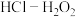 混合物作浸取剂。
混合物作浸取剂。
①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:___________ 。
②工业生产时在盐酸中加入 ,
, 的作用是
的作用是___________ 。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为
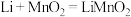 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀
 作电解质
作电解质(2)钴酸锂(
 )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。①钴酸锂电池放电时示意图如图1所示。放电时,
 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式: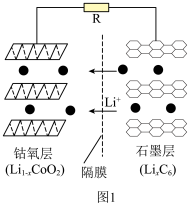
 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=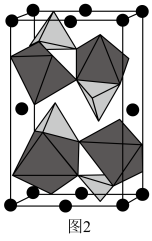
 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。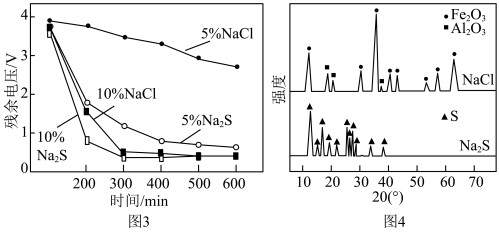
②与
 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为
 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用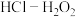 混合物作浸取剂。
混合物作浸取剂。①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:
②工业生产时在盐酸中加入
 ,
, 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
3 . 以下是一系列非金属元素间的置换反应,其中不能说明反应前的非金属单质的氧化性强于产物中非金属单质的氧化性的是
A. | B.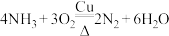 |
C. | D. |
您最近一年使用:0次
4 . “价类”二维图体现了元素的分类观、转化观,下图是 元素及其化合物的“价类”二维图。下列说法正确的是
元素及其化合物的“价类”二维图。下列说法正确的是
 元素及其化合物的“价类”二维图。下列说法正确的是
元素及其化合物的“价类”二维图。下列说法正确的是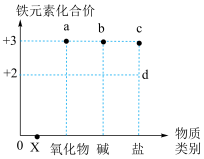
| A.a到b可以一步实现 | B.实验室保存d的溶液可以加入少量铜粉 |
| C.b为红褐色固体 | D.d转化为c需要加入还原剂 |
您最近一年使用:0次
5 .  是一种新型多功能绿色消毒剂。
是一种新型多功能绿色消毒剂。
I.某兴趣小组利用废铁屑(含少量 )制备高铁酸钠的工艺流程如图所示:
)制备高铁酸钠的工艺流程如图所示: ;
; ;
;_______ 。
(2)“操作”中通入空气的目的是_______ 。
(3)“氧化”时发生反应的化学方程式为_______ 。
(4)称取一定质量碘化钾于碘量瓶中,加入 溶液和一定质量氟化钠固体,待溶解完毕;准确称取
溶液和一定质量氟化钠固体,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用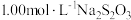 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为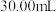 。已知
。已知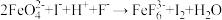 (未配平);
(未配平); 计算样品中
计算样品中 的质量分数
的质量分数_____ (写出计算过程)。
II. 主要用于废水处理。
主要用于废水处理。
(5) 净水原理如图所示。
净水原理如图所示。 是一种多功能水处理剂的原因为
是一种多功能水处理剂的原因为_______ 。 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。
① 时,
时,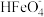 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为_______ 。
②酸性溶液中 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是_______ 。
 是一种新型多功能绿色消毒剂。
是一种新型多功能绿色消毒剂。I.某兴趣小组利用废铁屑(含少量
 )制备高铁酸钠的工艺流程如图所示:
)制备高铁酸钠的工艺流程如图所示:
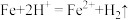 ;
; ;
;(2)“操作”中通入空气的目的是
(3)“氧化”时发生反应的化学方程式为
(4)称取一定质量碘化钾于碘量瓶中,加入
 溶液和一定质量氟化钠固体,待溶解完毕;准确称取
溶液和一定质量氟化钠固体,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用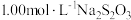 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为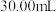 。已知
。已知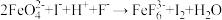 (未配平);
(未配平); 计算样品中
计算样品中 的质量分数
的质量分数II.
 主要用于废水处理。
主要用于废水处理。(5)
 净水原理如图所示。
净水原理如图所示。 是一种多功能水处理剂的原因为
是一种多功能水处理剂的原因为
 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。①
 时,
时,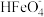 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为②酸性溶液中
 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是
您最近一年使用:0次
名校
解题方法
6 . 土壤中的 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法不正确 的是
 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法A. 被氧化为 被氧化为 的过程中, 的过程中, 与 与 的物质的量之比为 的物质的量之比为 |
B.在反硝化过程中,土壤 降低 降低 |
C. 与 与 反应时,每生成 反应时,每生成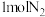 ,转移电子数为 ,转移电子数为 |
| D.适当疏松土壤,有利于提高铵态氮肥的肥效 |
您最近一年使用:0次
名校
7 . 硫及其化合物种类繁多,在生产生活中应用广泛。下图是硫及其部分化合物的“价类二维图”。

(1)硫元素在元素周期表中的位置是_______ 。
(2)从氧化还原的角度分析,欲制备硫代硫酸钠( ),下列方案合理的是
),下列方案合理的是____ (填序号)。
① 和
和 ②
② 和浓
和浓 ③
③ 和
和 ④
④ 和
和
(3)硫代硫酸钠( )常用作纸浆漂白的脱氯剂,实验室可用下图装置制备少量
)常用作纸浆漂白的脱氯剂,实验室可用下图装置制备少量 。
。
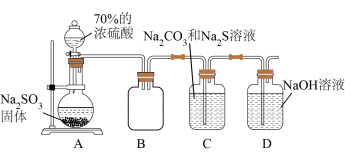
①实验室制备少量: 气体也可以用浓硫酸与
气体也可以用浓硫酸与 反应,该反应的化学方程式是
反应,该反应的化学方程式是_________ 。
②装置B的作用是________ 。装置C中发生反应生成 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是________ 。
③装置D的作用是______ 。若装置D中是足量氨水,则与 反应的离子方程式是
反应的离子方程式是_____ 。

(1)硫元素在元素周期表中的位置是
(2)从氧化还原的角度分析,欲制备硫代硫酸钠(
 ),下列方案合理的是
),下列方案合理的是①
 和
和 ②
② 和浓
和浓 ③
③ 和
和 ④
④ 和
和
(3)硫代硫酸钠(
 )常用作纸浆漂白的脱氯剂,实验室可用下图装置制备少量
)常用作纸浆漂白的脱氯剂,实验室可用下图装置制备少量 。
。
①实验室制备少量:
 气体也可以用浓硫酸与
气体也可以用浓硫酸与 反应,该反应的化学方程式是
反应,该反应的化学方程式是②装置B的作用是
 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是③装置D的作用是
 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
解题方法
8 . 生活中常用的消毒剂有含氯消毒剂、双氧水等。
Ⅰ.实验室模拟获得少量漂白粉的装置如图

(1)实验室可以用 和浓盐酸反应制取氮气,反应方程式如下:
和浓盐酸反应制取氮气,反应方程式如下:
①浓盐酸在反应中显示出来的性质是___________ ;
②请用双线桥表示该反应电子转移的方向和数目:___________
 ;
;
③D装置的作用是___________ 。
(2)已知:a.氯气和石灰乳在反应的过程中会放出热量。
b.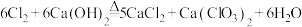
①写出制取漂白粉的化学方程式:___________ 。
②兴趣小组制得的漂白粉中 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低,主要原因可能是
含量明显偏低,主要原因可能是___________ 。
Ⅱ.亚氯酸钠( )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
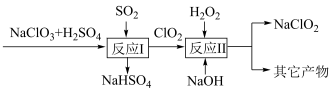
(3)①反应Ⅰ的氧化剂是___________ (写化学式,下同)。
②反应Ⅱ中其它产物除了 外还有
外还有___________ ,当 和
和 的物质的量为
的物质的量为 混合时完全反应,则反应Ⅱ的化学方程式为
混合时完全反应,则反应Ⅱ的化学方程式为___________ 。
Ⅰ.实验室模拟获得少量漂白粉的装置如图

(1)实验室可以用
 和浓盐酸反应制取氮气,反应方程式如下:
和浓盐酸反应制取氮气,反应方程式如下:
①浓盐酸在反应中显示出来的性质是
②请用双线桥表示该反应电子转移的方向和数目:
 ;
;③D装置的作用是
(2)已知:a.氯气和石灰乳在反应的过程中会放出热量。
b.
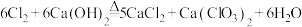
①写出制取漂白粉的化学方程式:
②兴趣小组制得的漂白粉中
 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低,主要原因可能是
含量明显偏低,主要原因可能是Ⅱ.亚氯酸钠(
 )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
(3)①反应Ⅰ的氧化剂是
②反应Ⅱ中其它产物除了
 外还有
外还有 和
和 的物质的量为
的物质的量为 混合时完全反应,则反应Ⅱ的化学方程式为
混合时完全反应,则反应Ⅱ的化学方程式为
您最近一年使用:0次
9 . 甲烷是一种能量密度低、难液化、运输成本较高的能源。将甲烷转化成能量密度较高的液体燃料已成为重要的课题。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1: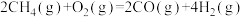

反应2: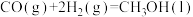
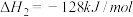
写出甲烷氧化法制甲醇的热化学方程式:______ 。
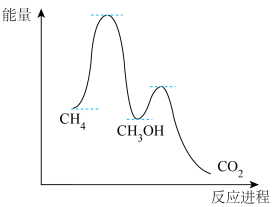
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是______ 。
Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为______ 。

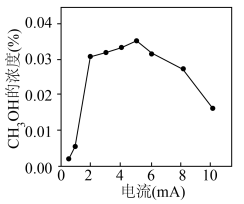
(4)钒(V)物种被认为是形成活性氧物质(如 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是______ 。
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
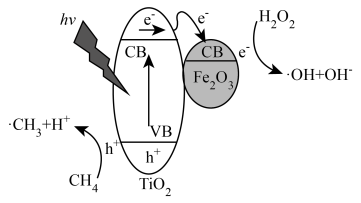
(5)光照时,表面形成的空穴(h+)具有强______ (填“氧化性”或“还原性”)。
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式______ 。
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是______ 。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1:
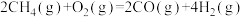

反应2:
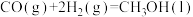
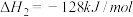
写出甲烷氧化法制甲醇的热化学方程式:
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是

Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为

(4)钒(V)物种被认为是形成活性氧物质(如
 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性
 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
(5)光照时,表面形成的空穴(h+)具有强
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是
您最近一年使用:0次
名校
10 . 工业废气中的 的脱除是目前学术界研究的热点。
的脱除是目前学术界研究的热点。
I.某研究小组用新型 催化剂对
催化剂对 、
、 催化转化进行研究,测得一段时间内
催化转化进行研究,测得一段时间内 的转化率、
的转化率、 剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
反应I: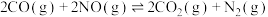

反应Ⅱ:


○:无CO且无催化剂时 直接分解成
直接分解成 的转化率
的转化率
△: 时,
时, 转化为
转化为 的转化率
的转化率
□: 时,
时, 的剩余百分率
的剩余百分率
(1)无 且无催化剂时,在
且无催化剂时,在 以上,随着温度的升高,
以上,随着温度的升高, 的转化率不断降低,其可能原因是
的转化率不断降低,其可能原因是___________ 。
(2) 时,该催化剂脱除
时,该催化剂脱除 的最适宜温度在
的最适宜温度在___________ ℃左右。
(3) ,初始
,初始 ,且不考虑除反应
,且不考虑除反应 、反应Ⅱ之外的反应时,反应相同时间后体系内
、反应Ⅱ之外的反应时,反应相同时间后体系内
___________ 。
(4) 条件下,温度高于
条件下,温度高于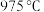 时,随着温度的升高,
时,随着温度的升高, 的转化率迅速降低,其可能原因是
的转化率迅速降低,其可能原因是___________ 。
Ⅱ.在 催化剂中,起催化作用的
催化剂中,起催化作用的 被负载于纳米
被负载于纳米 颗粒上。将含有
颗粒上。将含有 的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:

(5)根据上图所示反应过程,请推断过程I中 的化合价如何变化
的化合价如何变化 :反应前
:反应前___________ 价,反应后___________ 价。
(6)请写出NO被催化还原的总反应方程式___________ 。
 的脱除是目前学术界研究的热点。
的脱除是目前学术界研究的热点。I.某研究小组用新型
 催化剂对
催化剂对 、
、 催化转化进行研究,测得一段时间内
催化转化进行研究,测得一段时间内 的转化率、
的转化率、 剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:
剩余的百分率随温度变化情况如下图所示。已知NO可发生下列反应:反应I:
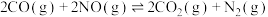

反应Ⅱ:



○:无CO且无催化剂时
 直接分解成
直接分解成 的转化率
的转化率△:
 时,
时, 转化为
转化为 的转化率
的转化率□:
 时,
时, 的剩余百分率
的剩余百分率(1)无
 且无催化剂时,在
且无催化剂时,在 以上,随着温度的升高,
以上,随着温度的升高, 的转化率不断降低,其可能原因是
的转化率不断降低,其可能原因是(2)
 时,该催化剂脱除
时,该催化剂脱除 的最适宜温度在
的最适宜温度在(3)
 ,初始
,初始 ,且不考虑除反应
,且不考虑除反应 、反应Ⅱ之外的反应时,反应相同时间后体系内
、反应Ⅱ之外的反应时,反应相同时间后体系内
(4)
 条件下,温度高于
条件下,温度高于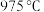 时,随着温度的升高,
时,随着温度的升高, 的转化率迅速降低,其可能原因是
的转化率迅速降低,其可能原因是Ⅱ.在
 催化剂中,起催化作用的
催化剂中,起催化作用的 被负载于纳米
被负载于纳米 颗粒上。将含有
颗粒上。将含有 的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
的尾气与空气、氨气按一定比例通入已知催化体系中,已知反应过程如下图所示:
(5)根据上图所示反应过程,请推断过程I中
 的化合价如何变化
的化合价如何变化 :反应前
:反应前(6)请写出NO被催化还原的总反应方程式
您最近一年使用:0次



