名校
1 . 资料显示银镜用稀硝酸或 溶液清洗均可,某研究小组探究如下。
溶液清洗均可,某研究小组探究如下。
实验所用试剂: 溶液,
溶液, 溶液(向
溶液(向 溶液中加入
溶液中加入 至饱和),饱和碘水,
至饱和),饱和碘水,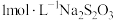 溶液。已知:
溶液。已知: 在水溶液中无色。下列说法错误的是
在水溶液中无色。下列说法错误的是
 溶液清洗均可,某研究小组探究如下。
溶液清洗均可,某研究小组探究如下。实验所用试剂:
 溶液,
溶液, 溶液(向
溶液(向 溶液中加入
溶液中加入 至饱和),饱和碘水,
至饱和),饱和碘水,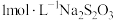 溶液。已知:
溶液。已知: 在水溶液中无色。下列说法错误的是
在水溶液中无色。下列说法错误的是
A.黄色固体为 |
B.①②实验银镜溶解速度对比说明发生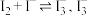 氧化性与 氧化性与 相近但溶解性更好 相近但溶解性更好 |
| C.由实验可知任一氧化剂和碘化钾的混合环境均可溶解银镜 |
D.可向①中试管底部黄色固体加入 溶液验证银镜是否溶解完全,相应的离子方程式为: 溶液验证银镜是否溶解完全,相应的离子方程式为: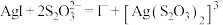 |
您最近一年使用:0次
解题方法
2 . 近日,清华大学某课题组报道了一种在碳纳米管上负载金属钴酞菁的分子催化剂(CoPc/CNT),实现了一步电化学乙烯( )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示:
 )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示: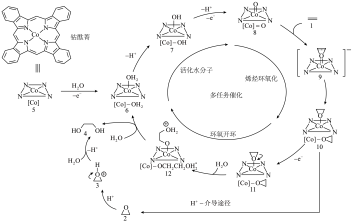
已知: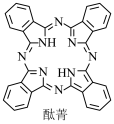 为平面形分子。
为平面形分子。
A.酞菁分子中氮原子的杂化类型为 、 、 |
| B.步骤“5→6”中钴元素被还原 |
| C.上述反应过程中没有极性键的形成 |
D.步骤“2→3→4”的总反应为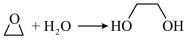 |
您最近一年使用:0次
解题方法
3 . 一种催化还原NO的机理如图所示,下列说法正确的是
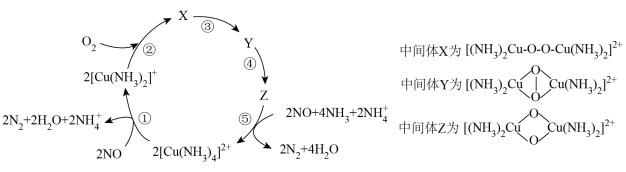

| A.中间体X和Z中O和Cu的化合价均不变 |
B.使用催化剂 ,可以提高NO的反应速率和平衡转化率 ,可以提高NO的反应速率和平衡转化率 |
| C.过程①中既有极性键的断裂,也有极性键的形成 |
D.该催化还原过程的总反应方程式为 |
您最近一年使用:0次
2024-05-14更新
|
59次组卷
|
2卷引用:2024届新疆维吾尔自治区高三下学期三模考试理综试题-高中化学
4 . 稍过量零价铁与亚硫酸钠体系能有效降解废水中有机污染物活性红。
已知:
ⅰ.体系中产生的 、
、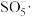 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性
ⅱ.

ⅲ. 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3
 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系
下列说法不正确 的是
已知:
ⅰ.体系中产生的
 、
、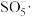 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性ⅱ.


ⅲ.
 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8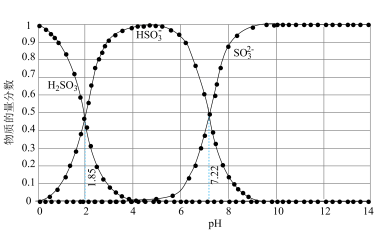
 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系 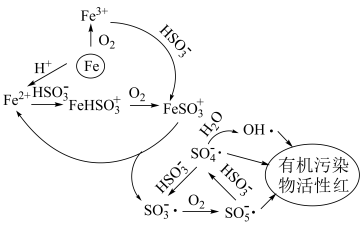
下列说法
A.由图1,25℃时 的 的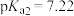 |
| B.pH=4时较pH=8时具有更好的降解效果 |
C.反应一段时间后零价铁表面产生 ,投入 ,投入 可消除 可消除 |
| D.用等物质的量的硫酸亚铁代替零价铁可提高有机物的降解率 |
您最近一年使用:0次
名校
5 . 下列离子方程式不能用来解释相应实验现象的是
| 选项 | 实验现象 | 离子方程式 |
| A | Pb放入 溶液中,产生沉淀 溶液中,产生沉淀 | 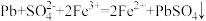 |
| B | 向氨水中滴入氯化铝溶液 | 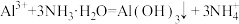 |
| C | 向稀硝酸中滴加 溶液产生气体 溶液产生气体 | 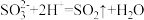 |
| D | 酸性高锰酸钾溶液中滴入双氧水后,溶液褪色 | 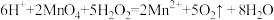 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列反应的离子方程式书写正确的是
A.向 溶液中滴加稀 溶液中滴加稀 : :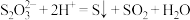 |
B.将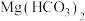 溶液长时间煮沸时形成水垢: 溶液长时间煮沸时形成水垢: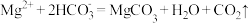 |
C.铅酸蓄电池充电时的阴极反应: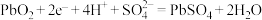 |
D.向含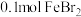 的溶液中通入 的溶液中通入 |
您最近一年使用:0次
7 . NH4NO3受撞击时会发生爆炸: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 溶液中含 溶液中含 数目为 数目为 |
B.1molN2中含 键数目为 键数目为 |
C.标准状况下,22.4LH2O中含电子数为 |
D.每生成0.2molNO2,该反应中转移电子数为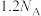 |
您最近一年使用:0次
名校
8 . 红树林沉积物中微生物驱动的硫循环过程原理如图所示,下列叙述错误的是
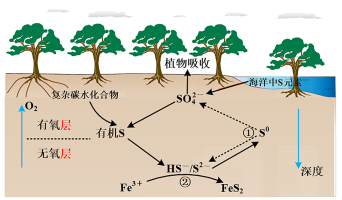
A.海洋中疏元素主要以 形式存在 形式存在 |
B.依据价态及图示分析,在无氧层, 是重要的氧化剂 是重要的氧化剂 |
| C.硫循环与金属元素的耦合可以有效固定沉积物中的重金属元素 |
| D.反应①与反应②过程中硫元素均被氧化 |
您最近一年使用:0次
9 . 废钼催化剂中钼、钴、镍等有价金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如图:
等)中回收有价金属的工艺流程如图:
(1)基态Mo原子的价层电子排布式为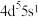 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为___________ 。
(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,这样做的优点是___________ ;“焙烧”时生成的气体A的主要成分为___________ 。 转化为
转化为 ,写出“碱浸”时
,写出“碱浸”时 参与反应的离子方程式:
参与反应的离子方程式:___________ 。
(4)已知 和
和 不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是
不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是___________ 。
(5)已知: ,“除铁”后所得滤液中
,“除铁”后所得滤液中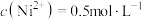 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中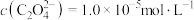 ,则沉镍率=
,则沉镍率=___________ [沉镍率=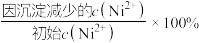 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。
(6) 在加热过程中会生成
在加热过程中会生成 ,已知
,已知 中钴显+2价和+3价,
中钴显+2价和+3价, 晶体的晶胞结构如图所示,则顶点上的离子为
晶体的晶胞结构如图所示,则顶点上的离子为___________ (用离子符号表示)。
 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如图:
等)中回收有价金属的工艺流程如图: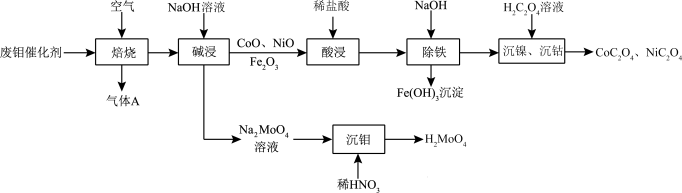
(1)基态Mo原子的价层电子排布式为
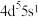 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,这样做的优点是

 转化为
转化为 ,写出“碱浸”时
,写出“碱浸”时 参与反应的离子方程式:
参与反应的离子方程式:(4)已知
 和
和 不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是
不易被稀硝酸氧化,但“酸浸”过程中仍不能用稀硝酸替换稀盐酸,可能的原因是(5)已知:
 ,“除铁”后所得滤液中
,“除铁”后所得滤液中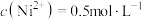 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中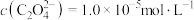 ,则沉镍率=
,则沉镍率=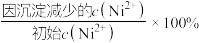 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。(6)
 在加热过程中会生成
在加热过程中会生成 ,已知
,已知 中钴显+2价和+3价,
中钴显+2价和+3价, 晶体的晶胞结构如图所示,则顶点上的离子为
晶体的晶胞结构如图所示,则顶点上的离子为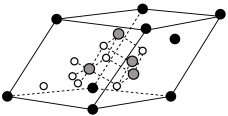
您最近一年使用:0次
10 . 将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
A.基态Cu原子的电子排布式为 |
B.过程①的离子方程式为: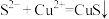 |
C.氧化性: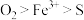 |
D.相同条件下, 和空气的比例不影响处理效果 和空气的比例不影响处理效果 |
您最近一年使用:0次



