解题方法
1 . 用下列试剂和试管中的物质不能完成相应实验目的的是
| 实验目的 | 试剂 | 试管中的物质 |   | |
| A | 鉴别碳酸钠和碳酸氢钠固体 | 稀盐酸 | ①碳酸钠②碳酸氢钠 | |
| B | 比较 、 、 、 、 的还原性 的还原性 | 氯水 | ① 溶液② 溶液② 溶液 溶液 | |
| C | 证明苯分子中没有碳碳双键 |  的 的 溶液 溶液 | ①苯②己烯 | |
| D | 探究接触面积对反应速率的影响 | VmL、 的盐酸 的盐酸 | ①ag大理石块②ag大理石粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . “优先反应思想”是一条重要的化学学科思想.根据所学知识及题目提供的相关数据,回答下列问题:
 向
向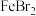 溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是
溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是 ______ ,用实验证明你的观点,简述实验操作及现象 ______ .
 用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是
用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是 ______ .
 已知常温下一些电解质的相关数据如表:
已知常温下一些电解质的相关数据如表:
 向等物质的量浓度的
向等物质的量浓度的 、
、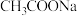 、NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是
、NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是 ______ .
 向浓度均为
向浓度均为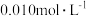 的NaCl、
的NaCl、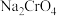 组成的混合溶液中逐滴加入浓度为
组成的混合溶液中逐滴加入浓度为 溶液,首先生成的沉淀其化学式为
溶液,首先生成的沉淀其化学式为 ______ .
 分别向四份各100mL、浓度均为
分别向四份各100mL、浓度均为 的
的 溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
 根据表中的数据可求出粉末中铁、铜的物质的量之比为
根据表中的数据可求出粉末中铁、铜的物质的量之比为 ______ .
 根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有
根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有 用离子符号表示
用离子符号表示
______ .
 向
向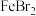 溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是
溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是  用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是
用惰性电极电解由等物质的量的NaBr、KI、NaCl组成的混合溶液,阳极首先发生的电极反应式是  已知常温下一些电解质的相关数据如表:
已知常温下一些电解质的相关数据如表:  |  | HClO |  |
 | AgCl |  | |
 |  | 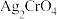 | 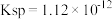 |
 向等物质的量浓度的
向等物质的量浓度的 、
、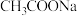 、NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是
、NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是  向浓度均为
向浓度均为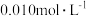 的NaCl、
的NaCl、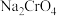 组成的混合溶液中逐滴加入浓度为
组成的混合溶液中逐滴加入浓度为 溶液,首先生成的沉淀其化学式为
溶液,首先生成的沉淀其化学式为  分别向四份各100mL、浓度均为
分别向四份各100mL、浓度均为 的
的 溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据: | Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
FeCl3溶液体积 | 100 | 100 | 100 | 100 |
加入粉末质量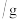 | 3 |  | 9 | 12 |
剩余粉末质量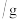 | 0 | 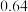 |  |  |
 根据表中的数据可求出粉末中铁、铜的物质的量之比为
根据表中的数据可求出粉末中铁、铜的物质的量之比为  根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有
根据表中的数据分析Ⅰ反应后的溶液中存在的金属阳离子有 用离子符号表示
用离子符号表示
您最近一年使用:0次
3 . 某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是_________ 。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。
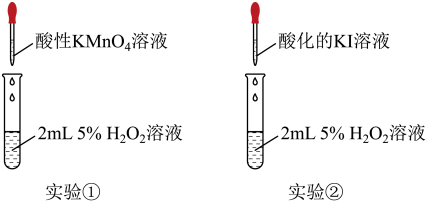
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有________ 。
(3)实验②是为了验证H2O2的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式____________ 。
解释和结论:
(4)以上实验可得出的结论是______________________ 。
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。

(2)实验①利用了酸性高锰酸钾的
(3)实验②是为了验证H2O2的
解释和结论:
(4)以上实验可得出的结论是
您最近一年使用:0次
2020-01-10更新
|
734次组卷
|
8卷引用:北京市昌平区2019-2020学年高一上学期期末考试化学试题
名校
解题方法
4 . 某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
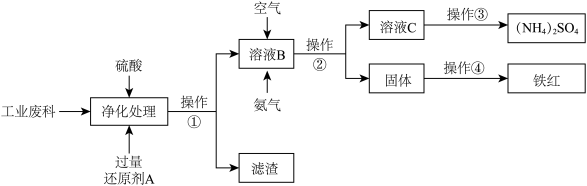
回答下列问题:
(1)滤渣的成分为______________ ,操作②的名称为____________ 。
(2)上图溶液B中所发生反应的离子方程式为_________________________________ 。
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是___________________
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要____________________________ 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。

①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________ →________ →________ →D(除D装置外,其他装置不能重复使用),最后D装置中所加药品为________ ,其作用是_______________________________ 。

回答下列问题:
(1)滤渣的成分为
(2)上图溶液B中所发生反应的离子方程式为
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。

①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→
您最近一年使用:0次
名校
5 . 已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡: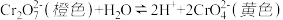
实验①:向2mL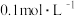 K2Cr2O7溶液中滴入3滴
K2Cr2O7溶液中滴入3滴 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓
NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓 ,溶液由黄色变为橙色.
,溶液由黄色变为橙色.
实验②:向2mL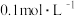 酸化的K2Cr2O7溶液中滴入适量
酸化的K2Cr2O7溶液中滴入适量 溶液,溶液由橙色变为绿色,发生反应:
溶液,溶液由橙色变为绿色,发生反应: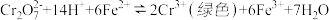 .
.
下列分析正确的是( )
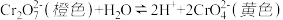
实验①:向2mL
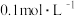 K2Cr2O7溶液中滴入3滴
K2Cr2O7溶液中滴入3滴 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓
NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓 ,溶液由黄色变为橙色.
,溶液由黄色变为橙色.实验②:向2mL
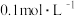 酸化的K2Cr2O7溶液中滴入适量
酸化的K2Cr2O7溶液中滴入适量 溶液,溶液由橙色变为绿色,发生反应:
溶液,溶液由橙色变为绿色,发生反应: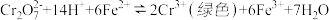 .
.下列分析正确的是( )
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: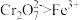 |
C. 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
| D.稀释 K2Cr2O7溶液时,溶液中各离子浓度均减小 |
您最近一年使用:0次
2019-08-19更新
|
888次组卷
|
15卷引用:2015届北京市海淀区高三一模理综化学试卷
2015届北京市海淀区高三一模理综化学试卷2015届浙江省宁波市高三4月模拟练习化学试卷2016届辽宁省大连二十四中高三上学期期中测试化学试卷2016-2017学年天津市六校高二上学期期中化学卷北京市西城区重点中学2018届高三上学期期末复习检验化学试题【全国百强校】河北省辛集中学2017-2018学年高二6月月考化学试题甘肃省兰州第一中学2018-2019学年高二(理)上学期期中考试化学试题百所名校联考-化学物质及其变化北京师范大学附中2019-2020学年高二上学期期中考试化学试题(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)(已下线)2.2.2 影响化学平衡的因素(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)练习4 化学平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)微专题07 氧化性和还原性强弱的实验探究及应用-备战2022年高考化学考点微专题重庆市育才中学2021-2022学年上学期高二上学期第六次定时练习化学试题辽宁省部分高中2021-2022学年高三上学期期中评测化学试题
解题方法
6 . 2019年9月12日11时26分,我国在太原卫星发射中心用长征四号乙运载火箭,成功将资源一号02D卫星发射升空。资源一号02D卫星将为国家自然资源资产管理和生态监理工作提供稳定的数据保障,同时兼顾防灾减灾、环境保护、城乡建设、交通运输、应急管理等相关领域应用需求。
(1)卫星改变运行的路线时需要喷火消耗燃料,其燃料一般是肼(N2H4)。肼中N的化合价是___ ,肼在空气中燃烧的化学方程式如下,请用双线桥法标出该反应中电子转移的方向和数目___ 。
N2H4+O2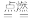 N2+2H2O
N2+2H2O
该反应中的氧化剂是___ ,被氧化的元素是___ ,每生成1molH2O转移电子___ mol。
(2)近几年来,太原市在环境保护方面采取了一系列措施,其中的喷雾车、洒水车都是为了降低空气中的粉尘。含有粉尘的空气是否属于胶体___ (填“是”或“否”),证明的方法是___ ,观察到的现象是___ 。
(1)卫星改变运行的路线时需要喷火消耗燃料,其燃料一般是肼(N2H4)。肼中N的化合价是
N2H4+O2
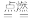 N2+2H2O
N2+2H2O该反应中的氧化剂是
(2)近几年来,太原市在环境保护方面采取了一系列措施,其中的喷雾车、洒水车都是为了降低空气中的粉尘。含有粉尘的空气是否属于胶体
您最近一年使用:0次
7 . 下列解释或结论中,错误的是
A.利用NaOH溶液除去金属铝表面的氧化膜: |
B.NaCl溶液与 溶液均呈中性,说明两溶液中水的电离程度相同 溶液均呈中性,说明两溶液中水的电离程度相同 |
C.1mol某醇与足量的钠反应生成 氢气 氢气 标况下 标况下 ,该醇为二元醇 ,该醇为二元醇 |
D.向KI溶液中滴加氯水和 ,振荡,静置后溶液出现分层且下层显紫色,证明 ,振荡,静置后溶液出现分层且下层显紫色,证明 氧化性强于 氧化性强于 |
您最近一年使用:0次
8 . 向硝酸酸化的2mL0.1mol•L-1AgNO3溶液(pH=2)中加入过量铁粉,振荡后静置,溶液先呈浅绿色,后逐渐呈棕黄色,试管底部仍存有黑色固体,过程中无气体生成。实验小组同学针对该实验现象进行如下探究。
Ⅰ.探究Fe2+产生的原因
(1)提出猜想:Fe2+可能是Fe与____ 或___ 反应的产物。
(2)实验探究:在两支试管中分别加入与上述实验等量的铁粉,再加入不同的液体试剂,5min后取上层清液,分别加入相同体积和浓度的铁氰化钾溶液
①2号试管中所用的试剂为____ 。
②资料显示:该温度下,0.1mol•L-1的AgNO3溶液可以将Fe氧化为Fe2+。但1号试管中未观察到蓝色沉淀的原因可能为____ 。
③小组同学继续进行实验,证明了2号试管得出的结论正确。实验如下:取100mL0.1mol•L-1硝酸酸化的AgNO3溶液(pH=2),加入铁粉井搅拌,分别插入pH传感器和NO3-传感器(传感器可检测离子浓度),得到如图图示,其中pH传感器测得的图示为___ (填“图甲”或“图乙”)。

④实验测得2号试管中有NH4+生成,则2号试管中发生反应的离子方程式为___ 。
Ⅱ.探究Fe3+产生的原因
查阅资料可知,反应中溶液逐渐变棕黄色是因为Fe2+被Ag+氧化。小组同学设计不同实验方案对此进行验证。
(3)方案一;取出少量黑色固体,洗涤后___ (填操作和现象),证明黑色固体中有Ag。
(4)方案二:按图连接装置,一段时间后取出左侧烧杯溶液,加入KSCN溶液,溶液变F红。该实验现象____ (填“能“或“不能“)证明Fe2+可被Ag+氧化,理由为__ 。

Ⅰ.探究Fe2+产生的原因
(1)提出猜想:Fe2+可能是Fe与
(2)实验探究:在两支试管中分别加入与上述实验等量的铁粉,再加入不同的液体试剂,5min后取上层清液,分别加入相同体积和浓度的铁氰化钾溶液
| 液体试剂 | 加入铁氰化钾溶液 | |
| 1号试管 | 2mL.0.1mol•L-1AgNO3溶液 | 无蓝色沉淀 |
| 2号试管 | ______ | 蓝色沉淀 |
②资料显示:该温度下,0.1mol•L-1的AgNO3溶液可以将Fe氧化为Fe2+。但1号试管中未观察到蓝色沉淀的原因可能为
③小组同学继续进行实验,证明了2号试管得出的结论正确。实验如下:取100mL0.1mol•L-1硝酸酸化的AgNO3溶液(pH=2),加入铁粉井搅拌,分别插入pH传感器和NO3-传感器(传感器可检测离子浓度),得到如图图示,其中pH传感器测得的图示为

④实验测得2号试管中有NH4+生成,则2号试管中发生反应的离子方程式为
Ⅱ.探究Fe3+产生的原因
查阅资料可知,反应中溶液逐渐变棕黄色是因为Fe2+被Ag+氧化。小组同学设计不同实验方案对此进行验证。
(3)方案一;取出少量黑色固体,洗涤后
(4)方案二:按图连接装置,一段时间后取出左侧烧杯溶液,加入KSCN溶液,溶液变F红。该实验现象

您最近一年使用:0次
名校
9 . 已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系中,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该氧化还原反应的体系中,还原剂是______ ,化合价没有发生变化的反应物是________ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):__________________________ 。
(3)上述反应中,1 mol氧化剂在反应中转移的电子为_______ mol。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。证明NaBiO3的一个性质是:_______________________________________ 。
(1)该氧化还原反应的体系中,还原剂是
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):
(3)上述反应中,1 mol氧化剂在反应中转移的电子为
(4)如果在反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。证明NaBiO3的一个性质是:
您最近一年使用:0次
名校
10 . 某小组同学设计实验实现几种价态硫元素的转化。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红
(1)写出实现转化的化学方程式_______________
(2)设计实验,证明实现了该转化(写出操作和现象)_______________ 。
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
(3)i中加入的物质是__________ ,该转化利用的是SO2的_______ 性质。
(4)写出iii的离子方程式_____________ 。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红
(1)写出实现转化的化学方程式
(2)设计实验,证明实现了该转化(写出操作和现象)
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。

(3)i中加入的物质是
(4)写出iii的离子方程式
您最近一年使用:0次
2020-01-10更新
|
155次组卷
|
2卷引用:北京市昌平区2019-2020学年高一上学期期末考试化学试题



