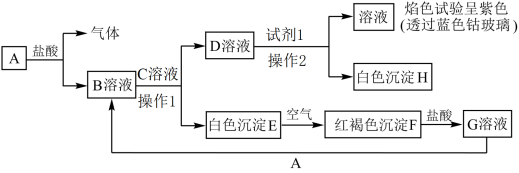
1 . 各物质间的转化关系如图所示,其中A为生活中常见金属单质,根据以下转化关系,回答问题:___________ F(红褐色沉淀)___________ 。
(2)操作1和操作2操作名称是___________ 。
(3)检验G中金属阳离子的试剂为___________ 。
(4)①E转化为红褐色沉淀化学方程式为:___________ 。
②G溶液和A反应的离子方程式为:___________ 。
(2)操作1和操作2操作名称是
(3)检验G中金属阳离子的试剂为
(4)①E转化为红褐色沉淀化学方程式为:
②G溶液和A反应的离子方程式为:
您最近一年使用:0次
2023-02-14更新
|
216次组卷
|
3卷引用:江西省宜春市宜丰中学2022-2023学年高一下学期3月月考化学试题
2 . 由短周期元素组成的中学常见物质A、B、C、D、E、X存在如图所示的转化关系(部分生成物和反应条件略去)。下列推断错误的是
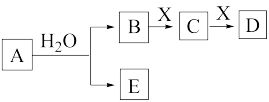

| A.若D是白色沉淀,D与A的摩尔质量相等,则X可能是铝盐 |
B.若A是金属单质,B和D的反应可能是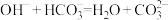 |
C.若D是 ,则A可能是 ,则A可能是 ,X只有2种同素异形体 ,X只有2种同素异形体 |
D.若A是氯气,X是 ,C是气体,则D和E能发生反应 ,C是气体,则D和E能发生反应 |
您最近一年使用:0次
2023-02-13更新
|
993次组卷
|
5卷引用:江西省贵溪市实验中学2023-2024学年高三上学期9月第一次月考化学试题
江西省贵溪市实验中学2023-2024学年高三上学期9月第一次月考化学试题陕西省咸阳市2022-2023学年高三高考模拟检测(一)化学试题 (已下线)回归教材重难点05 元素周期律再熟悉-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)先机卷 03 -【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)第07练 元素及其化合物基础知识和应用 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
3 . 在实验室进行少量铁粉和硫粉混合加热的实验,将其产物又进行了系列实验,流程如下。下列说法正确的是
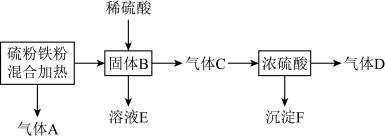

A.气体A和D含有 ,且均为氧化产物 ,且均为氧化产物 |
| B.上述过程中,硫元素共参加了2个氧化还原反应 |
| C.气体A、C混合也能生成固体F |
D.气体C与浓硫酸反应的化学方程式为: |
您最近一年使用:0次
2023-02-12更新
|
1319次组卷
|
4卷引用:江西省南昌市进贤县第一中学2022-2023学年高一下学期第一次月考化学试题
解题方法
4 . Ⅰ.绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程。已知:NO+NO2+2OH-=2NO
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程。已知:NO+NO2+2OH-=2NO +H2O,请回答下列问题:
+H2O,请回答下列问题:
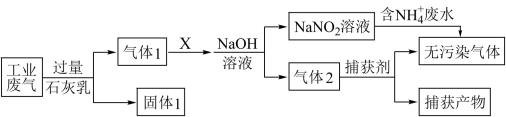
(1)固体1中主要含有_______ 。
(2)X可以是_______ ,是否需要过量_______ (填“需要”或“不需要”)。
(3)处理含NH 废水时,发生的离子反应是
废水时,发生的离子反应是_______ 。
(4)捕获剂所捕获的气体主要是_______ 。
Ⅱ.今年我国多个城市遭遇雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
(5)NO2可用水吸收,相应的化学反应方程式为_______ 。
(6)利用反应6NO2+8NH3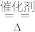 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是_______ L。
(7)硝酸工业尾气中含NO和NO2气体,常用NaOH溶液来吸收,反应方程式为
NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O,则NO和NO2的混合气能被足量氢氧化钠溶液完全吸收的条件是n(NO2):n(NO)_______ 。
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程。已知:NO+NO2+2OH-=2NO
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程。已知:NO+NO2+2OH-=2NO +H2O,请回答下列问题:
+H2O,请回答下列问题:
(1)固体1中主要含有
(2)X可以是
(3)处理含NH
 废水时,发生的离子反应是
废水时,发生的离子反应是(4)捕获剂所捕获的气体主要是
Ⅱ.今年我国多个城市遭遇雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
(5)NO2可用水吸收,相应的化学反应方程式为
(6)利用反应6NO2+8NH3
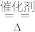 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是(7)硝酸工业尾气中含NO和NO2气体,常用NaOH溶液来吸收,反应方程式为
NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O,则NO和NO2的混合气能被足量氢氧化钠溶液完全吸收的条件是n(NO2):n(NO)
您最近一年使用:0次
解题方法
5 . 在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。

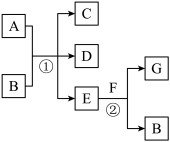
回答下列问题:
(1)A、G的化学式分别为______ 、_________ 。
(2)写出反应①的化学方程式__________________________ 。
(3)在反应②中,每生成2.24L气体G(标准状况)时,消耗F_____ g。
(4)A与石灰乳反应制得的漂白粉的有效成分是__________ (填化学式),该物质在空气中失效的原因是 ________________________ (用化学方程式表示)。


回答下列问题:
(1)A、G的化学式分别为
(2)写出反应①的化学方程式
(3)在反应②中,每生成2.24L气体G(标准状况)时,消耗F
(4)A与石灰乳反应制得的漂白粉的有效成分是
您最近一年使用:0次
名校
解题方法
6 . 某金属单质在一定条件下有如下转化关系。Y是氧化物,能被强磁铁吸附,溶液P呈浅绿色。

请回答下列问题:
(1)W是___________ (填化学式),Y的俗名是___________ 。
(2)写出X在高温下与水蒸气反应的化学方程式:___________ 。
(3)检验Q中显黄色的阳离子实验方法是___________ 。
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:___________ 。
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有___________ (填两条)。
(6)在溶液Q中加入单质M粉末从反应的离子方程式为___________ 。

请回答下列问题:
(1)W是
(2)写出X在高温下与水蒸气反应的化学方程式:
(3)检验Q中显黄色的阳离子实验方法是
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有
(6)在溶液Q中加入单质M粉末从反应的离子方程式为
您最近一年使用:0次
2022-12-10更新
|
236次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
解题方法
7 . 目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融) 2Na+Cl2↑。已知A、B、C、D、E、F有如图转化关系:
2Na+Cl2↑。已知A、B、C、D、E、F有如图转化关系:
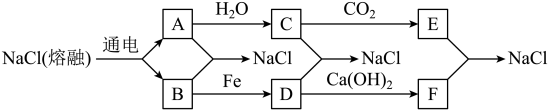
(1)写出化学式:E_______ 。
(2)C与过量的CO2反应的离子方程式为_______ 。
(3)将4.6g金属钠投入95.6g水中,所得溶液中溶质的质量分数为_______ (用百分数表示)
(4)若把A投入盛有D的溶液中,溶液中出现_______ (填沉淀颜色)沉淀,该过程所发生的总反应的化学方程式为_______ 。
 2Na+Cl2↑。已知A、B、C、D、E、F有如图转化关系:
2Na+Cl2↑。已知A、B、C、D、E、F有如图转化关系:
(1)写出化学式:E
(2)C与过量的CO2反应的离子方程式为
(3)将4.6g金属钠投入95.6g水中,所得溶液中溶质的质量分数为
(4)若把A投入盛有D的溶液中,溶液中出现
您最近一年使用:0次
名校
解题方法
8 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为_______ ;丁属于_______ (“酸性”或“碱性”)氧化物。
(2)根据氯元素的化合价判断,乙物质的性质_______ (填标号)。
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为: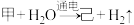 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是_______ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_______ 。庚与洁厕灵(主要成分盐酸)同时使用会产生有毒的氯气,写出反应的离子方程式:_______ 。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为_______ 。
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式_______ 。

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质的性质
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:
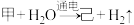 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.根据下图转化关系及现象回答问题:
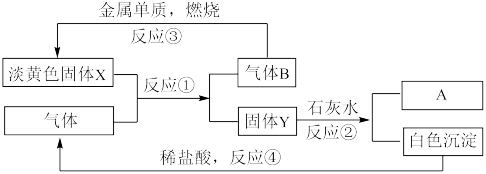
(1)物质A是_______ (填写化学式)
(2)反应①的化学方程式为_______ 。
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是_______ 。(填序号)
①NaCl溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液
Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。
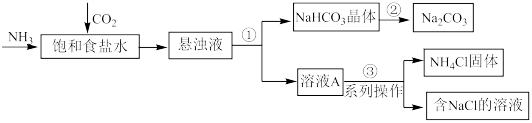
(4)步骤①②③中涉及“过滤”操作的是_______ (填序号)。
(5)向饱和食盐水中通入 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是_______ 。
(6)从步骤①中分离出的 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是_______ (写出杂质的化学式),欲得到纯净的 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,_______ 。

(1)物质A是
(2)反应①的化学方程式为
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是
①NaCl溶液 ②
 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。

(4)步骤①②③中涉及“过滤”操作的是
(5)向饱和食盐水中通入
 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是(6)从步骤①中分离出的
 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
您最近一年使用:0次
2022-11-16更新
|
554次组卷
|
5卷引用:江西省丰城中学2022-2023学年高一上学期第三次段考化学试卷
10 . 图中A为一种中学化学中常见的金属单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
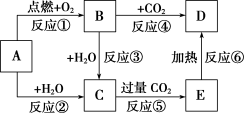
(1)B的化学式中阳离子和阴离子的个数比为______ 。
(2)以上6个反应中属于氧化还原反应的有____________ (填写编号)。
(3)写出B→D反应的化学方程式________________________ 。
(4)若用所示装置验证D、E的热稳定性,则乙中装入的固体最好是______ (填化学式)。
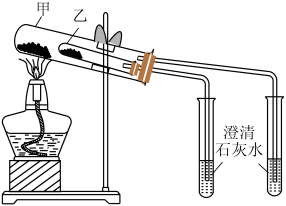
(5)向滴入酚酞的D溶液中滴入少量稀盐酸,现象是没有气泡生成,溶液__________ ,反应的离子方程式为_______________ ,继续滴加盐酸至过量,现象是_______________
(6)将一定量的B投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后溶液中上述离子数目明显增多的有
,反应完毕后溶液中上述离子数目明显增多的有______ (填离子符号).

(1)B的化学式中阳离子和阴离子的个数比为
(2)以上6个反应中属于氧化还原反应的有
(3)写出B→D反应的化学方程式
(4)若用所示装置验证D、E的热稳定性,则乙中装入的固体最好是

(5)向滴入酚酞的D溶液中滴入少量稀盐酸,现象是没有气泡生成,溶液
(6)将一定量的B投入到含有下列离子的溶液中:
 、
、 、
、 、
、 ,反应完毕后溶液中上述离子数目明显增多的有
,反应完毕后溶液中上述离子数目明显增多的有
您最近一年使用:0次
2022-11-05更新
|
409次组卷
|
3卷引用:江西省上饶市万年中学2023届高三一模化学试题



