名校
1 . 设 为阿伏加德罗常数的值,下列有关叙述正确的是
为阿伏加德罗常数的值,下列有关叙述正确的是
 为阿伏加德罗常数的值,下列有关叙述正确的是
为阿伏加德罗常数的值,下列有关叙述正确的是A.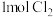 溶于水,溶液中 溶于水,溶液中 、 、 、 、 的粒子数之和等于 的粒子数之和等于 |
B.14g由乙烯和丙烯组成的混合气体中氢原子数为 |
C.高温下,5.6gFe与足量的水蒸气充分反应,转移的电子总数为 |
D.标准状况下,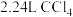 含有的共价键数为 含有的共价键数为 |
您最近一年使用:0次
2022-11-09更新
|
168次组卷
|
3卷引用:湖南省株洲市第二中学2022-2023学年高三上学期12月月考化学(B)试题
名校
2 . 下列关于实验的叙述中,不正确的是
| 选项 | 实验操作 | 实验现象或结论 |
| A | 把一小块钠迅速投入到热坩埚中,继续加热坩埚片刻 | 钠受热后熔成小球,剧烈燃烧,火焰呈黄色,产物为淡黄色固体 |
| B | 把一小块钠投入到滴有酚酞的冷水中 | 钠熔化成闪亮的小球,在水面上四处游动,有“嘶嘶”的响声发出,反应后溶液变红 |
| C | 将红色干花放入盛有干燥氯气的集气瓶中,盖上玻璃片 | 干花褪色,证明氯气具有漂白性 |
| D | 用洁净铂丝蘸取溶液,在酒精灯外焰上灼烧,观察到火焰呈黄色 | 溶液中一定不存在K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-04更新
|
135次组卷
|
2卷引用:湖南省株洲市九方中学2022-2023学年高一上学期第三次月考化学试题
解题方法
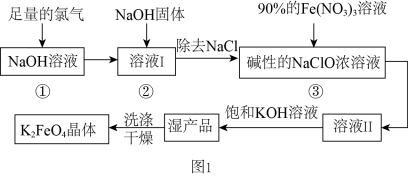
3 . 高铁酸钾( )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
 )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
| A.反应①应在较高温度下进行,升高温度加快反应速率 |
B.在溶液Ⅰ中加入NaOH固体可与过量的 继续反应,生成更多的NaClO 继续反应,生成更多的NaClO |
C.反应③的离子方程式为: |
| D.该工艺流程中可循环使用的物质是NaOH |
您最近一年使用:0次
解题方法
4 . 部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理 的是
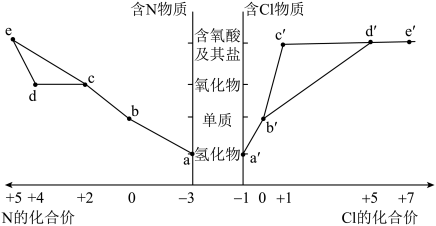

| A.b′通入热的NaOH溶液中可以得到e′ | B.工业上通过a→b→c→d→e来制备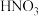 |
| C.久制的b′水溶液pH会变小 | D.a→b过程属于氮的固定 |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式能用来解释相应实验操作或现象,且操作和现象均描述正确的是
A.向硫酸铜溶液中加入过量氨水,产生蓝色沉淀: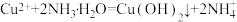 |
B.用酸化的硝酸铁溶液腐蚀铜箔,刻印电路板: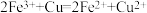 |
C.向 中加入过量的HI溶液,使之溶解: 中加入过量的HI溶液,使之溶解: |
D.向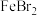 溶液中滴加少量氯水,溶液变黄: 溶液中滴加少量氯水,溶液变黄: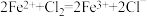 |
您最近一年使用:0次
2022-10-13更新
|
265次组卷
|
2卷引用:湖南省株洲市攸县第一中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
6 . 某溶液Q中含有如表所示离子中的5种离子,且离子浓度均为0.5mol/L(不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。
已知 在酸性溶液中会发生歧化反应。请回答下列问题:
在酸性溶液中会发生歧化反应。请回答下列问题:
(1)由“加入足量稀氢溴酸,……”“反应前后阴离子种类不变”推知:溶液Q中一定不含的阴离子有_______ (填数字)种。
(2)综合推断,溶液Q中一定含有的阳离子有_______ (填离子符号,下同)。产生气体R的反应中,原溶液中过量的离子是_______ ,反应后溶液中物质的量一定发生变化的阳离子有_______ 。
(3)一定量溶液Q与氯气缓慢反应,反应后的溶液分为3份,分别进行以下操作,实验现象如图:
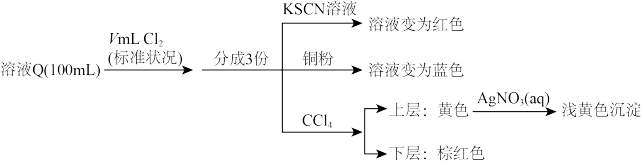
①铜粉参与的反应中,氧化产物是_______ (填离子符号)。
②当V=448时,向溶液Q中通入氯气时发生反应的离子方程式为_______ ;假设不考虑 与
与 的反应,则根据实验现象可推算出V的范围为
的反应,则根据实验现象可推算出V的范围为_______ <V<_______ 。
| 阳离子 | 阴离子 |
 、 、 、 、 、 、 、 、 、 、 、 、 、 、 |  、 、 、 、 、 、 、 、 、 、 、 、 、 、 |
 在酸性溶液中会发生歧化反应。请回答下列问题:
在酸性溶液中会发生歧化反应。请回答下列问题:(1)由“加入足量稀氢溴酸,……”“反应前后阴离子种类不变”推知:溶液Q中一定不含的阴离子有
(2)综合推断,溶液Q中一定含有的阳离子有
(3)一定量溶液Q与氯气缓慢反应,反应后的溶液分为3份,分别进行以下操作,实验现象如图:

①铜粉参与的反应中,氧化产物是
②当V=448时,向溶液Q中通入氯气时发生反应的离子方程式为
 与
与 的反应,则根据实验现象可推算出V的范围为
的反应,则根据实验现象可推算出V的范围为
您最近一年使用:0次
2022-10-10更新
|
403次组卷
|
4卷引用:湖南省株洲市攸县第二中学2023届高三上学期第一次月考化学试题
名校
解题方法
7 . 卤素间形成的化合物如“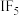 、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应正确的是
、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应正确的是
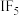 、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应正确的是
、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应正确的是A.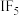 和卤素单质分子都是非极性分子 和卤素单质分子都是非极性分子 |
B.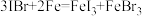 |
C.1 mol BrCl与足量 溶液完全反应时转移的电子为1mol 溶液完全反应时转移的电子为1mol |
| D.IBr与NaOH溶液发生的反应不是氧化还原反应 |
您最近一年使用:0次
名校
解题方法
8 . 四氯化锡是一种重要的化工产品,实验室可用熔融的锡与Cl2反应制备SnCl4,装置如图所示。
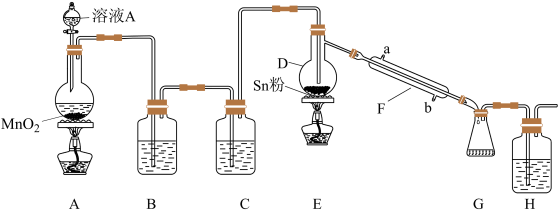
已知:①金属锡的熔点为231℃,化学活泼性与铁相似;
②干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4常温下为无色液体,沸点为114℃;
③SnCl4极易水解生成SnO2•xcH2O,并产生白雾;
④Sn2+易被氧化。
回答下列问题:
(1)检查装置气密性并加入Sn,先加热装置____ (填“A”或“E”),装置A内发生反应的离子方程式为_____ 。
(2)如果去掉装置B,从实验安全的角度看可能产生的影响是_____ 。
(3)实验过程中,发现装置G中有____ 产生(填现象),改进的措施为_____ 。
(4)所得产品中可能含有SnCl2,可用碘量法测定产品SnCl4的纯度。准确称取该样品mg,放入锥形瓶中,用少量浓盐酸溶解,再加水稀释,用淀粉溶液作指示剂,用0.1mol•L-1碘标准溶液滴定,发生反应Sn2++I2=Sn4++2I—,滴定到终点时消耗碘标准溶液40.00mL。产品中SnCl4的纯度为____ (用含m的代数式表示)。下列情况会导致纯度的测定值偏小的是____ (填标号)。
A.滴定管未用碘标准溶液润洗
B.Sn2+在盐酸中被空气氧化
C.滴定达终点时发现滴定管尖嘴内有气泡生成

已知:①金属锡的熔点为231℃,化学活泼性与铁相似;
②干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4常温下为无色液体,沸点为114℃;
③SnCl4极易水解生成SnO2•xcH2O,并产生白雾;
④Sn2+易被氧化。
回答下列问题:
(1)检查装置气密性并加入Sn,先加热装置
(2)如果去掉装置B,从实验安全的角度看可能产生的影响是
(3)实验过程中,发现装置G中有
(4)所得产品中可能含有SnCl2,可用碘量法测定产品SnCl4的纯度。准确称取该样品mg,放入锥形瓶中,用少量浓盐酸溶解,再加水稀释,用淀粉溶液作指示剂,用0.1mol•L-1碘标准溶液滴定,发生反应Sn2++I2=Sn4++2I—,滴定到终点时消耗碘标准溶液40.00mL。产品中SnCl4的纯度为
A.滴定管未用碘标准溶液润洗
B.Sn2+在盐酸中被空气氧化
C.滴定达终点时发现滴定管尖嘴内有气泡生成
您最近一年使用:0次
2022-09-30更新
|
406次组卷
|
2卷引用:湖南省湖湘名校教育联合体2023届高三上学期9月大联考化学试题
解题方法
9 . 1774年,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热时,制得了氯气,该方法现在仍在实验室用于制备Cl2。下列反应的离子方程式正确的是
A.MnO2与浓盐酸加热反应制取氯气:MnO2+4HCl Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| B.湿润的KI-淀粉试纸检验氯气:Cl2+2KI=2K++2Cl-+I2 |
C.相同条件下,Cl2与SO2按体积比1:1通入水中:Cl2+SO2+2H2O=4H++2Cl-+SO |
| D.用氢氧化钠溶液吸收多余氯气:Cl2+2OH-=2ClO-+H2 |
您最近一年使用:0次
10 . 五种主族元素X、Y、Z、M和N在周期表中的位置如图,下列说法正确的是


| A.M的原子半径比N小 |
| B.M的简单氢化物的热稳定性比Y的简单氢化物强 |
| C.Z的最高价氧化物对应的水化物为弱碱 |
| D.N的单质与Z的最高价氧化物的水化物反应的产物之一可用于杀菌消毒 |
您最近一年使用:0次



