名校
解题方法
1 . Ⅰ.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入6mL0.5mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:___ 。
(2)实验②的化学反应中转移电子的物质的量是__ 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是__ 。
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是___ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是___ (用离子方程式表示)。
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入6mL0.5mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:
(2)实验②的化学反应中转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
2019-12-10更新
|
145次组卷
|
7卷引用:重庆市南开中学2019届高三上学期第一次月考化学试题
重庆市南开中学2019届高三上学期第一次月考化学试题吉林省东辽五中2020届高三上学期9月月考化学试题山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题江西省南昌市新建县第一中学2020届高三上学期第一次月考化学试题吉林省大安市第一中学校2021届高三上学期第二次月考化学试题2018版化学(苏教版)高考总复习课时跟踪训练:氧化还原反应基础(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (题型专练)
名校
解题方法
2 . 铜及其化合物在工业生产中应用广泛。
Ⅰ.某同学设计如下实验装置测定铜的相对原子质量(夹持和加热仪器已略去),并检验氯气的氧化性。
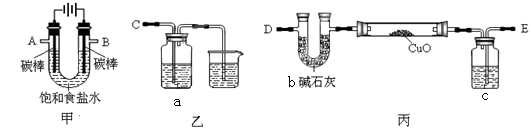
(1)该实验装置的连接顺序为:A连接________ ,B连接________ (填字母)。
(2)乙装置a瓶中的溶液可以是_______
A.NaOH溶液 B.Na2S溶液 C.酸性KMnO4溶液 D.含少量KSCN的FeCl2溶液
(3)对丙装置进行加热前需要________ 。
(4)准确称量 m g CuO进行实验,当CuO完全反应后测出b中增重n g。则Cu的相对原子质量为________ (只要求列出算式)。该实验方案的装置有不合理之处,若不加以改正会导致测定结果________ (填“偏大”、”偏小“或”不变“)。
Ⅱ.研究发现Cu与稀盐酸不反应,但在持续通入空气的条件下可反应生成CuCl2。
(5)已知Fe3+对该反应有催化作用,其催化原理如图所示:
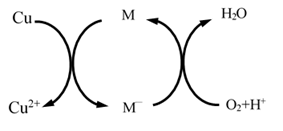
则图中的M‘为________ (填化学符号)
(6)向CuCl2溶液中通入H2S气体,可产生CuS沉淀,反应离子方程式为:Cu2++H2S=CuS(s)+2H+ , 则该反应的平衡常数K=________ (保留一位小数)。已知:CuS溶度积KSP=1.0×10-36 , H2S电离常数Ka1=1.3×10-7 , Ka2=7.0×10-15。
Ⅰ.某同学设计如下实验装置测定铜的相对原子质量(夹持和加热仪器已略去),并检验氯气的氧化性。

(1)该实验装置的连接顺序为:A连接
(2)乙装置a瓶中的溶液可以是
A.NaOH溶液 B.Na2S溶液 C.酸性KMnO4溶液 D.含少量KSCN的FeCl2溶液
(3)对丙装置进行加热前需要
(4)准确称量 m g CuO进行实验,当CuO完全反应后测出b中增重n g。则Cu的相对原子质量为
Ⅱ.研究发现Cu与稀盐酸不反应,但在持续通入空气的条件下可反应生成CuCl2。
(5)已知Fe3+对该反应有催化作用,其催化原理如图所示:

则图中的M‘为
(6)向CuCl2溶液中通入H2S气体,可产生CuS沉淀,反应离子方程式为:Cu2++H2S=CuS(s)+2H+ , 则该反应的平衡常数K=
您最近一年使用:0次
名校
3 . Ⅰ.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成都有着重要的应用。
(1)NaClO中Cl的化合价为___________ ,有较强的___________ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式___________ 。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO ,此反应的离子方程式
,此反应的离子方程式___________ 。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ.某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:

(3)另一种制氯气的方法是用固体高锰酸钾与浓盐酸,在常温条件下制取氯气,写出化学反应方程式___________ ;
(4)C装置的作用是___________ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是___________ 。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,可将装置如何改进___________ 。
(1)NaClO中Cl的化合价为
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO
 ,此反应的离子方程式
,此反应的离子方程式②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:

(3)另一种制氯气的方法是用固体高锰酸钾与浓盐酸,在常温条件下制取氯气,写出化学反应方程式
(4)C装置的作用是
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,可将装置如何改进
您最近一年使用:0次
4 . 某化学小组同学在学习Cl2的实验室制法后,发现用加热浓盐酸与MnO2混合物的方法制Cl2既浪费能源又不易控制温度,他们现欲对该实验进行改进并验证Cl2的部分性质,进行了如下探究活动。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:___________
(2)选择实验装置:现有如图所示的装置,可以选择其中的___________ (填序号)进行实验。
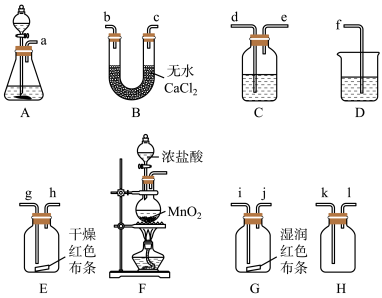
(3)装置的正确连接顺序为___________ (用小写字母序号表示)。
(4)①实验时C中所装液体是___________ 。
②在制氯气前,必须进行的一项操作是___________ 。
③D中所装试剂是___________ ,发生反应的离子方程式是___________ 。
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于___________ 反应(填四种基本反应类型之一)
②在450℃条件下,反应II的化学方程式为___________
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:3Cl2+____ =_____ +N2
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:
(2)选择实验装置:现有如图所示的装置,可以选择其中的

(3)装置的正确连接顺序为
(4)①实验时C中所装液体是
②在制氯气前,必须进行的一项操作是
③D中所装试剂是
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于
②在450℃条件下,反应II的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:3Cl2+
您最近一年使用:0次
2022-03-17更新
|
86次组卷
|
2卷引用:河南省南阳市第一中学校2021-2022学年高一上学期第三次月考化学试题
5 . 某化学小组在学习了 的实验室制法后,发现用加热浓盐酸与
的实验室制法后,发现用加热浓盐酸与 的方法制
的方法制 既浪费能源又不宜控制温度,他们现欲对该实验进行改进并验证
既浪费能源又不宜控制温度,他们现欲对该实验进行改进并验证 的部分性质,进行了如下探究活动。
的部分性质,进行了如下探究活动。
查阅资料: 和
和 的氧化性均比
的氧化性均比 的氧化性强,在不加热的条件下即可与浓盐酸反应制取
的氧化性强,在不加热的条件下即可与浓盐酸反应制取 。
。
(1)反应原理: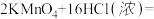
________________________ 。
(2)现有如图所示的装置:
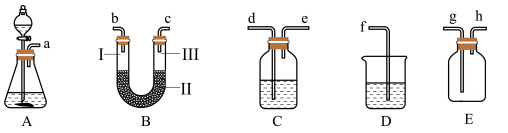
①实验时C中所装液体是______________ ,其作用是______________________ 。
②在制氯气前,必须进行的一项操作是_____________________________ 。
③D中所装液体是_____________________________ 。
④装置B的实验目的是验证氯气是否具有漂白性,因此B中Ⅰ、Ⅱ、Ⅲ处依次放入的物质的组合是________________________ (填序号)。
⑤装置的正确连接顺序为__________________ (用小写字母序号表示)。
 的实验室制法后,发现用加热浓盐酸与
的实验室制法后,发现用加热浓盐酸与 的方法制
的方法制 既浪费能源又不宜控制温度,他们现欲对该实验进行改进并验证
既浪费能源又不宜控制温度,他们现欲对该实验进行改进并验证 的部分性质,进行了如下探究活动。
的部分性质,进行了如下探究活动。查阅资料:
 和
和 的氧化性均比
的氧化性均比 的氧化性强,在不加热的条件下即可与浓盐酸反应制取
的氧化性强,在不加热的条件下即可与浓盐酸反应制取 。
。(1)反应原理:
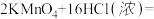
(2)现有如图所示的装置:

①实验时C中所装液体是
②在制氯气前,必须进行的一项操作是
③D中所装液体是
④装置B的实验目的是验证氯气是否具有漂白性,因此B中Ⅰ、Ⅱ、Ⅲ处依次放入的物质的组合是
编号 | Ⅰ | Ⅱ | Ⅲ |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
B | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
您最近一年使用:0次
2020-10-06更新
|
227次组卷
|
2卷引用:内蒙古乌兰浩特第一中学2022-2023学年高一上学期第三次月考化学试题
6 . 用浓盐酸与氯酸钾固体反应制氯气时,发现所得气体颜色偏深,经分析该气体主要含有Cl2和ClO2两种气体,某学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。
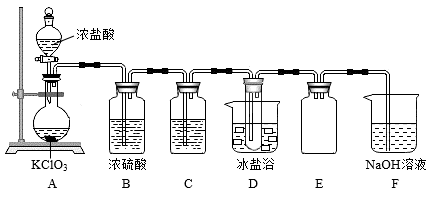
Ⅰ.查阅资料:
ClO2是一种黄色气体,能凝聚成红色液体,熔点-59℃,沸点11℃;能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性;能与NaOH溶液反应生成等物质的量的两种盐,其中一种为NaClO3。
Ⅱ.制备与分离:
(1)实验前应进行的实验操作为_ 。
(2)装置C中盛装的试剂为__ ,装置E的作用是__ 。
(3)F中ClO2与NaOH溶液反应的离子方程式为__ 。
Ⅲ.测量与计算:
反应结束后,测得B、C装置分别增重2.0g和14.2g,将D中的液体溶于水,配成2L溶液,取20.00mL该溶液,调节试样pH<2.0,加入足量KI晶体,振荡后静置片刻;加入指示剂X,用0.200mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00mL。(已知:ClO2+H++I-→I2+Cl-+H2O,2Na2S2O3+I2=Na2S4O6+2NaI)
(4)应选用的指示剂X为__ 。
(5)原装置收集到的ClO2的物质的量为__ (忽略F中吸收的尾气)。
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为__ 。

Ⅰ.查阅资料:
ClO2是一种黄色气体,能凝聚成红色液体,熔点-59℃,沸点11℃;能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性;能与NaOH溶液反应生成等物质的量的两种盐,其中一种为NaClO3。
Ⅱ.制备与分离:
(1)实验前应进行的实验操作为
(2)装置C中盛装的试剂为
(3)F中ClO2与NaOH溶液反应的离子方程式为
Ⅲ.测量与计算:
反应结束后,测得B、C装置分别增重2.0g和14.2g,将D中的液体溶于水,配成2L溶液,取20.00mL该溶液,调节试样pH<2.0,加入足量KI晶体,振荡后静置片刻;加入指示剂X,用0.200mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00mL。(已知:ClO2+H++I-→I2+Cl-+H2O,2Na2S2O3+I2=Na2S4O6+2NaI)
(4)应选用的指示剂X为
(5)原装置收集到的ClO2的物质的量为
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为
您最近一年使用:0次
2020-12-23更新
|
251次组卷
|
3卷引用:重庆市西南大学附属中学校高2021届高三第二次月考化学试题
21-22高一·全国·课时练习
7 . 某化学小组同学发现“84”消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混和有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2.装置中仪器a的名称为_______ 。
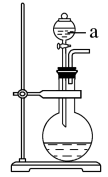
(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是_______ 。
(3)某实验小组对氯水成分和性质进行研究,实验如图:
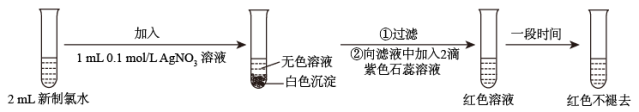
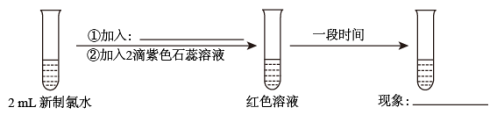
甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
加入:_______ ,现象:_______ 。
(4)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。
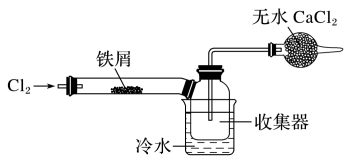
①下列操作步骤的正确排序为_______ (填字母)
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是_______ 。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2.装置中仪器a的名称为

(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是
(3)某实验小组对氯水成分和性质进行研究,实验如图:

甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
加入:

(4)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。

①下列操作步骤的正确排序为
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是
您最近一年使用:0次
8 . I.某化学小组同学发现“84”消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混和有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2。装置中仪器a的名称为___ 。

(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是___ 。
(3)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。
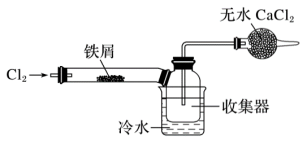
①下列操作步骤的正确排序为___ (填字母)
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是___ 。
(4)世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂。
II.已知:NaCl+3H2O NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
有关物质的熔、沸点如表:
ClO2的生产流程示意图:
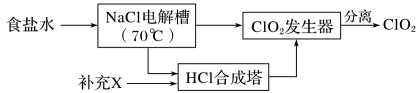
该工艺中,需要补充的物质X为__ (填化学式,下同),能参与循环的物质是___ 。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2。装置中仪器a的名称为

(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是
(3)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。

①下列操作步骤的正确排序为
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是
(4)世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂。
II.已知:NaCl+3H2O
 NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。有关物质的熔、沸点如表:
| 物质 | 熔点/℃ | 沸点/℃ |
| ClO2 | -59 | 11 |
| Cl2 | -107 | -34.6 |

该工艺中,需要补充的物质X为
您最近一年使用:0次
2021-08-19更新
|
323次组卷
|
2卷引用:厦门大学附属科技中学2019-2020学年高一上学期第一次月考(10月)化学试题
名校
解题方法
9 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I- I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。
Ⅰ.制备消毒液(夹持装置略)
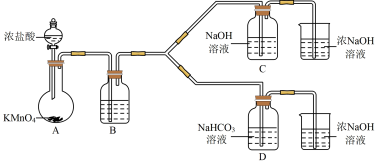
(1)制备NaClO消毒液的装置是__________ (填C或D)。
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用___________________ 。
(3)结合资料i,写出D中反应的化学方程式______________________ 。
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(4)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是________ 。
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是_____________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是______________________ 。
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由______________________ 。
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。Ⅰ.制备消毒液(夹持装置略)

(1)制备NaClO消毒液的装置是
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用
(3)结合资料i,写出D中反应的化学方程式
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体再加入1mo/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近一年使用:0次
2020-05-07更新
|
450次组卷
|
4卷引用:北京市第八十中学2024届高三上学期10月月考化学试题
北京市第八十中学2024届高三上学期10月月考化学试题北京市石景山区2020届高三第一次模拟化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究北京首都师范大学附属中学2022届高三下学期三模化学试题
名校
解题方法
10 . 下列操作、现象和结论均正确且有关联性的是
| 选项 | 操作及现象 | 结论 |
| A | 向品红溶液中通入氯气,品红溶液褪色 | 氯气有漂白性 |
| B | 向酸性 溶液中滴加乙醇,溶液褪色 溶液中滴加乙醇,溶液褪色 | 乙醇表现还原性 |
| C | 在酚酞溶液中加入 粉末,溶液先变红后褪色 粉末,溶液先变红后褪色 |  表现碱性 表现碱性 |
| D | 在盛满 的集气瓶中加入烘干的活性炭,气体颜色变浅 的集气瓶中加入烘干的活性炭,气体颜色变浅 | 活性炭表现还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-27更新
|
391次组卷
|
5卷引用:陕西省汉中市多校2023-2024学年高三上学期第四次联考化学试题



