名校
1 . 实验室用如下装置制取氯气,并进行性质实验。回答下列问题;
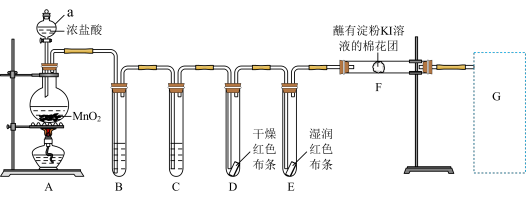
(1)写出A中反应的化学方程式________ 。装置中B盛装________ 装置中C盛装________ 。
(2)能证明氯气无漂白性的现象是________ 。
(3)F处观察到棉花团变蓝色,说明氯气具有________ 性(填“氧化”或“还原”)。
(4)写出G处尾气吸收的离子方程式________ 。
(5)实验室还可用 固体与浓盐酸常温下反应制备氯气;
固体与浓盐酸常温下反应制备氯气;
( ) ( )HCl(浓)=( )KCl+( )
( )HCl(浓)=( )KCl+( ) ( )
( ) ( )
( ) (未配平)。
(未配平)。
请写出该反应配平后的离子方程式:________ 。若生成等量的 ,所需
,所需 与
与 的物质的量之比为
的物质的量之比为________ 。

(1)写出A中反应的化学方程式
(2)能证明氯气无漂白性的现象是
(3)F处观察到棉花团变蓝色,说明氯气具有
(4)写出G处尾气吸收的离子方程式
(5)实验室还可用
 固体与浓盐酸常温下反应制备氯气;
固体与浓盐酸常温下反应制备氯气;( )
 ( )HCl(浓)=( )KCl+( )
( )HCl(浓)=( )KCl+( ) ( )
( ) ( )
( ) (未配平)。
(未配平)。请写出该反应配平后的离子方程式:
 ,所需
,所需 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
2 . 如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:
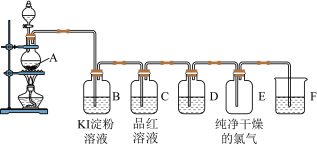
(1)装置A的名称是___________ ,装置A中反应的离子方程式为___________ 。
(2)装置B中的现象是___________ 。反应的离子方程式为___________ 。
(3)装置D中所装试剂是___________ ,作用是___________ 。
(4)装置F中发生反应的化学方程式为___________ 。

(1)装置A的名称是
(2)装置B中的现象是
(3)装置D中所装试剂是
(4)装置F中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO2.D中盛放浓H2SO4的目的是________ 。
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是________ ,对比E和F中现象的差异可得出的结论是________ 。
(3)G处的现象是_______ 。
(4)用化学方程式表示H处尾气吸收装置中的反应原理:________ 。
(5)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如图。

①消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)_____ 。
②需“密封保存”的原因是_______ 。

(1)A中盛有浓盐酸,B中盛有MnO2.D中盛放浓H2SO4的目的是
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(3)G处的现象是
(4)用化学方程式表示H处尾气吸收装置中的反应原理:
(5)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如图。

①消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)
②需“密封保存”的原因是
您最近一年使用:0次
名校
解题方法
4 . I.元素的价-类二维图是我们学习元素及其化合物相关知识的重要模型工具,也是发展证据推理与模型认知这一科学核心素养的重要途径。如图为氯元素的价一类二维图,回答下列问题:
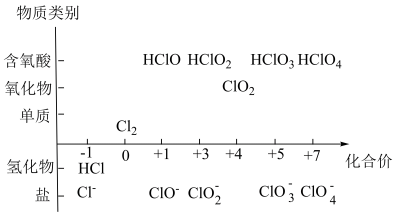
(1)实验室制取Cl2的离子方程式为___________ 。
(2)物质的量均为1mol的Cl2和Fe充分反应,转移电子的物质的量为___________ 。
(3)写出ClO2与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式_________ 。
Ⅱ.ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白。用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质
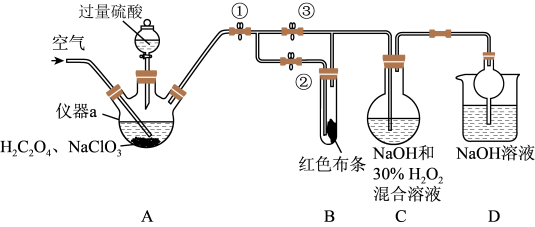
回答下列问题:
(4)装置A用于制备ClO2且生成的ClO2中混有CO2,该反应的化学方程式为___________ 。
(5)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了NaClO2和气体,该反应体现了H2O2的___________ 性;若关闭止水夹③,打开止水夹②,B中可观察到的现象为___________ 。

(1)实验室制取Cl2的离子方程式为
(2)物质的量均为1mol的Cl2和Fe充分反应,转移电子的物质的量为
(3)写出ClO2与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式
Ⅱ.ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白。用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质

回答下列问题:
(4)装置A用于制备ClO2且生成的ClO2中混有CO2,该反应的化学方程式为
(5)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了NaClO2和气体,该反应体现了H2O2的
您最近一年使用:0次
5 . 室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E溶液是无色溶液,F是淡绿色溶液,B和C反应发出苍白色火焰。请回答:
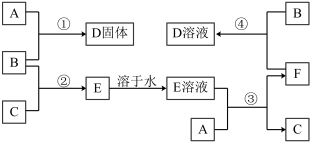
(1)A是___________ ,B是___________ ,C是___________ (填写化学式);
(2)反应①的化学方程式___________ ;
(3)反应③的离子方程式___________ ;
(4)反应④的离子方程式___________ 。

(1)A是
(2)反应①的化学方程式
(3)反应③的离子方程式
(4)反应④的离子方程式
您最近一年使用:0次
6 . 实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
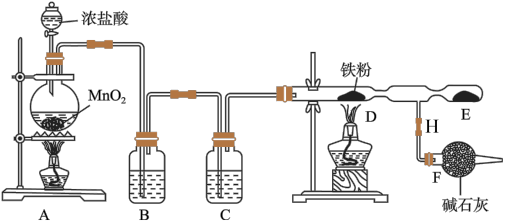
(1)装置B、C中应盛放的试剂名称分别为___________ 、___________ 。
(2)实验时,先点燃A处的酒精灯,让Cl2充满装置,再点燃D处酒精灯,写出A中与D中反应的化学方程式:___________ 、___________ 。
(3)生产消毒液是将氯气通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为___________ 。
(4)F装置所起的作用是___________ 和___________ 。
(5)漂白液露置在空气中,可以生成有漂白性的酸性物质和小苏打溶液,请写出此过程的离子方程式:___________ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(1)装置B、C中应盛放的试剂名称分别为
(2)实验时,先点燃A处的酒精灯,让Cl2充满装置,再点燃D处酒精灯,写出A中与D中反应的化学方程式:
(3)生产消毒液是将氯气通入
 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(4)F装置所起的作用是
(5)漂白液露置在空气中,可以生成有漂白性的酸性物质和小苏打溶液,请写出此过程的离子方程式:
您最近一年使用:0次
名校
7 . 实验室中利用下图装置制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
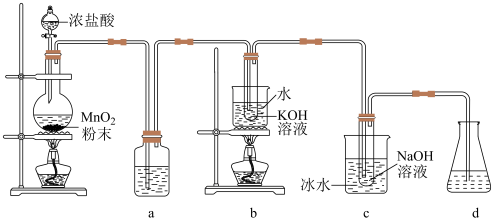
已知: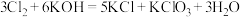
请回答下列问题:
(1)该实验制备氯气的离子方程式为_____ ,盛装浓盐酸的仪器名称为_____ ,a中的试剂为_____ 。检验氯化氢气体中是否混有 ,可采用的方法是
,可采用的方法是_____ 。
A.用加有氢氧化钠的酚酞溶液 B.用干燥有色布条
C.用淀粉碘化钾溶液 D.用饱和食盐水
(2)b中试管内发生反应的氧化剂和还原剂的质量比为________ 。
(3)c中采用冰水浴冷却的目是________ ,c中反应的化学方程式是________ 。
(4)d的作用是吸收多余的氯气,可选用试剂_______。
(5)少量 溶液和
溶液和 溶液分别滴加到1号和2号淀粉-KI试纸上。两个试纸显示的现象不同:1号试纸颜色不变,2号试纸变为
溶液分别滴加到1号和2号淀粉-KI试纸上。两个试纸显示的现象不同:1号试纸颜色不变,2号试纸变为_____ 色。可知该条件下 的氧化能力
的氧化能力_______ (填“大于”或“小于”) 。
。
(6)用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是___________。
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是___________。

 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
已知:
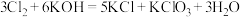
请回答下列问题:
(1)该实验制备氯气的离子方程式为
 ,可采用的方法是
,可采用的方法是A.用加有氢氧化钠的酚酞溶液 B.用干燥有色布条
C.用淀粉碘化钾溶液 D.用饱和食盐水
(2)b中试管内发生反应的氧化剂和还原剂的质量比为
(3)c中采用冰水浴冷却的目是
(4)d的作用是吸收多余的氯气,可选用试剂_______。
| A.稀盐酸 | B. 溶液 溶液 | C.饱和食盐水 | D. 溶液 溶液 |
(5)少量
 溶液和
溶液和 溶液分别滴加到1号和2号淀粉-KI试纸上。两个试纸显示的现象不同:1号试纸颜色不变,2号试纸变为
溶液分别滴加到1号和2号淀粉-KI试纸上。两个试纸显示的现象不同:1号试纸颜色不变,2号试纸变为 的氧化能力
的氧化能力 。
。(6)用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加
 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是___________。
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是___________。
| A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应 |
| B.阶段②的压强变小,该过程发生了氧化还原反应 |
C.阶段③发生反应的离子方程式为: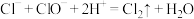 |
D.若将 换成 换成 ,所得的压强变化趋势与图2相似 ,所得的压强变化趋势与图2相似 |
您最近一年使用:0次
名校
解题方法
8 . 已知三氯化铁的熔点为:306℃,沸点为315℃,易溶于水并且有强烈的吸水性,吸收空气里的水分而潮解,某学习小组对氯气与铁的反应及产物做了如下探究实验。
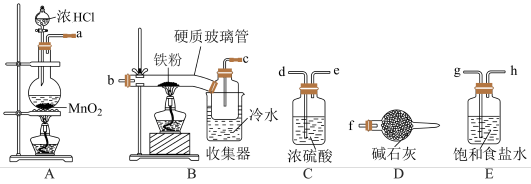
(1)图中装有MnO2的仪器名称为___________ ,A中发生反应的离子方程式为___________ ;
(2)B中发生反应的化学方程式为___________ ;
(3)为制取纯净的三氯化铁,装置连接顺序为a→___________ (用abcdefgh表示);
(4)D的作用为___________ ;E的作用为___________ ;
(5)B装置中的冷水浴作用是___________ 。

(1)图中装有MnO2的仪器名称为
(2)B中发生反应的化学方程式为
(3)为制取纯净的三氯化铁,装置连接顺序为a→
(4)D的作用为
(5)B装置中的冷水浴作用是
您最近一年使用:0次
9 . 无水氯化铁固体呈棕褐色,易潮解,100 ℃左右时升华,冷却后易凝华。如图是两名学生设计的用氯气与铁反应制备无水氯化铁的实验装置图。左边的反应装置相同,而右边的产品收集装置则不同,分别如(I)和(Ⅱ)所示。试回答:

(1)实验前,需进行的操作是___________ ;B仪器的名称是___________ 。
(2)B中反应的化学方程式为___________ 。
(3)下列说法不正确 的是___________。
(4)装置(I)的主要缺点:___________ 、___________ ;
(5)如果选用(Ⅱ)装置来完成实验,则必须采取的改进措施是___________ 。

(1)实验前,需进行的操作是
(2)B中反应的化学方程式为
(3)下列说法
| A.C装置的目的是防止水蒸气进入D中 |
| B.装置(Ⅱ)F中发生反应的离子方程式为Cl2+2OH-=ClO-+Cl-+H2O |
| C.用50mL 12 mol·L-1的浓盐酸与足量的MnO2反应,所得氯气可以制取16.25g FeCl3 |
| D.实验中应先点燃B处的酒精灯,再立刻点燃D处的酒精灯 |
(4)装置(I)的主要缺点:
(5)如果选用(Ⅱ)装置来完成实验,则必须采取的改进措施是
您最近一年使用:0次
10 . 某实验小组使用 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:

(1)实验室常用二氧化锰与浓盐酸制取氯气写出该反应的化学方程式:___________ 。
(2)在实验过程中,装置C的作用为___________ ,装置D中观察到的现象是___________ 。
(3)小组成员观察到装置E中的现象:___________ ,根据实验现象小明同学设计了如下图的实验研究氯气是否具有漂白性。已知通入的氯气中含有空气和水蒸气,浓硫酸用于吸收氯气中的水蒸气。回答下列问题:
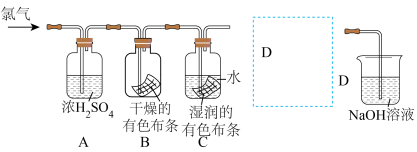
①实验现象:B中布条___________ ,C中布条___________ (填“褪色”或“不褪色”),写出相关的化学方程式:___________ 。
②写出D中反应的离子方程式:___________ ,若有标况下22.4L氯气与500mLNaOH溶液恰好完全反应,则NaOH溶液中溶质的物质的量浓度为___________ 。
(4)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应氧化剂是___________ (写化学式)。
 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:
(1)实验室常用二氧化锰与浓盐酸制取氯气写出该反应的化学方程式:
(2)在实验过程中,装置C的作用为
(3)小组成员观察到装置E中的现象:

①实验现象:B中布条
②写出D中反应的离子方程式:
(4)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应氧化剂是
您最近一年使用:0次



