名校
1 . Ⅰ.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成都有着重要的应用。
(1)NaClO中Cl的化合价为___________ ,有较强的___________ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式___________ 。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO ,此反应的离子方程式
,此反应的离子方程式___________ 。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ.某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:

(3)另一种制氯气的方法是用固体高锰酸钾与浓盐酸,在常温条件下制取氯气,写出化学反应方程式___________ ;
(4)C装置的作用是___________ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是___________ 。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,可将装置如何改进___________ 。
(1)NaClO中Cl的化合价为
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO
 ,此反应的离子方程式
,此反应的离子方程式②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:

(3)另一种制氯气的方法是用固体高锰酸钾与浓盐酸,在常温条件下制取氯气,写出化学反应方程式
(4)C装置的作用是
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,可将装置如何改进
您最近一年使用:0次
名校
解题方法
2 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I2的一种制备方法如下图所示:
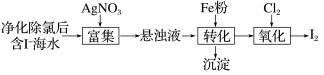
①加入Fe粉进行转化反应是一个置换反应,该反应的化学方程式为___________ ,生成的沉淀与硝酸反应,生成___________ 后可循环使用。
②通入Cl2的过程中,若氧化产物只有一种,反应的的离子方程式为___________ ;当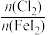 >1.5后,单质碘的收率会降低,原因是
>1.5后,单质碘的收率会降低,原因是___________ 。
(2)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为___________ mol。I2在KI溶液中可发生反应:I2+I- 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是___________ 。
(1)I2的一种制备方法如下图所示:

①加入Fe粉进行转化反应是一个置换反应,该反应的化学方程式为
②通入Cl2的过程中,若氧化产物只有一种,反应的的离子方程式为
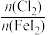 >1.5后,单质碘的收率会降低,原因是
>1.5后,单质碘的收率会降低,原因是(2)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为
 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
您最近一年使用:0次
3 . 某学生应用如图所示的装置来研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
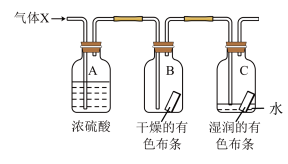
(1)该项研究(实验)的主要目的是_______ 。
(2)与研究目的直接相关的实验现象是_______ 。
(3)从绿色化学的角度分析,上述实验装置图中存在一处缺陷,改正的方法是加一个尾气处理装置,该装置发生反应的化学方程式为_______ 。
(4)漂白粉是用Cl2与石灰乳反应来制取的,制取反应的化学方程式为_______ 。漂白粉在空气中久置失效的原因(用化学方程式表示)_______ 。
(5)实验完毕后,将C中的水溶液(呈黄绿色)取出,分别加入两支试管中,进行如下实验:
(6)Cl2O7是一种酸酐,它可以与水反应生成相应的酸,写出该方程式_______ 。

(1)该项研究(实验)的主要目的是
(2)与研究目的直接相关的实验现象是
(3)从绿色化学的角度分析,上述实验装置图中存在一处缺陷,改正的方法是加一个尾气处理装置,该装置发生反应的化学方程式为
(4)漂白粉是用Cl2与石灰乳反应来制取的,制取反应的化学方程式为
(5)实验完毕后,将C中的水溶液(呈黄绿色)取出,分别加入两支试管中,进行如下实验:
| 实验编号 | 滴加的试剂 | 实验现象 | 证明存在的微粒 (填微粒符号) |
| A | AgNO3溶液 | ||
| B | 紫色石蕊溶液 |
(6)Cl2O7是一种酸酐,它可以与水反应生成相应的酸,写出该方程式
您最近一年使用:0次
4 . NaCl是一种化工原料,可以制备多种物质,如下图所示。请根据该转化关系填写下列空白。
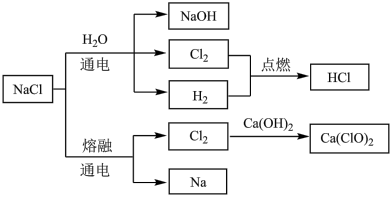
(1)氯化钠溶液通电后,发生反应的离子方程式为_________________________________ ,
氢气在氯气中燃烧的现象是:___________________________________________ 。
(2)在常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液。该反应的离子方程式为___________________________ ;该漂白液的有效成分是___________ (填名称)。
(3)漂白粉或漂粉精中的Ca(ClO)2能与空气中的CO2和水蒸气发生反应而进行漂白,请写出反应的化学方程式:________________________________________________________ 。
(4)检验某溶液中是否含有Cl-的方法是_________________________________________ 。

(1)氯化钠溶液通电后,发生反应的离子方程式为
氢气在氯气中燃烧的现象是:
(2)在常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液。该反应的离子方程式为
(3)漂白粉或漂粉精中的Ca(ClO)2能与空气中的CO2和水蒸气发生反应而进行漂白,请写出反应的化学方程式:
(4)检验某溶液中是否含有Cl-的方法是
您最近一年使用:0次
5 . 某研究性学习小组设计了如图所示的实验,以此来验证氯、溴、碘三种卤素单质的氧化性顺序。图中A、B、C分别是浸有饱和溴化钠溶液、饱和碘化钾溶液、冷水的棉球,烧杯D中盛有氢氧化钠溶液。实验时,打开止水夹从左端导管口缓慢通入氯气片刻,关闭止水夹停通氯气再对B棉球进行加热。
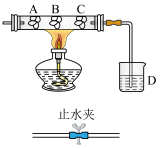
导管右侧插入玻璃管左侧橡胶塞
请利用下表提供的信息,结合所学知识,完成下列问题:
(1)棉球A的现象:_______ 。
(2)棉球B上反应的离子方程式:_______ 。
(3)棉球C的现象:_______ 。
(4)氢氧化钠溶液的作用是_______ ,写出其中一反应的离子方程式:_______ 。
(5)由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:_______ 、_______ 。

导管右侧插入玻璃管左侧橡胶塞
请利用下表提供的信息,结合所学知识,完成下列问题:
| 卤素单质 | 颜色和状态 | 蒸气颜色 | 在水中的溶解度 | 水溶液的颜色 | 熔点/℃ | 沸点/℃ |
 | 黄绿色气体 | / | 在一定量水中溶解的溶质的物质的量逐渐减少 | 淡黄绿色 |  |  |
 | 深红棕色液体 | 红棕色 | 橙色 |  | 58.78 | |
 | 紫黑色固体 | 紫色 | 黄褐色 | 113.5 | 184.4 |
(1)棉球A的现象:
(2)棉球B上反应的离子方程式:
(3)棉球C的现象:
(4)氢氧化钠溶液的作用是
(5)由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:
您最近一年使用:0次
6 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
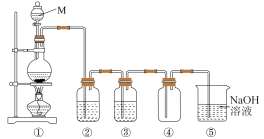
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
名校
解题方法
7 .  作为一种广泛的消毒剂,它易溶于水而难溶于有机溶剂,实验室用
作为一种广泛的消毒剂,它易溶于水而难溶于有机溶剂,实验室用 与
与 反应制得
反应制得 和NaCl。如图是实验室用于制备和收集一定量纯净的
和NaCl。如图是实验室用于制备和收集一定量纯净的 的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
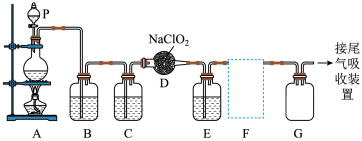
(1)仪器P的名称是__________ 。
(2)请写出装置A中烧瓶内发生反应的化学方程式:______________________________ ,每转移1mol电子时,产生标准状况下
__________ L。
(3)B、C装置中所盛试剂分别是__________ 、__________ 。
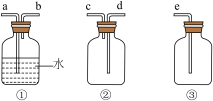
(4)F为 收集装置,应选用如图的哪组装置来收集
收集装置,应选用如图的哪组装置来收集__________ (填序号),其中与装置E导管相连的导管口是__________ (填接口字母)。
(5)装置D中发生反应的化学方程式为______ 。
(6)将 通入冷的石灰乳中即制得漂白粉,请写出该反应的化学方程式
通入冷的石灰乳中即制得漂白粉,请写出该反应的化学方程式______________________________ ,漂白粉在使用时会与空气中 反应,
反应, 为
为__________ (填“酸性氧化物”或“碱性氧化物”)。
 作为一种广泛的消毒剂,它易溶于水而难溶于有机溶剂,实验室用
作为一种广泛的消毒剂,它易溶于水而难溶于有机溶剂,实验室用 与
与 反应制得
反应制得 和NaCl。如图是实验室用于制备和收集一定量纯净的
和NaCl。如图是实验室用于制备和收集一定量纯净的 的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。

(1)仪器P的名称是
(2)请写出装置A中烧瓶内发生反应的化学方程式:

(3)B、C装置中所盛试剂分别是
(4)F为
 收集装置,应选用如图的哪组装置来收集
收集装置,应选用如图的哪组装置来收集(5)装置D中发生反应的化学方程式为
(6)将
 通入冷的石灰乳中即制得漂白粉,请写出该反应的化学方程式
通入冷的石灰乳中即制得漂白粉,请写出该反应的化学方程式 反应,
反应, 为
为
您最近一年使用:0次
名校
8 . 下图是化学实验室浓盐酸试剂标签上的部分内容。
(1)写出工业上制 的化学方程式
的化学方程式___________ ,在实验室中进行该反应,现象是___________ 。
(2)该盐酸的物质的量浓度为___________ 。
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸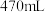 ,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
①配制稀盐酸时,选择的仪器有:___________ (填序号),还缺少的仪器有___________ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为___________  。
。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是___________ (填序号)。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
B.转移溶液后,未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
| 盐酸 分子式:  相对分子质量:36.5 密度约   的质量分数:36.5% 的质量分数:36.5% |
 的化学方程式
的化学方程式(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸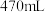 ,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为 。
。③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
B.转移溶液后,未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近一年使用:0次
解题方法
9 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。

(1)若A为化合物,且焰色试验为黄色,回答下列问题:
①A与 反应的离子方程式为
反应的离子方程式为___________ 。
②若X为一种温室气体,用C溶液与X反应制得的D中常含E杂质,可先将C溶液分成两等份,再通过两步操作避免这个问题,试写出这两步操作对应的离子方程式:___________ 、___________ 。
(2)若A为一种黄绿色气体,则:
①若B的溶液有漂白性,它是___________ (写名称)。
②常温下,A通至冷的石灰乳反应可制得漂白粉,可用于棉、麻、纸张的漂白,用化学方程式表示漂白粉的制备原理:___________ 。
③漂白粉的保存要注意密封,为了判断一份久置的漂白粉是I.没有变质 II.部分变质III.完全变质。某化学兴趣小组设计实验进行验证。
已知: 溶液呈碱性:
溶液呈碱性: ;
;
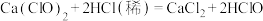 。
。
a.甲同学取适量该漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此判断结论为I,乙同学不同意这一观点,你认为的结论是___________ 。
A.II B.III C.I或II D.I、II、III均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又用pH试纸进一步检验后得出的结论是II,其操作及现象是___________ 。

(1)若A为化合物,且焰色试验为黄色,回答下列问题:
①A与
 反应的离子方程式为
反应的离子方程式为②若X为一种温室气体,用C溶液与X反应制得的D中常含E杂质,可先将C溶液分成两等份,再通过两步操作避免这个问题,试写出这两步操作对应的离子方程式:
(2)若A为一种黄绿色气体,则:
①若B的溶液有漂白性,它是
②常温下,A通至冷的石灰乳反应可制得漂白粉,可用于棉、麻、纸张的漂白,用化学方程式表示漂白粉的制备原理:
③漂白粉的保存要注意密封,为了判断一份久置的漂白粉是I.没有变质 II.部分变质III.完全变质。某化学兴趣小组设计实验进行验证。
已知:
 溶液呈碱性:
溶液呈碱性: ;
;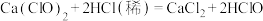 。
。a.甲同学取适量该漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此判断结论为I,乙同学不同意这一观点,你认为的结论是
A.II B.III C.I或II D.I、II、III均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又用pH试纸进一步检验后得出的结论是II,其操作及现象是
您最近一年使用:0次
10 . 按要求回答下列问题:
Ⅰ.实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
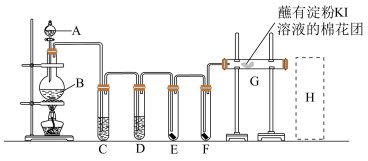
(1)写出实验室制备氯气反应的离子方程式:_________________ 。
(2)C中溶液为_________ ,D中放入浓H2SO4的目的是_________ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是:_________ ,对比E和F中现象的差异可得出的结论是_________ 。
(4)用化学方程式写出H处尾气吸收装置中的反应原理:_________ 。
Ⅱ.家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
(5)消毒液与洁厕灵不能同时使用,否则会产生有毒气体引起中毒,原因是(用离子方程式表示)_________ 。
Ⅰ.实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)写出实验室制备氯气反应的离子方程式:
(2)C中溶液为
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是:
(4)用化学方程式写出H处尾气吸收装置中的反应原理:
Ⅱ.家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
| 注意事项: 1.本品对棉织品有漂白脱白作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年。 |
(5)消毒液与洁厕灵不能同时使用,否则会产生有毒气体引起中毒,原因是(用离子方程式表示)
您最近一年使用:0次



