名校
解题方法
1 . 化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置I中仪器c的名称是___________ 。
(2)实验结束后,同学们在装置Ⅲ中观察到 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的___________ (填序号)装置。
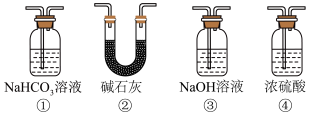
(3)若产生的 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是___________ 。
(4)写出装置V中发生反应的离子方程式___________ 。
(5)将制得的氯气通入如图装置可制备无水 ,已知
,已知 在
在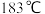 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。

①实验开始时应先___________ (填“通入氯气”或“点燃酒精灯”)。
②用粗短导管连接A、B的目的是___________ 。C中碱石灰的作用是___________ 。
③若制备氯气时消耗 为
为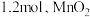 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为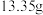 ,则该实验中
,则该实验中 的产率为
的产率为___________ ( )。
)。
(6)若将 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置I中仪器c的名称是
(2)实验结束后,同学们在装置Ⅲ中观察到
 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
(3)若产生的
 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是(4)写出装置V中发生反应的离子方程式
(5)将制得的氯气通入如图装置可制备无水
 ,已知
,已知 在
在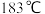 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。
①实验开始时应先
②用粗短导管连接A、B的目的是
③若制备氯气时消耗
 为
为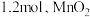 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为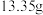 ,则该实验中
,则该实验中 的产率为
的产率为 )。
)。(6)若将
 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为
您最近一年使用:0次
名校
2 . 某同学用以下装置制备并检验 的性质。按要求回答问题。
的性质。按要求回答问题。
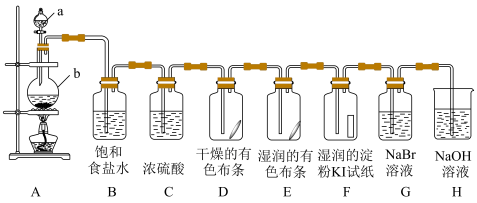
(1)a中加入浓盐酸、b中加入 ,A中制备氯气的化学反应方程式为:
,A中制备氯气的化学反应方程式为:__________ 。
(2)若用含有 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得
,制得 的物质的量总是小于
的物质的量总是小于 的原因是
的原因是__________ 、__________ 。
(3)①装置D和E中现象不同,说明具有漂白性的物质是__________ 。(写化学式)
②装置F中可观察到的现象是_____________________________ 。
③实验结束后,取装置G中少许溶液于试管中,加入苯,充分振荡、静置,观察到的现象是__________ 。
④装置H中发生反应的化学方程式为_______________________ 。
 的性质。按要求回答问题。
的性质。按要求回答问题。
(1)a中加入浓盐酸、b中加入
 ,A中制备氯气的化学反应方程式为:
,A中制备氯气的化学反应方程式为:(2)若用含有
 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得
,制得 的物质的量总是小于
的物质的量总是小于 的原因是
的原因是(3)①装置D和E中现象不同,说明具有漂白性的物质是
②装置F中可观察到的现象是
③实验结束后,取装置G中少许溶液于试管中,加入苯,充分振荡、静置,观察到的现象是
④装置H中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 如图是制取干燥纯净的 Cl2 并探究其化学性质的装置图(已知:I2 遇淀粉变蓝)。
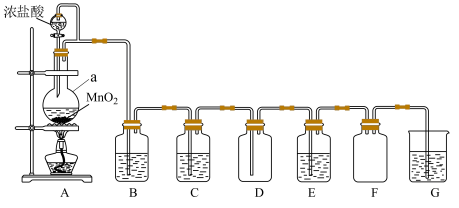
(1)仪器 a 的名称为_______ ,其中发生反应的化学方程式为_______ , 氧化剂与还原剂之比为_______ 。
(2)B 中应盛放的试剂是_______ ;C 的作用是_______ ;F 的作用是_______ 。
(3)E 中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是_______ 。
(4)G 中发生反应的离子方程式为_______ 。

(1)仪器 a 的名称为
(2)B 中应盛放的试剂是
(3)E 中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是
(4)G 中发生反应的离子方程式为
您最近一年使用:0次
4 . 如图是制取干燥纯净的Cl2并探究其化学性质的装置图(已知:I2遇淀粉变蓝)。
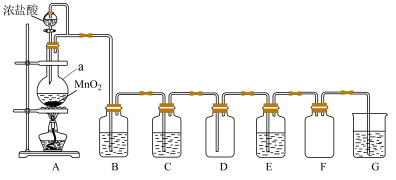
(1)仪器a的名称为___________ ,其中发生反应的离子方程式为___________ 。
(2)装置B中盛放的试剂是___________ (填名称);装置C的作用是___________ ,装置F的作用是___________ 。
(3)装置E中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是(用化学方程式解释)___________ 。
(4)装置G中发生反应的化学方程式为___________ 。

(1)仪器a的名称为
(2)装置B中盛放的试剂是
(3)装置E中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是(用化学方程式解释)
(4)装置G中发生反应的化学方程式为
您最近一年使用:0次
5 . 实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。
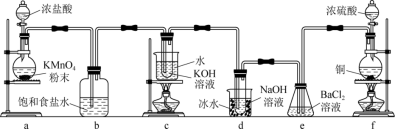
图中a为氯气发生装置,c的试管中盛有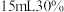 的
的 溶液,并置于热水浴中,d的试管中盛有
溶液,并置于热水浴中,d的试管中盛有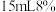 的
的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。
(1)制取 时,在烧瓶中先加入一定量的
时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过___________ (填写仪器名称)向烧瓶中加入适量的浓盐酸。若反应中转移的电子物质的量为 ,则在标准状况下产生的
,则在标准状况下产生的 的体积为
的体积为___________ 。
(2)比较制取氯酸钾和次氯酸钠的条件,两者的差异是___________ 。
(3)将d中余气与f中产生的气体通入e中,产生的现象是___________ ,请用化学方程式表示产生此现象的原因:___________ 、___________ 。
(4)该实验有一处明显的缺点是___________ 。而工业上为了变废为宝,可用多种方式处理硫酸工业排出的尾气(主要含 ),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:___________ 。

图中a为氯气发生装置,c的试管中盛有
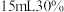 的
的 溶液,并置于热水浴中,d的试管中盛有
溶液,并置于热水浴中,d的试管中盛有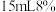 的
的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。(1)制取
 时,在烧瓶中先加入一定量的
时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过 ,则在标准状况下产生的
,则在标准状况下产生的 的体积为
的体积为(2)比较制取氯酸钾和次氯酸钠的条件,两者的差异是
(3)将d中余气与f中产生的气体通入e中,产生的现象是
(4)该实验有一处明显的缺点是
 ),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
),其中一种便是用氨水来吸收。写出用过量氨水吸收尾气的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 下列物质之间有如下反应关系,已知E在空气里可以转化成C。
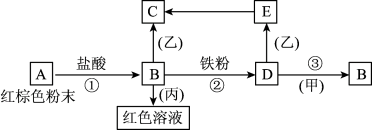
(1)写出下列物质的化学式:A___________ ;D___________ ;甲___________ ;丙___________ ;
(2)写出E→C的化学反应方程式:___________ 。写出D→B的离子反应方程式:___________ 。
(3)E在空气里转化成C的现象是___________ 。

(1)写出下列物质的化学式:A
(2)写出E→C的化学反应方程式:
(3)E在空气里转化成C的现象是
您最近一年使用:0次
7 . 氯及其化合物在日常生活中有广泛应用。某实验小组设计多组实验,对氯气及氯的化合物的性质进行研究
I.氯气的制备与性质研究
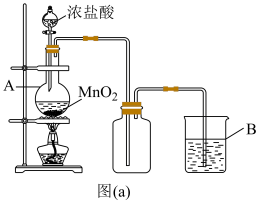
(1)实验室中常用如图(a)所示的装置制备氯气,反应的化学方程式为___________ 。
(2)图中仪器A的名称是___________ 。
(3)装置B内的溶液可以是___________ 。
(4)实验室中常用图(b)所示的装置制备氯气,并同时得到较浓的烧碱溶液。
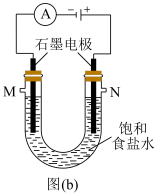
①图(b)反应的化学方程式为___________ 。
②检验制得的烧碱溶液中是否含有NaCl的实验方法是___________ 。
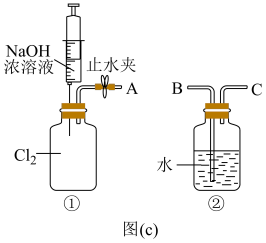
③用图(c)所示的组合装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有___________ ;若其它操作不变,将A与C连接,②中观察到的现象有___________ 。
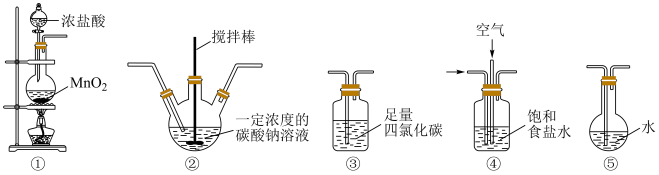
Ⅱ.次氯酸是重要的含氯化合物,应用于杀菌消毒、漂白等领域。学习小组以Cl2O为原料制备HClO。
i.常温常压下Cl2O是一种黄绿色气体
ii.将氯气和空气(不参与反应)通入足量的Na2CO3溶液,发生反应生成Cl2O。
iii.Cl2O易溶于水并与水立即反应生成HClO
iv.已知:HClO+2I-+H+=I2+Cl-+H2O,I2+2 =2I-+
=2I-+
(5)装置③中的液体不可燃、不助燃也不导电,关于其用途正确的是___________。
(6)各装置的连接顺序为___________ 。
①→___________→___________→___________→___________
(7)装置②中发生的化学反应中氧化产物与还原产物的物质的量之比为___________ 。
(8)装置④的作用有___________ 。(至少写出2点)
I.氯气的制备与性质研究

(1)实验室中常用如图(a)所示的装置制备氯气,反应的化学方程式为
(2)图中仪器A的名称是
(3)装置B内的溶液可以是
(4)实验室中常用图(b)所示的装置制备氯气,并同时得到较浓的烧碱溶液。

①图(b)反应的化学方程式为
②检验制得的烧碱溶液中是否含有NaCl的实验方法是
③用图(c)所示的组合装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有

Ⅱ.次氯酸是重要的含氯化合物,应用于杀菌消毒、漂白等领域。学习小组以Cl2O为原料制备HClO。

i.常温常压下Cl2O是一种黄绿色气体
ii.将氯气和空气(不参与反应)通入足量的Na2CO3溶液,发生反应生成Cl2O。
iii.Cl2O易溶于水并与水立即反应生成HClO
iv.已知:HClO+2I-+H+=I2+Cl-+H2O,I2+2
 =2I-+
=2I-+
(5)装置③中的液体不可燃、不助燃也不导电,关于其用途正确的是___________。
| A.可浮于水溶液上方——隔绝空气 | B.与水互不相溶——萃取剂 |
| C.可隔绝空气——灭火剂 | D.遇碘变色——指示剂 |
(6)各装置的连接顺序为
①→___________→___________→___________→___________
(7)装置②中发生的化学反应中氧化产物与还原产物的物质的量之比为
(8)装置④的作用有
您最近一年使用:0次
名校
解题方法
8 . 亚硝酰氯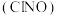 主要用于合成洗涤剂、触媒,也可用作有机合成中间体,遇水易水解生成
主要用于合成洗涤剂、触媒,也可用作有机合成中间体,遇水易水解生成 和
和 。实验室常制备亚硝酰氯的反应为
。实验室常制备亚硝酰氯的反应为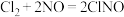 ,设计如图所示装置(部分夹持装置略去)。
,设计如图所示装置(部分夹持装置略去)。
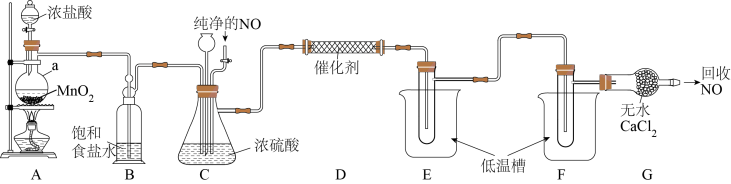
已知:相关物质熔沸点如下:
回答下列问题:
(1)仪器 中反应的离子方程式为
中反应的离子方程式为___________ ,若提供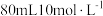 浓盐酸与足量
浓盐酸与足量 充分发生反应,则制得
充分发生反应,则制得 的体积在标准状况下
的体积在标准状况下___________  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(2)装置 具有如下作用:①根据气泡观察气体流速、调节气体比例关系;②除去氯气中混有的水蒸气,还具有的作用是
具有如下作用:①根据气泡观察气体流速、调节气体比例关系;②除去氯气中混有的水蒸气,还具有的作用是________ ,若没有装置 ,则制得产品容易发生的副反应为
,则制得产品容易发生的副反应为__________ 。
(3)一段时间后,装置 中反应结束的现象是
中反应结束的现象是_______ , 控制的温度应低于
控制的温度应低于_________ 。
(4)实验结束后,需改用氮气替换 通入到装置
通入到装置 中一段时间,其目的是
中一段时间,其目的是_________ 。
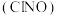 主要用于合成洗涤剂、触媒,也可用作有机合成中间体,遇水易水解生成
主要用于合成洗涤剂、触媒,也可用作有机合成中间体,遇水易水解生成 和
和 。实验室常制备亚硝酰氯的反应为
。实验室常制备亚硝酰氯的反应为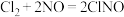 ,设计如图所示装置(部分夹持装置略去)。
,设计如图所示装置(部分夹持装置略去)。
已知:相关物质熔沸点如下:
| 物质化学式 | 熔点/ | 沸点/ |
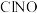 |  | 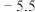 |
 |  | 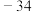 |
 | 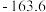 | 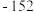 |
(1)仪器
 中反应的离子方程式为
中反应的离子方程式为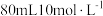 浓盐酸与足量
浓盐酸与足量 充分发生反应,则制得
充分发生反应,则制得 的体积在标准状况下
的体积在标准状况下 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(2)装置
 具有如下作用:①根据气泡观察气体流速、调节气体比例关系;②除去氯气中混有的水蒸气,还具有的作用是
具有如下作用:①根据气泡观察气体流速、调节气体比例关系;②除去氯气中混有的水蒸气,还具有的作用是 ,则制得产品容易发生的副反应为
,则制得产品容易发生的副反应为(3)一段时间后,装置
 中反应结束的现象是
中反应结束的现象是 控制的温度应低于
控制的温度应低于(4)实验结束后,需改用氮气替换
 通入到装置
通入到装置 中一段时间,其目的是
中一段时间,其目的是
您最近一年使用:0次
名校
解题方法
9 . 实验小组对氯气的制备和性质进行探究。
Ⅰ.实验室制备和收集氯气的常用装置如下图。
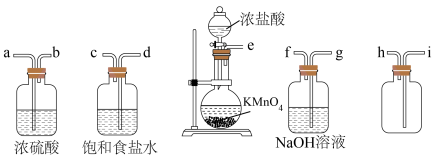
(1)盛放KMnO4固体的仪器名称是___________ 。
(2)实验装置接口的连接顺序为e→____→____→____→____→____→____→g→f,______ 。
(3)在实验过程中饱和食盐水的作用是___________ 。
(4)利用该装置制备氯气的化学方程式为___________ 。
Ⅱ.现利用如下装置进行 的性质探究,并制备家用消毒液(主要成分为
的性质探究,并制备家用消毒液(主要成分为 )。
)。
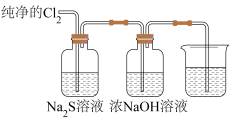
(5)B中出现黄色浑浊现象,产生此现象的离子方程式为________ ,该实验说明了氧化性:
___ S(填“>、<、=”)。
(6)制备家用消毒液的离子方程式为___________ 。
(7)家用消毒液请勿与洁厕灵(主要成分为盐酸)同时使用,否则会产生有毒气体。写出该反应的化学方程式______ 。
Ⅰ.实验室制备和收集氯气的常用装置如下图。

(1)盛放KMnO4固体的仪器名称是
(2)实验装置接口的连接顺序为e→____→____→____→____→____→____→g→f,
(3)在实验过程中饱和食盐水的作用是
(4)利用该装置制备氯气的化学方程式为
Ⅱ.现利用如下装置进行
 的性质探究,并制备家用消毒液(主要成分为
的性质探究,并制备家用消毒液(主要成分为 )。
)。
(5)B中出现黄色浑浊现象,产生此现象的离子方程式为

(6)制备家用消毒液的离子方程式为
(7)家用消毒液请勿与洁厕灵(主要成分为盐酸)同时使用,否则会产生有毒气体。写出该反应的化学方程式
您最近一年使用:0次
名校
10 . “84”消毒液能有效杀灭新型冠状病毒,某同学购买了一瓶“84”消毒液,其说明中有如下信息: 质量分数
质量分数 、密度
、密度 ,稀释后使用。请根据信息和相关知识回答下列问题:
,稀释后使用。请根据信息和相关知识回答下列问题:
(1)该“84”消毒液中 的物质的量浓度为
的物质的量浓度为______  。(保留至小数点后一位)
。(保留至小数点后一位)
(2)现实验室需要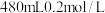 的
的 溶液,某同学用
溶液,某同学用 固体配制该物质的量浓度的溶液。
固体配制该物质的量浓度的溶液。
①应用托盘天平称取 固体
固体______ g。
②配制 溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、
溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、______ 、_____ 。
③实验时遇下列情况,会导致溶液物质的量浓度偏高的是______ 。
A.容量瓶内壁附有水珠而未干燥处理 B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤 D.溶解后没有冷却便进行定容
E.定容时俯视刻度线 F.摇匀后发现液面低于刻度线后未作处理
(3)实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
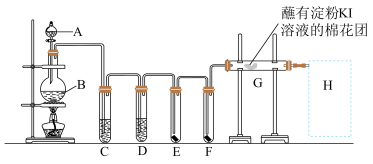
①写出实验室制备氯气反应的离子方程式:______ 。
②C中溶液为______ ,D中放入浓 的目的是
的目的是_______ 。
③E中为红色干布条,F中为红色湿布条,可观察到的现象是______ ,对比E和F中现象的差异可得出的结论是_____ 。
(4)洁厕灵(主要成分盐酸)清洁卫生。"84”消毒液与洁厕灵不能同时使用,否则会产生有毒气体引起中毒,原因是(用离子方程式表示)______ 。
 质量分数
质量分数 、密度
、密度 ,稀释后使用。请根据信息和相关知识回答下列问题:
,稀释后使用。请根据信息和相关知识回答下列问题:(1)该“84”消毒液中
 的物质的量浓度为
的物质的量浓度为 。(保留至小数点后一位)
。(保留至小数点后一位)(2)现实验室需要
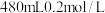 的
的 溶液,某同学用
溶液,某同学用 固体配制该物质的量浓度的溶液。
固体配制该物质的量浓度的溶液。①应用托盘天平称取
 固体
固体②配制
 溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、
溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、③实验时遇下列情况,会导致溶液物质的量浓度偏高的是
A.容量瓶内壁附有水珠而未干燥处理 B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤 D.溶解后没有冷却便进行定容
E.定容时俯视刻度线 F.摇匀后发现液面低于刻度线后未作处理
(3)实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

①写出实验室制备氯气反应的离子方程式:
②C中溶液为
 的目的是
的目的是③E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)洁厕灵(主要成分盐酸)清洁卫生。"84”消毒液与洁厕灵不能同时使用,否则会产生有毒气体引起中毒,原因是(用离子方程式表示)
您最近一年使用:0次



