1 . 实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。

(1)装置A中发生的化学方程式为__________ ,装置B、C中应盛放的试剂名称为__________ 。
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是__________ 。
(3)实验时,先点燃__________ 处的酒精灯,其目的是__________ ,写出D中反应的化学方程式:__________ 。
(4)F装置所起的作用是__________ 和防止空气中的水蒸气进入E中。
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为__________ 。
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:__________ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(1)装置A中发生的化学方程式为
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是
(3)实验时,先点燃
(4)F装置所起的作用是
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:
您最近一年使用:0次
2 . 有关氯气制备的装置如图所示,下列有关说法不正确的是


| A.图中气体通入浓硫酸时导管连接错误,应该是长管进气,短管出气 |
| B.可用饱和碳酸氢钠溶液代替饱和NaCl溶液 |
| C.制备氯气时,二氧化锰做氧化剂 |
| D.图中采用了向上排空气法收集氯气 |
您最近一年使用:0次
2022-09-19更新
|
1028次组卷
|
6卷引用:河南省开封市新世纪高级中学2022-2023学年高一上学期期末考试化学试题
河南省开封市新世纪高级中学2022-2023学年高一上学期期末考试化学试题安徽省宿州北方中学2021-2022学年高一上学期期中考试化学试题(已下线)海水中的重要元素—钠和氯——进阶学习上海市金山中学2022-2023学年高一上学期期中考试化学试题新疆昌吉州行知学校2022-2023学年高一上学期第一次线上月考化学试题(已下线)【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册
3 . 制备物质是化学工作者的重要任务之一,实验室用如图装置制备并收集干燥、纯净的Cl2。
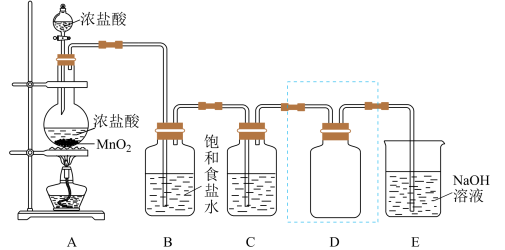
(1)装置A 中发生反应的离子方程式是_______ ,反应中盐酸体现的性质有_______ 。
(2)装置B 的作用是_______ 。
(3)装置C 中盛放的物质是_______ 。
(4)装置D 用于收集Cl2,请将装置D 中的导气管在装置图上补充完整______ (表示气流方向)。
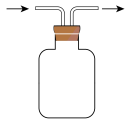
(5)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:_______ 。

(1)装置A 中发生反应的离子方程式是
(2)装置B 的作用是
(3)装置C 中盛放的物质是
(4)装置D 用于收集Cl2,请将装置D 中的导气管在装置图上补充完整

(5)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:
您最近一年使用:0次
2023-09-06更新
|
232次组卷
|
4卷引用:河南省周口市鹿邑县第二高级中学校2023-2024学年高一上学期期中考试化学试卷
河南省周口市鹿邑县第二高级中学校2023-2024学年高一上学期期中考试化学试卷四川省乐山市井研县2023-2024学年高一上学期开学考试化学试题(已下线)【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册陕西省西安市鄠邑区2023-2024学年高一上学期期中质量检测化学试题
4 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图所示装置(部分装置省略)制备 和NaClO。
和NaClO。
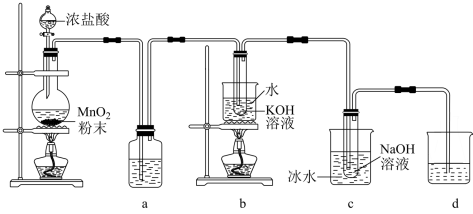
回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是_______ ,其中发生反应的化学方程式为_______ 。
(2)a中的试剂为_______ ,其作用是_______ 。
(3)b中采用的加热方式是_______ ,这样加热的优点有_______ (答两点)。
(4)c中化学反应的离子方程式为_______ ,采用冰水浴冷却的目的是_______ 。
(5)d的作用是_______ 。反应结束后,取出b中试管,经冷却结晶,_______ ,_______ ,干燥,得到 晶体。
晶体。
 和NaClO。
和NaClO。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)a中的试剂为
(3)b中采用的加热方式是
(4)c中化学反应的离子方程式为
(5)d的作用是
 晶体。
晶体。
您最近一年使用:0次
名校
解题方法
5 . 瑞典化学家舍勒是最早发现氯气的人,他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气,装置如图所示,化学反应方程式为: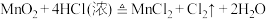
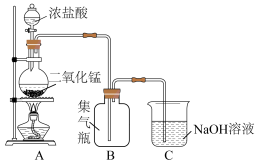
回答下列问题:
(1)实验室制取 的反应中,浓盐酸表现
的反应中,浓盐酸表现_________ (填“氧化性”、“还原性”或“酸性”)。
(2)请用单线桥表示该反应中电子转移的方向和数目_________ 。
(3)标况下,若生成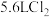 ,则转移电子的数目为
,则转移电子的数目为_________ 。
(4)装置C可吸收多余的 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式_________ 。所用 溶液一般为
溶液一般为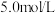 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、_________ 。
(5) 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是_________ 。
(6)装置C中也可能生成 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式_________ 。
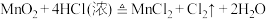

回答下列问题:
(1)实验室制取
 的反应中,浓盐酸表现
的反应中,浓盐酸表现(2)请用单线桥表示该反应中电子转移的方向和数目
(3)标况下,若生成
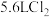 ,则转移电子的数目为
,则转移电子的数目为(4)装置C可吸收多余的
 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式 溶液一般为
溶液一般为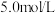 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、(5)
 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是(6)装置C中也可能生成
 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式
您最近一年使用:0次
名校
解题方法
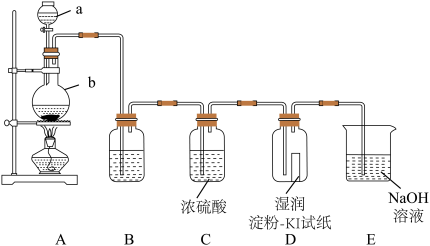
6 . Ⅰ.某研究性学习小组用如图装置制备氯气并对氯气及其化合物的性质进行实验探究。
完成下列填空:
(1)请指出仪器a的名称_______ ,装置A中发生的反应化学方程式是_______
(2)装置B中盛放_______ ,浓硫酸的作用是_______
(3)装置D中的现象是_______ ,反应的离子方程式是_______ 。
(4)装置E中发生的反应是(用离子方程式表示)_______
Ⅱ.实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,
(5)该反应中HCl的作用是_______ ,若反应产生0.5molCl2,则消耗的氧化剂的物质的量为_______ mol,反应转移的电子数是_______ 。

完成下列填空:
(1)请指出仪器a的名称
(2)装置B中盛放
(3)装置D中的现象是
(4)装置E中发生的反应是(用离子方程式表示)
Ⅱ.实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,
(5)该反应中HCl的作用是
您最近一年使用:0次
7 . 在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去)。图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15 mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液。

(1)③试管中制取次氯酸钠的化学方程式为__________________________________
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格。
(3)此实验有一个明显的不足之处,应如何改进?__________________________________

(1)③试管中制取次氯酸钠的化学方程式为
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格。
| 实验现象 | 原因 |
| 溶液最初从紫色变为 | 氯气与水反应生成的HCl使石蕊试液变红 |
| 随后溶液逐渐变为无色 | |
| 最后溶液从无色逐渐变为 |
(3)此实验有一个明显的不足之处,应如何改进?
您最近一年使用:0次
名校
8 .  是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
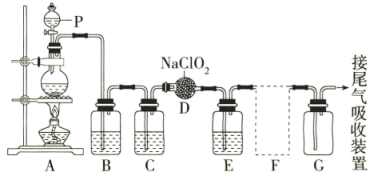
(1)仪器P的名称是________ 。
(2)请写出装置A中烧瓶内发生反应的化学方程式:__________ 。
(3)装置B、C中所盛试剂分别是________ 、__________ 。
(4)F为 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集_______ (填序号),其中与装置E导管相连的导管口是______ (填接口字母)。
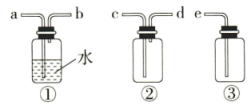
(5)装置D中发生反应的化学方程式为________ 。
(6) 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应:________ 。将 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为_______ (填“酸性氧化物”或“碱性氧化物”)。
 是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
(1)仪器P的名称是
(2)请写出装置A中烧瓶内发生反应的化学方程式:
(3)装置B、C中所盛试剂分别是
(4)F为
 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集
(5)装置D中发生反应的化学方程式为
(6)
 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应: 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为
您最近一年使用:0次
2022-08-17更新
|
290次组卷
|
2卷引用:河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题
名校
9 . 实验小组制备高铁酸钾 并探究其性质。
并探究其性质。
资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
I.制备 (夹持装置略)
(夹持装置略)
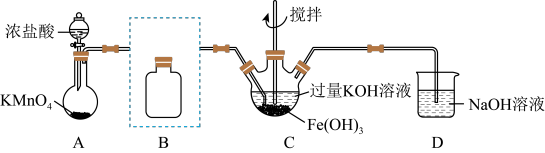
(1)A为氯气发生装置。 中反应的离子方程式是
中反应的离子方程式是_______
(2)B装置盛有饱和 溶液,
溶液, 中得到紫色固体和溶液。
中得到紫色固体和溶液。 中制备高铁酸钾的化学反应方程式为
中制备高铁酸钾的化学反应方程式为_______
II.探究 的性质
的性质
(3)取 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。
。
为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
由方案Ⅰ可知 中含有
中含有 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由_______ 产生,(用离子方程式表示)。
(4)根据 的制备实验得出:氧化性
的制备实验得出:氧化性
_______  (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是_______ 。
 并探究其性质。
并探究其性质。资料:
 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。I.制备
 (夹持装置略)
(夹持装置略)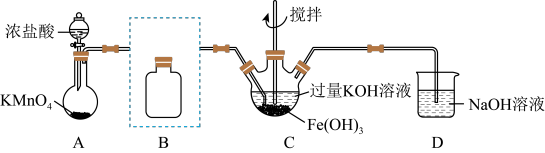
(1)A为氯气发生装置。
 中反应的离子方程式是
中反应的离子方程式是(2)B装置盛有饱和
 溶液,
溶液, 中得到紫色固体和溶液。
中得到紫色固体和溶液。 中制备高铁酸钾的化学反应方程式为
中制备高铁酸钾的化学反应方程式为II.探究
 的性质
的性质(3)取
 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。
。为证明是否
 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:| 方案Ⅰ | 取少量a,经过检验溶液中含有 。 。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 溶出,得到紫色溶液b。取少量b,滴加盐酸,有 溶出,得到紫色溶液b。取少量b,滴加盐酸,有 产生。 产生。 |
 中含有
中含有 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由(4)根据
 的制备实验得出:氧化性
的制备实验得出:氧化性
 (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是
您最近一年使用:0次
2023-01-22更新
|
584次组卷
|
3卷引用:河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题
名校
10 . 实验室可用如图装置制备无水FeCl3。已知FeCl3易升华,易吸收水分而潮解。请回答下列问题:_______ 。
(2)装置A盛放浓盐酸的仪器名称是_______ ,其上口与烧瓶用导管相连的作用是_______ 。
(3)A装置中发生反应的离子方程式为_______ 。当加入一定量的浓盐酸与足量MnO2反应,实际生成的Cl2体积小于理论值的原因是_______ 。
(4)装置B的作用是_______ ,G中发生反应的离子方程式为_______ 。
(5)F中所装试剂为_______ ,目的是_______ 。

(2)装置A盛放浓盐酸的仪器名称是
(3)A装置中发生反应的离子方程式为
(4)装置B的作用是
(5)F中所装试剂为
您最近一年使用:0次
2023-05-05更新
|
525次组卷
|
6卷引用:河南省平顶山市第二中学2023-2024学年高一上学期期末化学试题



