名校
1 . 新冠肺炎使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。图为84消毒液说明书,请回答下列问题。
(1)①洁厕剂主要成分为稀盐酸,用化学方程式解释注意事项中“不可与洁厕剂混合使用”的原因 _______ 。
②Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉或84消毒液,主要目的_______ 。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.提高氯的质量分数,有利于漂白、消毒
(2)某小组在实验室制备84消毒液,并进行性质探究。
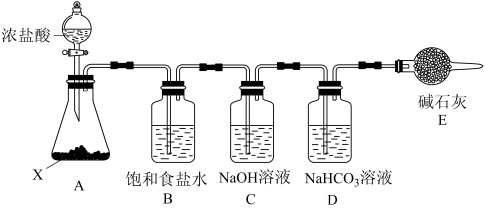
①装置 的名称是
的名称是_______ 。
②能否撤去装置B并说明理由_______ 。
③已知酸性:H2CO3>HClO>HCO ,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式
,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式_______ 。
(3)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25 g/L计算,该消毒液的NaClO的物质的量浓度是_______ mol·L-1。
| 84消毒液说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00 g/L~60.00 g/L | |
| 注意事项 | 不可与洁厕剂或其他消毒液混合使用 | |
| 用法用量 | 稀释后洗刷白色衣物、浴缸等1:200水溶液,餐饮具,瓜果等1:100水溶液 |
②Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉或84消毒液,主要目的
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.提高氯的质量分数,有利于漂白、消毒
(2)某小组在实验室制备84消毒液,并进行性质探究。

①装置
 的名称是
的名称是②能否撤去装置B并说明理由
③已知酸性:H2CO3>HClO>HCO
 ,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式
,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式(3)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25 g/L计算,该消毒液的NaClO的物质的量浓度是
您最近一年使用:0次
2 . 以Cl2、NaOH、CO(NH2)2 (尿素)和SO2为原料可制备N2H4∙H2O (水合肼)和无水Na2SO3,NaHSO3水溶液中含硫微粒随 的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
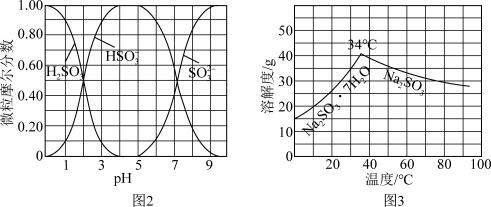
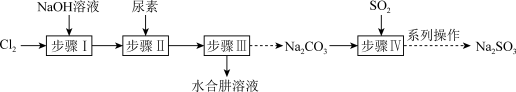
已知:
①Cl2+2OH-=Cl-+ClO-+H2O是放热反应,超过40℃发生副反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ用Cl2通入NaOH溶液制备NaClO溶液,Cl2需要缓慢通入的原因:_________________
(2)步骤Ⅱ合成N2H4∙H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应,使用冷凝管和迅速升温的目的分别是:__________

(3)关于实验操作下列说法正确的是______________。
(4)请补充完整由NaHSO3溶液制备较纯的无水Na2SO3的实验方案:
边搅拌边向NaHSO3溶液中滴加NaOH溶液→_______ →_______ →_______ 用少量无水乙醇洗涤、干燥,包装。
a.调节 至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
e.蒸发浓缩至有晶膜产生,冷却结晶 f.调节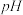 至7
至7
(5)①经某学习小组测定,Na2SO3中含有NaCl杂质,试分析杂质产生的原因:________
②产品的纯度是产品质量的重要指标,该小组同学利用cmol/L的KMnO4测定产品中Na2SO3的含量,装置如图,当酸性KMnO4与Na2SO3恰好完全反应时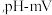 计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化
计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化 ):
):
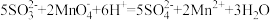
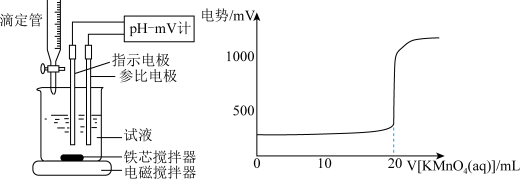
具体流程如下:称量ag样品,加入煮沸后冷却的蒸馏水溶解,配制为250mL的溶液,用碱式滴定管取25.00mL样品溶液于烧杯中,用cmol/L的KMnO4滴定,滴定曲线如图。则样品中Na2SO3纯度的表达式为:________________
 的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:
的分布曲线如图2所示,Na2SO3的溶解度曲线如图3所示)其主要实验流程如下:

已知:
①Cl2+2OH-=Cl-+ClO-+H2O是放热反应,超过40℃发生副反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ用Cl2通入NaOH溶液制备NaClO溶液,Cl2需要缓慢通入的原因:
(2)步骤Ⅱ合成N2H4∙H2O的装置如图1所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应,使用冷凝管和迅速升温的目的分别是:

(3)关于实验操作下列说法正确的是______________。
| A.步骤Ⅱ中通过滴液漏斗滴加NaClO溶液 |
| B.步骤Ⅲ为了得到较高浓度的水合肼,可以向水合肼溶液中加入NaOH,减压蒸馏 |
| C.步骤Ⅳ中边搅拌边向Na2CO3溶液中通入SO2至pH约为4时,即可以停止通入SO2 |
| D.为了快速得到无水Na2CO3,可以将产品烘干 |
边搅拌边向NaHSO3溶液中滴加NaOH溶液→
a.调节
 至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出
至10 b.减压抽滤 c.趁热过滤 d.蒸发浓缩至有大量晶体析出e.蒸发浓缩至有晶膜产生,冷却结晶 f.调节
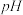 至7
至7(5)①经某学习小组测定,Na2SO3中含有NaCl杂质,试分析杂质产生的原因:
②产品的纯度是产品质量的重要指标,该小组同学利用cmol/L的KMnO4测定产品中Na2SO3的含量,装置如图,当酸性KMnO4与Na2SO3恰好完全反应时
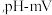 计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化
计测得的的电极电势将会迅速增加,KMnO4与Na2SO3反应方程式为(该条件下KMnO4不氧化 ):
):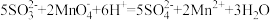

具体流程如下:称量ag样品,加入煮沸后冷却的蒸馏水溶解,配制为250mL的溶液,用碱式滴定管取25.00mL样品溶液于烧杯中,用cmol/L的KMnO4滴定,滴定曲线如图。则样品中Na2SO3纯度的表达式为:
您最近一年使用:0次
3 . 某同学利用如图装置制备一定量的KClO3并探究氯气的某些性质,下列有关说法中错误的是
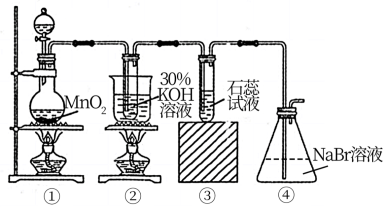

| A.若②中有0.1 mol KClO3生成,理论上应有0.5 mol KCl生成 |
| B.若④中溶液显橙色,则可证明Cl2的氧化性强于Br2 |
| C.若③中溶液先变红后褪色,则说明氯气有酸性、漂白性 |
| D.该套装置在实验中会造成空气污染 |
您最近一年使用:0次
名校
解题方法
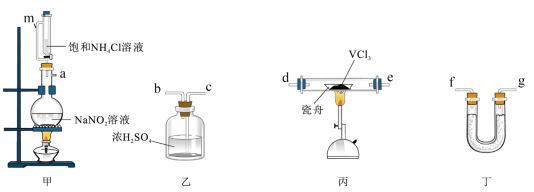
4 . 二氯化钒( )是重要的有机合成试剂,具有较强的吸湿性。某学习小组通过
)是重要的有机合成试剂,具有较强的吸湿性。某学习小组通过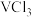 分解制备
分解制备 ,下列说法错误的是
,下列说法错误的是
 )是重要的有机合成试剂,具有较强的吸湿性。某学习小组通过
)是重要的有机合成试剂,具有较强的吸湿性。某学习小组通过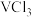 分解制备
分解制备 ,下列说法错误的是
,下列说法错误的是
| A.玻璃管m的作用为:平衡气压,使液体顺利流下 |
B.甲装置中每产生1mol  ,转移电子数目为3 ,转移电子数目为3 |
C.装置合理的连接顺序为: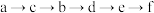 |
D.丁中的试剂可以为无水 |
您最近一年使用:0次
2021-09-06更新
|
520次组卷
|
4卷引用:重庆市第八中学校2022届高三上学期入学摸底测试化学试题
重庆市第八中学校2022届高三上学期入学摸底测试化学试题江苏省海安市南莫中学2022届高三上学期第一次月考备考金卷B卷化学试题(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题25 化学实验综合性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
5 . 氯酸钾及氯水均具有较强的氧化性,实验室中可利用下图装置制备 和较高浓度的氯水。
和较高浓度的氯水。

(1)装置B用于除去HCl,则试剂X是_______ ;实验中应先点燃_______ (填“A“或“C”)处酒精灯。整套装置有一个缺陷,改进的方法是_______ 。
(2)写出装置C中发生反应的离子方程式:_______ 。
(3)取装置D中得到的氯水放入试管中,然后向试管中滴加几滴紫色石蕊试液,可观察到的现象是_______ 。
(4)装置D中 与水的反应可表示为
与水的反应可表示为 ,若试剂Y能使
,若试剂Y能使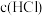 减小,进而使所制得的氯水中
减小,进而使所制得的氯水中 变大,则Y可能是
变大,则Y可能是_______ (填序号)。
A. B.
B. C.硫酸钡
C.硫酸钡
 和较高浓度的氯水。
和较高浓度的氯水。
(1)装置B用于除去HCl,则试剂X是
(2)写出装置C中发生反应的离子方程式:
(3)取装置D中得到的氯水放入试管中,然后向试管中滴加几滴紫色石蕊试液,可观察到的现象是
(4)装置D中
 与水的反应可表示为
与水的反应可表示为 ,若试剂Y能使
,若试剂Y能使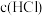 减小,进而使所制得的氯水中
减小,进而使所制得的氯水中 变大,则Y可能是
变大,则Y可能是A.
 B.
B. C.硫酸钡
C.硫酸钡
您最近一年使用:0次
名校
6 . 无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与Cl2反应制备SnCl4,装置如图所示。
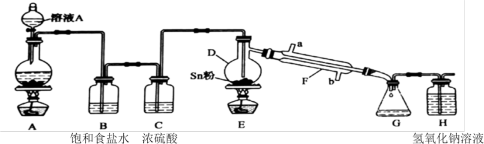
已知:①金属锡熔点为231℃,化学活泼性与铁相似。
②SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解生成SnO2·xH2O,在潮湿的空气中发烟。
③SnCl2中的Sn2+易被氧化为Sn4+。
回答下列问题:
(1)打开分液漏斗上端活塞的作用是___ ,装置A中发生反应的化学方程式为___ 。
(2)实验开始时,正确的操作顺序为___ (用下列序号排顺序)。
①点燃装置A处酒精灯②点燃装置D处酒精灯③打开分液漏斗活塞
(3)装置B中试剂的作用是___ ,装置F中冷凝水的方向是从___ 端进(填“a”或“b”)。
(4)若没有装置C(其他均相同),则D中发生的主要副反应的化学方程式为:___ 。
(5)该实验装置存在设计缺陷,你的改进措施为___ 。
(6)H为尾气处理,请写出反应的离子方程式___ 。

已知:①金属锡熔点为231℃,化学活泼性与铁相似。
②SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解生成SnO2·xH2O,在潮湿的空气中发烟。
③SnCl2中的Sn2+易被氧化为Sn4+。
回答下列问题:
(1)打开分液漏斗上端活塞的作用是
(2)实验开始时,正确的操作顺序为
①点燃装置A处酒精灯②点燃装置D处酒精灯③打开分液漏斗活塞
(3)装置B中试剂的作用是
(4)若没有装置C(其他均相同),则D中发生的主要副反应的化学方程式为:
(5)该实验装置存在设计缺陷,你的改进措施为
(6)H为尾气处理,请写出反应的离子方程式
您最近一年使用:0次
2021-08-13更新
|
156次组卷
|
2卷引用:云南省丽江市2020-2021学年高二下学期期末教学质量监测理科综合化学试题
名校
解题方法
7 . 二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。其制备原理为: 。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
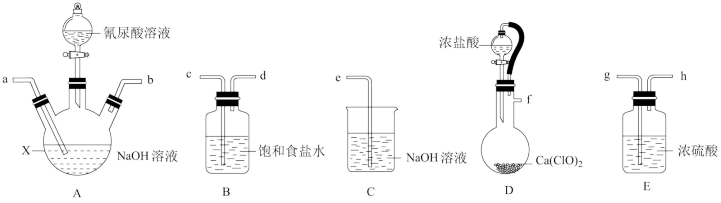
请回答下列问题:
(1)仪器X的名称是___________ 。
(2)装置B的作用是___________ 。
(3)D中发生反应的化学方程式为___________ 。
(4)选择合适装置,按气流从左至右,导管连接顺序为___________ (填字母)。
(5)实验时,先向A中通入氯气,生成高浓度的 溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是
溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是___________ 。
(6)反应结束后,A中浊液经过滤、___________ 、___________ 得到粗产品mg。
(7)粗产品中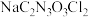 含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用
含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用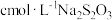 标准溶液进行滴定,加入指示剂,滴定至终点,消耗
标准溶液进行滴定,加入指示剂,滴定至终点,消耗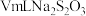 溶液。(假设杂质不与
溶液。(假设杂质不与 反应,涉及的反应为:
反应,涉及的反应为: ,
, )
)
①加入的指示剂是___________ 。
②则 的百分含量为
的百分含量为___________  。(用含m,c,V的代数式表示)
。(用含m,c,V的代数式表示)
 。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
。请选择下列部分装置制备二氯异氰尿酸钠并探究其性质。
请回答下列问题:
(1)仪器X的名称是
(2)装置B的作用是
(3)D中发生反应的化学方程式为
(4)选择合适装置,按气流从左至右,导管连接顺序为
(5)实验时,先向A中通入氯气,生成高浓度的
 溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是
溶液后,再加入氰尿酸溶液,并在整个过程中不断通入一定量的氯气,其原因是(6)反应结束后,A中浊液经过滤、
(7)粗产品中
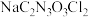 含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用
含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用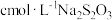 标准溶液进行滴定,加入指示剂,滴定至终点,消耗
标准溶液进行滴定,加入指示剂,滴定至终点,消耗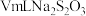 溶液。(假设杂质不与
溶液。(假设杂质不与 反应,涉及的反应为:
反应,涉及的反应为: ,
, )
)①加入的指示剂是
②则
 的百分含量为
的百分含量为 。(用含m,c,V的代数式表示)
。(用含m,c,V的代数式表示)
您最近一年使用:0次
2022-01-23更新
|
1064次组卷
|
4卷引用:重庆市2022届高三第一次联合诊断测试化学试题
重庆市2022届高三第一次联合诊断测试化学试题重庆市天星桥中学2021-2022学年高三下学期学业质量调研抽测化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)黑龙江省哈尔滨市第九中学校2022届高考最后押题卷(一)化学试题
解题方法
8 . 碘化钠在医疗及食品方面有重要的作用,实验室以NaOH、单质碘和水合肼N2H4•H2O(有还原性)为原料制备碘化钠。回答下列有关问题:
(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。
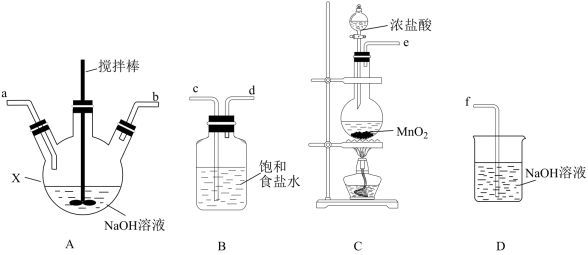
①仪器X的名称是___________ ,导管口连接顺序为___________ (按气流方向,用小写字母表示)。
②若该实验温度控制不当,反应后测得装置A内ClO﹣与ClO 的物质的量之比为5:1,则A中反应的化学方程式是
的物质的量之比为5:1,则A中反应的化学方程式是___________ 。
(2)制备水合肼:反应原理为CO(NH2)2(尿素)+NaClO+NaOH=N2H4•H2O+NaCl+Na2CO3。
①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是___________ 。
②N2H4•H2O一级电离方程式为N2H4•H2O=N2H +OH﹣,其二级电离方程式为
+OH﹣,其二级电离方程式为___________ 。
(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。
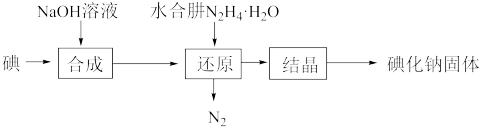
①“还原”过程主要消耗“合成”中生成的副产物IO ,反应的离子方程式是
,反应的离子方程式是___________
②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是___________ 。
(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。

①仪器X的名称是
②若该实验温度控制不当,反应后测得装置A内ClO﹣与ClO
 的物质的量之比为5:1,则A中反应的化学方程式是
的物质的量之比为5:1,则A中反应的化学方程式是(2)制备水合肼:反应原理为CO(NH2)2(尿素)+NaClO+NaOH=N2H4•H2O+NaCl+Na2CO3。
①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是
②N2H4•H2O一级电离方程式为N2H4•H2O=N2H
 +OH﹣,其二级电离方程式为
+OH﹣,其二级电离方程式为(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。

①“还原”过程主要消耗“合成”中生成的副产物IO
 ,反应的离子方程式是
,反应的离子方程式是②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是
您最近一年使用:0次
9 . 利用如图装置进行Cl2制备及其化学性质的探究。下列说法错误的是
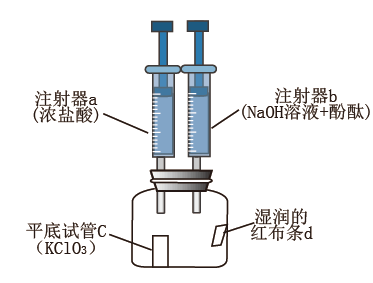

| A.拉动a或b的活塞,可检查装置气密性 |
| B.c中反应的氧化产物与还原产物的质量比为6:1 |
| C.c中产生Cl2后,d褪色的原因是次氯酸具有漂白性 |
| D.性质实验结束后,加入b中溶液除去多余的Cl2,溶液由红色变为无色 |
您最近一年使用:0次
2021-05-13更新
|
747次组卷
|
9卷引用:福建省宁德市2021届普通高中毕业班第三次质量检测化学试题
福建省宁德市2021届普通高中毕业班第三次质量检测化学试题(已下线)第12讲 富集在海水中的元素——卤素(精练)-2022年高考化学一轮复习讲练测(已下线)专题11 富集在海水中的元素——氯 (限时精炼)-2022年高三毕业班化学常考点归纳与变式演练陕西省咸阳市泾阳县2021-2022学年高三上学期期中考试化学试题广西百色市德保高中2021-2022学年高二上学期段考化学试题(已下线)专题13 装置气密性的检查方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)河南省信阳高级中学2021-2022学年高一下学期3月考试化学试题苏州市相城区陆慕高级中学2021-2022学年高二下学期4月线上教学质量检测化学试题黑龙江省黑河市嫩江市高级中学等部分学校2021-2022学年高一下学期第一次月考化学试题
10 . 高铁酸钾 为紫色固体,微溶于
为紫色固体,微溶于 溶液,具有强氧化性,在酸性或中性溶液中产生
溶液,具有强氧化性,在酸性或中性溶液中产生 ,在碱性溶液中较稳定.实验室用如图所示装置(夹持仪器已省略)制备
,在碱性溶液中较稳定.实验室用如图所示装置(夹持仪器已省略)制备 。
。

回答下列问题:
(1)仪器a的名称为_______ ,使用前需_______ 。
(2)装置A圆底烧瓶中发生反应的离子方程式为_______ 。
(3)装置B的作用是_______ 。
(4)装置C中发生反应的化学方程式为_______ ,该反应说明在此条件下 的氧化性比
的氧化性比
_______ (填“强”或“弱”),当装置C中得到大量紫色固体时立即停止通入 ,原因是
,原因是_______ 。
(5)装置D可用于吸收多余的 ,吸收液具有
,吸收液具有_______ (填字母)。
a.氧化性 b.还原性 c.漂白性
 为紫色固体,微溶于
为紫色固体,微溶于 溶液,具有强氧化性,在酸性或中性溶液中产生
溶液,具有强氧化性,在酸性或中性溶液中产生 ,在碱性溶液中较稳定.实验室用如图所示装置(夹持仪器已省略)制备
,在碱性溶液中较稳定.实验室用如图所示装置(夹持仪器已省略)制备 。
。
回答下列问题:
(1)仪器a的名称为
(2)装置A圆底烧瓶中发生反应的离子方程式为
(3)装置B的作用是
(4)装置C中发生反应的化学方程式为
 的氧化性比
的氧化性比
 ,原因是
,原因是(5)装置D可用于吸收多余的
 ,吸收液具有
,吸收液具有a.氧化性 b.还原性 c.漂白性
您最近一年使用:0次



