名校
解题方法
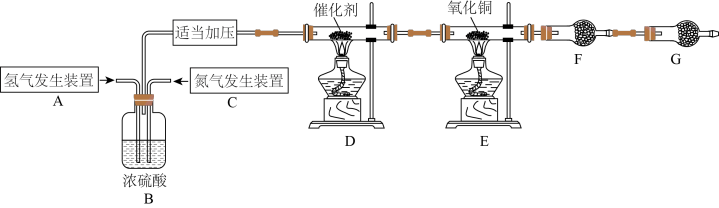
1 . 某学习小组根据氨气还原氧化铜的反应,设计实验测定铜元素相对原子质量Ar(Cu)(近似值)。甲同学模拟合成氨工业制备氨气,反应前先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。装置图如下: 。请回答下列问题:
。请回答下列问题:
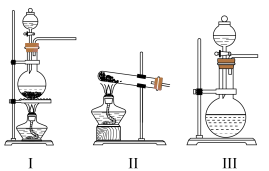
(1)C装置应选用______ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(2)装置B的作用是:①使气体混合均匀;②______ ;③______ 。
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为____________________ 。
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
(5)G装置的作用是①______ ;②______ 。
若没有G装置,测得结果Ar(Cu)______ (填“偏大”“偏小”或“无影响”)。
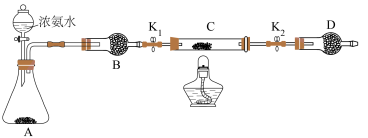
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。______ (填化学式)
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=______ (用含有m1、m2、m3的式子表示)。
 。请回答下列问题:
。请回答下列问题:(1)C装置应选用
(2)装置B的作用是:①使气体混合均匀;②
(3)氨气还原炽热氧化铜(产物之一为空气中含量最多的气体)化学方程式为
(4)干燥管F中盛放的干燥剂为______(填字母代号)。
| A.五氧化二磷 | B.无水CuSO4 | C.碱石灰 | D.无水CaCl2 |
(5)G装置的作用是①
若没有G装置,测得结果Ar(Cu)
(6)乙同学认为上述装置操作麻烦,对原装置改进,新装置如图所示。实验前将石英玻璃管(带两端开关K1和K2)(设为装置C)称重,记为m1 g。将氧化铜装入石英玻璃管中,再次将装置C称重,记为m2 g。按下图连接好装置进行实验,通入NH3,充分反应直至C恒重,记为m3 g。
②根据实验记录,计算铜元素相对原子质量Ar(Cu)=
您最近一年使用:0次
2024-03-12更新
|
573次组卷
|
5卷引用:江西省南昌市第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
2 . 氮及其化合物的转化关系如下图所示,则下列说法不正确的是
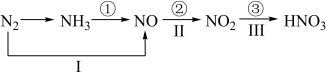
| A.路线①②③是工业生产硝酸的主要途径 | B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.上述所有反应都是氧化还原反应 | D.氮气可在足量的氧气中通过一步反应生成 |
您最近一年使用:0次
2024-03-12更新
|
1081次组卷
|
44卷引用:山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题
山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题河北保定市博野县实验中学2020-2021学年高一下学期期中考试化学试题江苏省镇江中学2020-2021学年高一下学期期中检测化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市晋元高级中学2021-2022学年高一下学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期中考试化学试题湖北省襄阳市第三中学2021-2022学年高一下学期期中考试化学试题江苏省盐城市响水县清源高级中学2021-2022学年高一下学期期中考试化学试题广东省茂名市电白区2021-2022学年高一下学期期中(选择性)考试化学试题广东省顺德市李兆基中学2022-2023学年高一下学期4月期中考试化学试题浙江省余姚中学2022-2023学年高一下学期期中考试 (选考)化学试题广西钦州市浦北县2022-2023学年高一下学期4月期中考试化学试题(已下线)【浙江新东方】双师185高一下山西省怀仁市大地学校2020-2021学年高一下学期第三次月考化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)河北省大名县第一中学2021-2022学年高二上学期开学考试化学试题江苏省常熟市2021-2022学年高二学生暑期自主学习调查化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)安徽省亳州市第二中学2021-2022学年高一下学期期末考试化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题河南省周口经济开发区黄泛区高级中学2021-2022学年高一下学期第一次月考化学试题宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)广西百色民族高级中学2021-2022学年高二上学期9月月考化学试题河南省郑州市第七高级中学2022-2023 学年高一上学期期末考试化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系广东省佛山市顺德区罗定邦中学2022-2023学年高一下学期3月第一次月考化学试题贵州省松桃民族中学2022-2023学年高一下学期3月月考化学试题(已下线)第6讲 硝酸 含氮化合物之间的转化陕西省安康市2023-2024学年高二上学期开学考化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题江苏省徐州市王杰中学2023-2024学年高一下学期第一次月考化学试题宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题14 2024年苏州昆山柏庐高级中学高一3月月考广西南宁一中2023-2024学年高一下学期3月教学质量调研化学试卷福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题
3 . 含氮化合物之间的相互转化对生产、生活有重要意义。N可发生如下转化,下列说法错误的是

| A.试剂B具有氧化性,在反应中发生还原反应 |
| B.反应I不是氧化还原反应 |
C.若试剂A是 ,其还原产物为 ,其还原产物为 |
D.反应Ⅱ中氧化产物与还原产物的物质的量之比为 |
您最近一年使用:0次
解题方法
4 . 氨是重要的化工原料,能与 结合生成
结合生成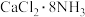 ,加热条件下NH3能将CuO还原成Cu,实验室制取少量NH3并探究其性质。下列装置
,加热条件下NH3能将CuO还原成Cu,实验室制取少量NH3并探究其性质。下列装置不能 达到实验目的的是
 结合生成
结合生成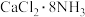 ,加热条件下NH3能将CuO还原成Cu,实验室制取少量NH3并探究其性质。下列装置
,加热条件下NH3能将CuO还原成Cu,实验室制取少量NH3并探究其性质。下列装置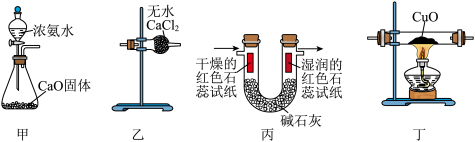
| A.用装置甲制取NH3 | B.用装置乙干燥NH3 |
| C.用装置丙检验NH3水溶液呈碱性 | D.用装置丁探究的NH3还原性 |
您最近一年使用:0次
2024-03-11更新
|
480次组卷
|
2卷引用:江苏省淮安市楚州中学、新马高级中学2023-2024学年高三上学期期中学情检测联考化学试题
5 . ⅤA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。氨是重要的化工原料,广泛用于生产铵盐、硝酸、纯碱、医药等;肼( )的燃烧热为624kJmol,是常用的火箭燃料。白磷(
)的燃烧热为624kJmol,是常用的火箭燃料。白磷( )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
)为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
 )的燃烧热为624kJmol,是常用的火箭燃料。白磷(
)的燃烧热为624kJmol,是常用的火箭燃料。白磷( )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
)为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。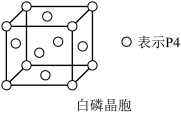
A. 易分解,可用作氮肥 易分解,可用作氮肥 |
| B.氨气易液化,可用于工业制硝酸 |
C. 具有脱水性,可用于实验室乙醇制取乙烯 具有脱水性,可用于实验室乙醇制取乙烯 |
| D.铅锑合金导热性好,可用作铅蓄电池的电极材料 |
您最近一年使用:0次
2024-03-04更新
|
175次组卷
|
2卷引用:江苏省连云港高级中学2023-2024学年高三下学期4月期中考试化学试题
名校
6 . 某课外活动小组在实验室用如图所示的装置进行实验,验证氨的某些性质并收集少量纯净的N2实验进行一段时间后,观察到加热的硬质玻璃管内黑色氧化铜粉末变为红色,盛无水 的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的N2。下列说法不正确的是
的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的N2。下列说法不正确的是
 的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的N2。下列说法不正确的是
的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的N2。下列说法不正确的是
| A.盛放无水硫酸铜的装置是干燥管 |
| B.这个反应说明氨气具有还原性 |
| C.洗气瓶中浓硫酸的作用只有干燥氮气 |
| D.在最后出气管口可以用塑料袋或球胆收集氮气 |
您最近一年使用:0次
2024-03-04更新
|
865次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
7 . 氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理设计实验探究硝酸的制备和性质,装置如图所示(装置内空气均已排尽)。下列说法错误的是
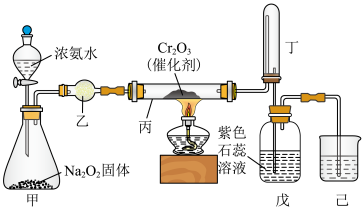
A.甲装置中的固体也可以是 或 或 |
| B.装置丁可以起到防倒吸作用 |
C.理论上装置丙中通入的氨气和氧气物质的量之比为 时可以完全被吸收生成 时可以完全被吸收生成 |
| D.装置乙中的干燥剂可以为碱石灰 |
您最近一年使用:0次
2024-02-26更新
|
740次组卷
|
6卷引用:河南省郑州市宇华实验学校2023-2024学年高一下学期4月期中考试化学试题
名校
8 . 下列实验操作及现象与对应的结论不匹配的是
| 选项 | 操作及现象 | 结论 |
| A | 将Al粉加入强碱性的NaNO3溶液,加热,产生可使湿润的红色石蕊试纸变蓝的气体 |  在强碱性溶液具有氧化性 在强碱性溶液具有氧化性 |
| B | 将浓硫酸与NaCl(s)混合后加热,瓶口有“白雾”出现 | 挥发性:H2SO4<HCl |
| C | 向盛有浓氨水的锥形瓶中通入氧气,并将灼热的铂丝置于液面上方,铂丝保持红热,且瓶内有白烟产生 | NH3的催化氧化反应是吸热反应 |
| D | 向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀后沉淀溶解 | Al(OH)3为两性氢氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
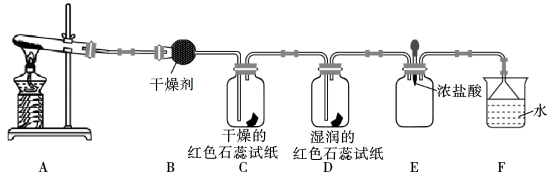
9 . 某化学兴趣小组用下图装置(部分夹持装置已略去)制取氨气并探究其性质。___________ (填化学式)。
(2)装置B中的干燥剂可以选用___________ (填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是________ (填字母),原因是________ 。
(4)当E装置中集满 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_______ 。
(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。___________ ,证明氨气具有___________ (填“氧化性”或“还原性”)。
②若向a中通入标准状况下 的氨气,理论上会得到铜的质量为
的氨气,理论上会得到铜的质量为___________ g。
(6)已知加热条件下,氨气可以与铝发生置换反应生成 ;
; 加热时可溶于浓碱溶液并产生氨气,发生反应:
加热时可溶于浓碱溶液并产生氨气,发生反应: 。称取
。称取 样品
样品 (假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为
(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为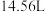 (标准状况),则样品中
(标准状况),则样品中 的质量分数为
的质量分数为___________ %(精确到0.1%)。
(2)装置B中的干燥剂可以选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是
(4)当E装置中集满
 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

②若向a中通入标准状况下
 的氨气,理论上会得到铜的质量为
的氨气,理论上会得到铜的质量为(6)已知加热条件下,氨气可以与铝发生置换反应生成
 ;
; 加热时可溶于浓碱溶液并产生氨气,发生反应:
加热时可溶于浓碱溶液并产生氨气,发生反应: 。称取
。称取 样品
样品 (假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为
(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为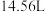 (标准状况),则样品中
(标准状况),则样品中 的质量分数为
的质量分数为
您最近一年使用:0次
2024-02-19更新
|
1237次组卷
|
4卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题陕西省咸阳市实验中学2022-2023学年高一下学期第二次月考化学试题(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省广元市川师大万达中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
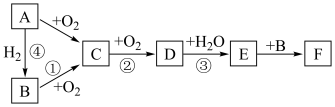
10 . 如图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。
已知:A为气体,A~F都含有相同的元素。
(1)写出下列物质的化学式:C___________ 、F___________
(2)在①②③④中属于氮的固定的是___________ (填序号)
(3)D易溶于水。常温常压下(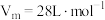 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。
①最终试管中所得E的物质的量浓度为(不考虑E的扩散)___________  。
。
②为了消除D的污染,可将它与B在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是___________ 。
③若C、D按物质的量之比1:1被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是___________ 。为提高吸收速率与效率,最好选用___________ 装置(填序号)。 的物质的量为
的物质的量为___________ 。
已知:A为气体,A~F都含有相同的元素。
(1)写出下列物质的化学式:C
(2)在①②③④中属于氮的固定的是
(3)D易溶于水。常温常压下(
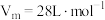 ),将体积为VmL的试管充满D后倒扣在水中。
),将体积为VmL的试管充满D后倒扣在水中。①最终试管中所得E的物质的量浓度为(不考虑E的扩散)
 。
。②为了消除D的污染,可将它与B在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是
③若C、D按物质的量之比1:1被
 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是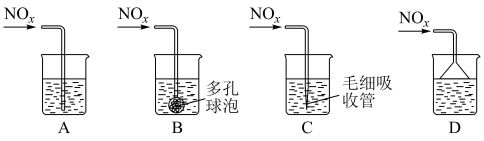
 的物质的量为
的物质的量为
您最近一年使用:0次
2024-01-28更新
|
274次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题



