名校
解题方法
1 . 下列化学反应的离子方程式正确的是
| A.往澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
B.往碳酸镁中滴加稀盐酸: +H+=CO2↑+H2O +H+=CO2↑+H2O |
C.向碳酸氢铵溶液中加入过量的NaOH溶液: |
D.氢氧化钡溶液与稀硫酸反应:Ba2++ +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
您最近一年使用:0次
2 . 下列各组离子中,能在溶液中大量共存的是
A.Na+、OH-、HCO 、Cl- 、Cl- | B.K+、H+、ClO-、Cl- |
C.K+、H+、MnO 、Cl– 、Cl– | D.Na+、OH-、ClO-、Cl- |
您最近一年使用:0次
名校
3 . 用下列装置或操作进行相应实验,能达到实验目的的是
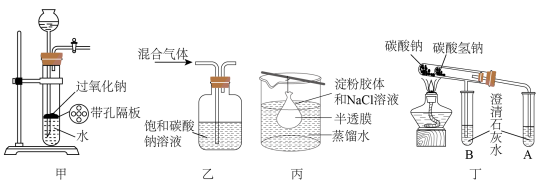

A.图甲装置用 固体粉末“随开随用、随关随停”制氧气 固体粉末“随开随用、随关随停”制氧气 |
B.图乙装置可用于除去 中的 中的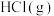 |
| C.图丙装置一段时间后,若往烧杯中液体滴加硝酸酸化硝酸银有白色沉淀,则半透膜破损 |
D.图丁装置用于探究 和 和 的热稳定性 的热稳定性 |
您最近一年使用:0次
4 . 联合制碱是工业生产纯碱的主要方法。下图是联合制碱的流程图:
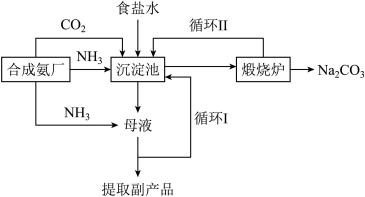
已知:
① 极易溶液于水,1体积水可溶液解700体积
极易溶液于水,1体积水可溶液解700体积 。
。
②煅烧炉中发生的主要反应是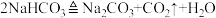 。
。
(1)合成氨厂所用的氮气在工业上通过什么办法生产_______ 。
(2)沉淀池中发生的主要离子反应方程式_______ 。
(3)沉淀池中通常是把氯化钠与两种气体之一配成溶液,再通入过量的另一种气体,后通入的气体是_______ 。
(4)母液中可提取的主要副产品是_______ 。

已知:
①
 极易溶液于水,1体积水可溶液解700体积
极易溶液于水,1体积水可溶液解700体积 。
。②煅烧炉中发生的主要反应是
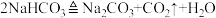 。
。(1)合成氨厂所用的氮气在工业上通过什么办法生产
(2)沉淀池中发生的主要离子反应方程式
(3)沉淀池中通常是把氯化钠与两种气体之一配成溶液,再通入过量的另一种气体,后通入的气体是
(4)母液中可提取的主要副产品是
您最近一年使用:0次
名校
5 . 应用下列装置能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 |  | 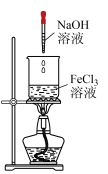 | 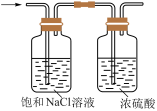 | 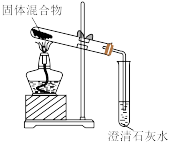 |
| 目的 | 灼烧Fe(OH)3固体制取Fe2O3 | 制备 Fe(OH)3胶体 | 除去 Cl2中的HCl并干燥Cl2 | 除去NaHCO3粉末中混有的少量Na2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-06更新
|
266次组卷
|
2卷引用:江西省上饶市万年县第一中学2023-2024学年高一上学期第二次月考化学试题
名校
6 . 海洋蕴藏着极为丰富的化学资源,如海水中有80多种元素,所含的盐大部分是氯化钠。十九世纪末工业上开始通过电解饱和食盐水的方法制备氯气、氢气和烧碱,并以它们为原料生产一系列含氯、含钠产品。回答下列问题:
(1)写出电解饱和食盐水的化学方程式:___________ 。
(2)工业上用氯气与石灰乳制成漂白粉,漂白粉的有效成分为___________ (填化学式)。
(3)1861年,比利时人索尔维利用氯化钠制取纯碱(被称为索尔维法),___________(填字母)改进了索尔维法,提出了联合制碱法。
(4)制取纯碱时,常伴随有NaHCO3生成。常温下,用如图1所示装置,分别向25mL0.3mol·L-1Na2CO3溶液和25mL0.3mol·L-1 NaHCO3溶液中逐滴滴加0.3mol·L-1的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
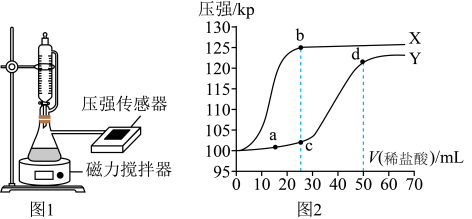
①表示向NaHCO3溶液中滴加盐酸的是曲线___________ (填“X”或“Y”)。
②写出ac段主要反应的实质:___________ (用离子方程式表示)。
③鉴别相同物质的量浓度的Na2CO3溶液和NaHCO3溶液,可使用的方法为___________ (任写一种)。
(5)向250mL1mol·L-1NaOH溶液中通入4.48L(标准状况下)CO2,此时溶液中的溶质为___________ (填化学式)。
(1)写出电解饱和食盐水的化学方程式:
(2)工业上用氯气与石灰乳制成漂白粉,漂白粉的有效成分为
(3)1861年,比利时人索尔维利用氯化钠制取纯碱(被称为索尔维法),___________(填字母)改进了索尔维法,提出了联合制碱法。
| A.侯德榜 | B.吴蕴初 | C.荣毅仁 | D.戴安邦 |
(4)制取纯碱时,常伴随有NaHCO3生成。常温下,用如图1所示装置,分别向25mL0.3mol·L-1Na2CO3溶液和25mL0.3mol·L-1 NaHCO3溶液中逐滴滴加0.3mol·L-1的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。

①表示向NaHCO3溶液中滴加盐酸的是曲线
②写出ac段主要反应的实质:
③鉴别相同物质的量浓度的Na2CO3溶液和NaHCO3溶液,可使用的方法为
(5)向250mL1mol·L-1NaOH溶液中通入4.48L(标准状况下)CO2,此时溶液中的溶质为
您最近一年使用:0次
2023-12-05更新
|
50次组卷
|
2卷引用:江西省上饶市第二中学2023-2024学年高一上学期期中考试化学试卷
名校
解题方法
7 . Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:已知 在低温下溶解度较小。
在低温下溶解度较小。
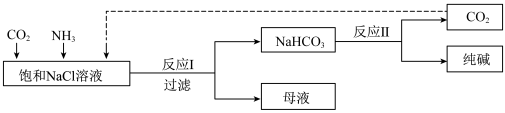
(1)一定温度下,往一定量饱和NaCl溶液中先通入___________ 达到饱和后,再不断通入另一种气体,一段时间后,出现沉淀,过滤得到 晶体。
晶体。
(2)得到的 晶体中可能含有少量NaCl、
晶体中可能含有少量NaCl、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是___________ 。
(3) 和
和 是两种常见的钠盐,
是两种常见的钠盐, 和
和 溶于水溶液均显
溶于水溶液均显___________ (填“酸性”、“中性”或“碱性”)。写出向饱和碳酸钠溶液中通入 的离子方程式
的离子方程式___________ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 的含量。
的含量。
(4)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若___________ ,说明装置不漏气。
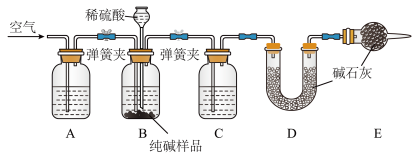
(5)装置A中的试剂为___________ ,装置C中的试剂为___________ 。
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中 的质量分数为
的质量分数为___________ (保留小数点后一位):若缺少E装置,会使测定结果___________ (填“偏高”或“偏低”)。
 在低温下溶解度较小。
在低温下溶解度较小。
(1)一定温度下,往一定量饱和NaCl溶液中先通入
 晶体。
晶体。(2)得到的
 晶体中可能含有少量NaCl、
晶体中可能含有少量NaCl、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是(3)
 和
和 是两种常见的钠盐,
是两种常见的钠盐, 和
和 溶于水溶液均显
溶于水溶液均显 的离子方程式
的离子方程式Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中
 的含量。
的含量。(4)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若

(5)装置A中的试剂为
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-12-03更新
|
77次组卷
|
2卷引用:江西省抚州市资溪县第一中学2023-2024学年高一上学期11月期中考试化学试题
名校
8 . 下列实验装置不能达到实验目的是
| A. 验证Na和水反应是否为放热反应 | B. 用 做喷泉实验 做喷泉实验 | C. 观察纯碱的焰色反应 | D. 比较 、 、 的稳定性 的稳定性 |
 | 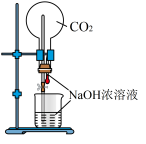 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-03更新
|
127次组卷
|
2卷引用:江西省上饶市广信二中2023-2024学年高一上学期期中考试化学试卷
名校
解题方法
9 . 类比是研究物质性质的常用方法之一,可预测许多物质的性质。下列类比推测的说法中正确的是
A.已知Fe与 能直接化合生成 能直接化合生成 ,推测Cu与 ,推测Cu与 可直接化合生成 可直接化合生成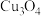 |
B.已知溶解度: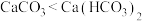 ,推测溶解度: ,推测溶解度: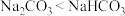 |
C.已知Cu与 反应生成 反应生成 ,推测Fe与 ,推测Fe与 反应生成 反应生成 |
D.已知Fe能与 溶液反应,推测Fe与 溶液反应,推测Fe与 溶液也能反应 溶液也能反应 |
您最近一年使用:0次
2023-12-02更新
|
295次组卷
|
4卷引用:江西省上饶市广信二中2023-2024学年高一上学期期中考试化学试卷
名校
10 . 侯氏制碱法为我国纯碱工业做出了重要贡献。
I.某化学兴趣小组模拟侯氏制碱法制备 ,进一步处理得到
,进一步处理得到 和
和 ,实验流程如图:
,实验流程如图:
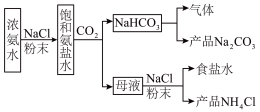
回答下列问题:
(1)生成 的总反应的化学方程式为
的总反应的化学方程式为___________ 。
II.实验中制得的纯碱中含有少量NaCl,该小组设计如图所示装置,测定实验得到的纯碱中 的含量。
的含量。
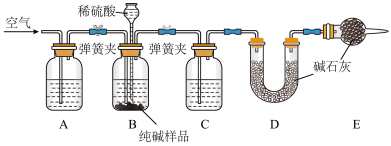
(2)装置A中的试剂为___________ ,装置C中的试剂为___________ 。
(3)实验结束后通入空气的目的:___________ 。
(4)实验前称取26.50g样品,实验后测得D装置增重8.80g,则样品中 的质量分数为
的质量分数为___________ (保留2位小数)。按照以上装置及操作,有同学提出测定结果可能会偏大,他的理由是___________ 。
I.某化学兴趣小组模拟侯氏制碱法制备
 ,进一步处理得到
,进一步处理得到 和
和 ,实验流程如图:
,实验流程如图:
回答下列问题:
(1)生成
 的总反应的化学方程式为
的总反应的化学方程式为II.实验中制得的纯碱中含有少量NaCl,该小组设计如图所示装置,测定实验得到的纯碱中
 的含量。
的含量。
(2)装置A中的试剂为
(3)实验结束后通入空气的目的:
(4)实验前称取26.50g样品,实验后测得D装置增重8.80g,则样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-11-30更新
|
130次组卷
|
2卷引用:江西省清江中学2023-2024学年高一上学期11月期中化学试题



