名校
1 . 纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)实验室中需0.2mol/L的 溶液980mL,配制时应选用容量瓶的规格和称取
溶液980mL,配制时应选用容量瓶的规格和称取 的质量分别是_______。
的质量分别是_______。
(2)碳酸钠和碳酸氢钠的鉴别与稳定性探究。
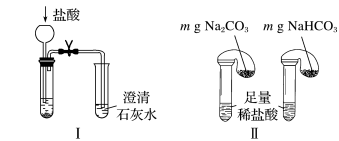
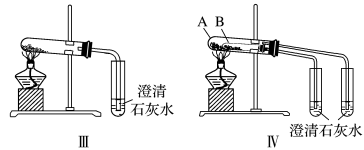
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是_______ (填装置序号)。
②图Ⅲ、Ⅳ中_______ 能更好说明二者的稳定性(填装置序号)。Ⅳ中受热处发生反应的化学方程式:_______ 。
(3)利用图Ⅲ的装置加热 和
和 的混合物,剩余固体成分会随二者物质的量不同而发生变化。当
的混合物,剩余固体成分会随二者物质的量不同而发生变化。当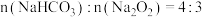 充分混合后,加热至完全反应,试管内剩余的固体是
充分混合后,加热至完全反应,试管内剩余的固体是_______ (填化学式)。
(1)实验室中需0.2mol/L的
 溶液980mL,配制时应选用容量瓶的规格和称取
溶液980mL,配制时应选用容量瓶的规格和称取 的质量分别是_______。
的质量分别是_______。| A.500mL;21.2g | B.900mL;20.1g | C.1000mL;20.1g | D.1000mL;21.2g |


①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②图Ⅲ、Ⅳ中
(3)利用图Ⅲ的装置加热
 和
和 的混合物,剩余固体成分会随二者物质的量不同而发生变化。当
的混合物,剩余固体成分会随二者物质的量不同而发生变化。当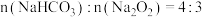 充分混合后,加热至完全反应,试管内剩余的固体是
充分混合后,加热至完全反应,试管内剩余的固体是
您最近一年使用:0次
2021-12-02更新
|
446次组卷
|
2卷引用:黑龙江省大庆实验中学2021-2022学年高一上学期期中考试化学试题
名校
2 . 侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
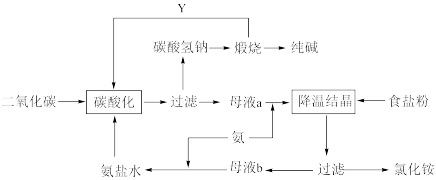
Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是___________
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)___________
(3)侯氏制碱法副产品的一种用途为___________ 。
(4)Y物质是___________ 。
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
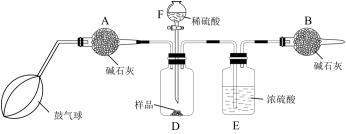
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量( )。
)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质( )。
)。
⑧计算
(5)操作⑥中,鼓入空气的作用是___________ ;
(6)根据题干所给的数据列出样品中 的质量分数表达式
的质量分数表达式___________ 。
(7)经实验发现最终所得的 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是___________ 。

Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)
(3)侯氏制碱法副产品的一种用途为
(4)Y物质是
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中
 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(
 )。
)。③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质(
 )。
)。⑧计算
(5)操作⑥中,鼓入空气的作用是
(6)根据题干所给的数据列出样品中
 的质量分数表达式
的质量分数表达式(7)经实验发现最终所得的
 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是
您最近一年使用:0次
名校
3 . 如图中,A为一种常见的金属单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
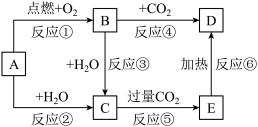
(1)写出下列物质的化学式:B_______ ;E_______ 。
(2)写出B→C反应的化学方程式:_______ ;E→D的化学方程式:_______ 。
(3)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量为_______ 。

(1)写出下列物质的化学式:B
(2)写出B→C反应的化学方程式:
(3)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量为
您最近一年使用:0次
2021-10-09更新
|
225次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高一上学期期中考试化学试题
名校
4 . 现有含 、
、 和
和 的混合物,某同学设计如图所示的实验装置,通过测量反应产生的
的混合物,某同学设计如图所示的实验装置,通过测量反应产生的 和
和 的质量,来确定该混合物中各组分的质量分数。
的质量,来确定该混合物中各组分的质量分数。
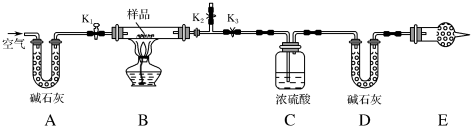
(1)实验步骤:
①按图(夹持装置已省略)组装好实验装置后,首先进行的操作是___________ 。
②称取样品,并将其放入硬质玻璃管中;称量盛装浓硫酸的洗气瓶C的质量和盛装碱石灰的U形管D的质量。
③打开 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是___________ 。
④关闭 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为___________ 、___________ 。
⑤打开 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题:
①若加热反应后不鼓入空气,对测定结果的影响是___________ 。
②E处干燥管中盛放的药品是___________ ,其作用是___________ ,如果实验中没有该装置,则会导致测量结果中 的质量分数
的质量分数___________ (填“偏大”“偏小”或“无影响”)。
 、
、 和
和 的混合物,某同学设计如图所示的实验装置,通过测量反应产生的
的混合物,某同学设计如图所示的实验装置,通过测量反应产生的 和
和 的质量,来确定该混合物中各组分的质量分数。
的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持装置已省略)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中;称量盛装浓硫酸的洗气瓶C的质量和盛装碱石灰的U形管D的质量。
③打开
 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是④关闭
 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为⑤打开
 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。(2)关于该实验方案,请回答下列问题:
①若加热反应后不鼓入空气,对测定结果的影响是
②E处干燥管中盛放的药品是
 的质量分数
的质量分数
您最近一年使用:0次
2021-09-29更新
|
306次组卷
|
3卷引用:黑龙江省齐齐哈尔市齐齐哈尔中学2020-2021学年高一上学期期中考试化学试卷
名校
5 . I、某化学课外活动小组欲制取纯Na2CO3溶液并讨论实验过程中的相关问题,可供选择的试剂有:A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
甲、乙、丙三位同学设计的制备实验方案的反应流程分别如下:
甲:NaOH溶液 Na2CO3溶液
Na2CO3溶液
乙:NaOH溶液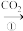 NaHCO3溶液
NaHCO3溶液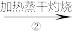 Na2CO3固体
Na2CO3固体 Na2CO3溶液
Na2CO3溶液
丙:NaOH溶液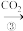 NaHCO3溶液
NaHCO3溶液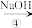 Na2CO3溶液
Na2CO3溶液
请回答下列问题:
(1)___________ 方案最优,其实验的关键是:_________ 。
(2)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学___________ (填“能”或“不能”)达到实验目的;若能,请说明计算所需的数据;若不能,请简要说明理由:___________ 。
II、若以上所需氢氧化钠溶液需要配制成98mL1.0mol/L的溶液,回答以下问题:
(3)计算:需___________ g的NaOH固体;实验中用到的玻璃仪器除了烧杯、玻璃棒、胶头滴管、量筒、试剂瓶,还需要___________ 。
(4)下列实验步骤,正确的操作顺序是:___________ 。
A.用少量蒸馏水洗涤烧杯及玻璃棒,将洗涤液注入容量瓶中,并重复操作两次
B.把已冷却的氢氧化钠溶液注入已查漏的容量瓶中
C.继续往容量瓶中加蒸馏水,使液面接近刻度线1-2cm处改用胶头滴管滴加蒸馏水,使液面达到刻度线
D.根据计算,用天平称取一定质量的氢氧化钠固体置于小烧杯中加入水溶解,并不断搅拌
E.盖上容量瓶的塞子,振荡,摇匀
(5)如果上述B操作中把未冷却的氢氧化钠溶液注入容量瓶中,所配溶液的浓度将___________ (填“偏高”、“偏低”或“无影响”,下同);如果上述D操作中用滤纸称量固体,所配溶液的浓度将___________ ;如果上述C操作中目光俯视,所配溶液的浓度将___________ 。
甲、乙、丙三位同学设计的制备实验方案的反应流程分别如下:
甲:NaOH溶液
 Na2CO3溶液
Na2CO3溶液乙:NaOH溶液
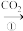 NaHCO3溶液
NaHCO3溶液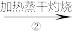 Na2CO3固体
Na2CO3固体 Na2CO3溶液
Na2CO3溶液丙:NaOH溶液
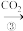 NaHCO3溶液
NaHCO3溶液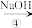 Na2CO3溶液
Na2CO3溶液请回答下列问题:
(1)
(2)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学
II、若以上所需氢氧化钠溶液需要配制成98mL1.0mol/L的溶液,回答以下问题:
(3)计算:需
(4)下列实验步骤,正确的操作顺序是:
A.用少量蒸馏水洗涤烧杯及玻璃棒,将洗涤液注入容量瓶中,并重复操作两次
B.把已冷却的氢氧化钠溶液注入已查漏的容量瓶中
C.继续往容量瓶中加蒸馏水,使液面接近刻度线1-2cm处改用胶头滴管滴加蒸馏水,使液面达到刻度线
D.根据计算,用天平称取一定质量的氢氧化钠固体置于小烧杯中加入水溶解,并不断搅拌
E.盖上容量瓶的塞子,振荡,摇匀
(5)如果上述B操作中把未冷却的氢氧化钠溶液注入容量瓶中,所配溶液的浓度将
您最近一年使用:0次
解题方法
6 . A、B、C、D是钠的重要化合物,有着非常广泛的用途,已知B是常见的供氧剂。其相互转化关系如图所示,回答下列问题:
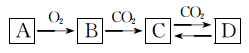
(1)灼烧A、B、C、D四种物质,其焰色为______ 色。
(2)写出 的化学方程式:
的化学方程式:______ 。
(3)等物质的量的A、B分别加入等质量的水中,所得溶液中溶质的质量分数:A______ (填“>”“<”或“=”)B。
(4)不能把等物质的量浓度的C、D鉴别开的是______ (填“澄清石灰水”或“稀盐酸”)。
(5)充分加热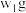 含有D杂质的C样品,若其质量变为
含有D杂质的C样品,若其质量变为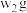 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ 。

(1)灼烧A、B、C、D四种物质,其焰色为
(2)写出
 的化学方程式:
的化学方程式:(3)等物质的量的A、B分别加入等质量的水中,所得溶液中溶质的质量分数:A
(4)不能把等物质的量浓度的C、D鉴别开的是
(5)充分加热
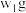 含有D杂质的C样品,若其质量变为
含有D杂质的C样品,若其质量变为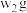 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为
您最近一年使用:0次
名校
解题方法
7 . 将标准状况下一定体积的CO2缓缓通入体积为VLNaOH溶液中,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(2)按反应的先后顺序,写出各步反应的离子方程式:________ 。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=________ .若不能,理由是________ 。
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=________ 。若不能,理由是________ 。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①
(2)按反应的先后顺序,写出各步反应的离子方程式:
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=
您最近一年使用:0次
名校
解题方法
8 . 下图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体
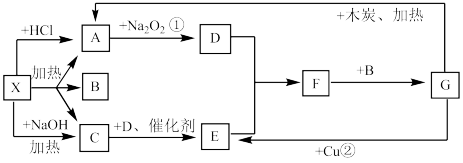
(1)写出有关物质的化学式X:_______ ;F_______
(2)写出A→D的化学方程式____________
(3)写出实验室制备C的化学方程式_______
(4)C可用于制备尿素,尿素CO(NH2)2适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是______
(5)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:
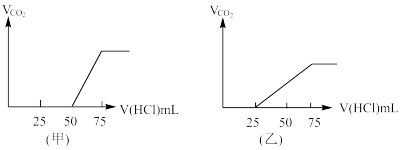
①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:_____ ,其物质的量之比是:_________
②原NaOH溶液的物质的量浓度是_______ mol/L,甲图所示溶液最多还能吸收A体积为_____ mL(标准状况)。

(1)写出有关物质的化学式X:
(2)写出A→D的化学方程式
(3)写出实验室制备C的化学方程式
(4)C可用于制备尿素,尿素CO(NH2)2适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是
(5)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:

①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:
②原NaOH溶液的物质的量浓度是
您最近一年使用:0次
2019-09-04更新
|
312次组卷
|
2卷引用:【全国百强校】黑龙江省哈尔滨市第三中学校2020届高三上学期第一次验收考试化学试题
解题方法
9 . A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图所示的关系,完成下列空白:
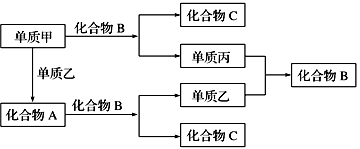
(1)向酚酞试液中加入化合物A的粉末,现象为________ 。
(2)单质甲与化合物B反应的离子方程式为__________ 。5.05g单质甲—钾合金溶于200mL水生成0.075mol氢气,确定该合金的化学式为______ 。
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。
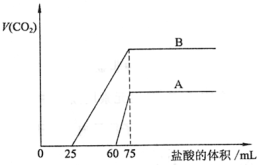
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_____________________
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少_____ 克。
③由A、B可知,两次实验通入的CO2的体积比为___________

(1)向酚酞试液中加入化合物A的粉末,现象为
(2)单质甲与化合物B反应的离子方程式为
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少
③由A、B可知,两次实验通入的CO2的体积比为
您最近一年使用:0次
2018-10-18更新
|
275次组卷
|
3卷引用:黑龙江省哈尔滨师范大学青冈实验中学校2019届高三上学期9月月考化学试题
名校
10 . 实验室配制460mL0.1mol/LNaOH溶液,回答下列问题:
(1)完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、_____ 、_____ 等。
(2)应用托盘天平称取NaOH固体的质量为_________ 。
(3)下面操作造成所配NaOH溶液浓度偏高的是_________________
A .将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
B .摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C .定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E. NaOH固体放在烧杯中称量时间过长
(4)取上述体积均为150mL的 A、B 两份NaOH 溶液,分别通入一定量的 CO2 后,再向所得溶液中滴加一定物质的量浓度的盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
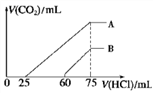
①B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________ 。
②A 曲线表明,盐酸的浓度为______ mol/L;通入的CO2在标准状况下的体积为______ mL。
(1)完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、
(2)应用托盘天平称取NaOH固体的质量为
(3)下面操作造成所配NaOH溶液浓度偏高的是
A .将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
B .摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C .定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E. NaOH固体放在烧杯中称量时间过长
(4)取上述体积均为150mL的 A、B 两份NaOH 溶液,分别通入一定量的 CO2 后,再向所得溶液中滴加一定物质的量浓度的盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。

①B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为
②A 曲线表明,盐酸的浓度为
您最近一年使用:0次



