1 . Ⅰ.化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有___________
①氢氧化亚铁在空气中最终变为灰绿色; ②淀粉溶液遇碘化钾变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色 ④品红溶液通入过量氯气后褪色
⑤无水硫酸铜吸收水蒸气变成浅绿色; ⑥新制氯水久置后变为无色;
Ⅱ.某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
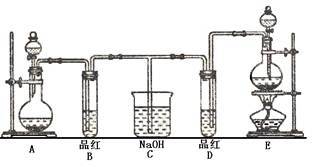
(1) 实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中_________ 装置(填装置序号)制Cl2。在制Cl2的反应中MnO2表现出的性质是_____________ 。
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___________ ,D:______________ 。
(3) 装置C的作用是_____________________________________________________ 。
(4) 甲乙两同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:____________ 。

②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:_________ ,并写出其相应的离子方程式:___________ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是:__________ 。
①氢氧化亚铁在空气中最终变为灰绿色; ②淀粉溶液遇碘化钾变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色 ④品红溶液通入过量氯气后褪色
⑤无水硫酸铜吸收水蒸气变成浅绿色; ⑥新制氯水久置后变为无色;
Ⅱ.某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。

(1) 实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:
(3) 装置C的作用是
(4) 甲乙两同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:

②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是:
您最近一年使用:0次
解题方法
2 . 硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
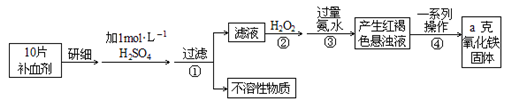
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法______________________ ,该过程的现象为:___________________
(2)步骤②加入过量H2O2的目的(用离子方程式表示):_______________ 。
(3)步骤③中反应的离子方程式:_______________________________________ 。
(4)实际上向滤液中直接滴加X溶液最终也会生成红褐色浊液,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________ 。
(5)步骤④中最终得到a克红棕色粉末,则一系列处理的操作步骤:_________ 、洗涤、_________ 、冷却、称量。
(6)若实验无损耗,则每片补血剂含铁元素的质量__________ g。
(7)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含______________ mgFeSO4·7H2O的片剂。

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法
(2)步骤②加入过量H2O2的目的(用离子方程式表示):
(3)步骤③中反应的离子方程式:
(4)实际上向滤液中直接滴加X溶液最终也会生成红褐色浊液,此过程中发生的氧化还原反应为(用化学方程式表达)
(5)步骤④中最终得到a克红棕色粉末,则一系列处理的操作步骤:
(6)若实验无损耗,则每片补血剂含铁元素的质量
(7)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含
您最近一年使用:0次
2017-03-01更新
|
168次组卷
|
2卷引用:2016-2017学年辽宁省六校协作体高一下学期期初化学试卷
名校
3 . 同学们在实验室里用废铁屑(含少量铜)制取FeCl3·6H2O的流程如下。
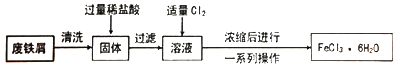
请回答下列问题。
(1)固体中加入过量稀盐酸时的现象是___________ 。
(2)溶液中通入Cl2时发生反应的化学方程式是______________ ,反应中Cl2表现出的性质是_________ ,此处的Cl2也可以用__________ 代替(填序号)。
A.H2O2 B.SO2 C.浓硫酸
(3)上述流程中由浓缩后的溶液获取FeCl3·6H2O的操作包括_____ 、过滤、洗涤。
(4)用FeCl3溶液制备Fe2O3,可向FeCl3溶液中滴加足量____________ ,然后过滤、洗涤、______ ,即可得到Fe2O3。
(5)FeCl3溶液能用作印制电路铜板的腐蚀液,FeCl3溶液与铜反应的离子方程式是______ ,反应一段时间后,取少量腐蚀液,向其中滴加_____ ,观察到_____ ,证明腐蚀液中任含Fe3+。此时腐蚀液中的金属阳离子是_______ 。

请回答下列问题。
(1)固体中加入过量稀盐酸时的现象是
(2)溶液中通入Cl2时发生反应的化学方程式是
A.H2O2 B.SO2 C.浓硫酸
(3)上述流程中由浓缩后的溶液获取FeCl3·6H2O的操作包括
(4)用FeCl3溶液制备Fe2O3,可向FeCl3溶液中滴加足量
(5)FeCl3溶液能用作印制电路铜板的腐蚀液,FeCl3溶液与铜反应的离子方程式是
您最近一年使用:0次
2017-02-27更新
|
270次组卷
|
2卷引用:2016-2017学年山西省太原市高一上学期期末考试化学试卷
4 . (1)电子工业常用FeCl3溶液做腐蚀液制造印刷电路板。用FeCl3做腐蚀液与Cu反应的原理为:2FeCl3+Cu=2FeCl2+CuCl2将一定量铁粉和铜粉的混合物放入等浓度的FeCl3和CuCl2的混合溶液中,可发生多个反应,其中首先发生反应的离子方程式为:________________ 。
(2)某校研究性学习小组用已生锈(Fe2O3)的废铁屑制作印刷电路板的腐蚀液(FeCl3溶液),并将刻蚀电路板后的废液再生为FeCl3溶液循环使用。实验流程如下:
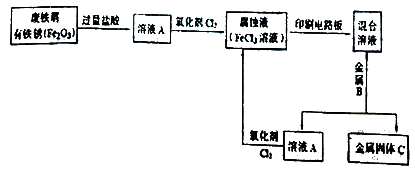
请根据使用流程写出下列反应的离子方程式:
溶液A→腐蚀液:___________________________ 。
混合溶液+金属B→金属固体C:__________________________ 。
(3)检验腐蚀液中Fe3+存在的常用试剂是____________ ,证明Fe3+存在的现象是___________ 。
(4)取适量混合溶液于试管中,加入一定量的铁粉,若反应结束后试管中仍有少量固体,则固体中一定含有___________ ,溶液中可能含有的金属阳离子是____________________ 。
(2)某校研究性学习小组用已生锈(Fe2O3)的废铁屑制作印刷电路板的腐蚀液(FeCl3溶液),并将刻蚀电路板后的废液再生为FeCl3溶液循环使用。实验流程如下:

请根据使用流程写出下列反应的离子方程式:
溶液A→腐蚀液:
混合溶液+金属B→金属固体C:
(3)检验腐蚀液中Fe3+存在的常用试剂是
(4)取适量混合溶液于试管中,加入一定量的铁粉,若反应结束后试管中仍有少量固体,则固体中一定含有
您最近一年使用:0次
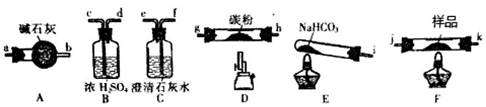
5 . 某研究小组利用下图装置探究CO还原Fe2O3所得到的一种黑色粉末的成分(固定装置略去)。(已知:Fe2+遇到K3[Fe(CN)6]溶液生成蓝色沉淀)
请回答问题:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→____________ →____________ →g→h→__________ →__________ →j → k→____________ →___________ 。(填字母编号)
(2)证明Fe2O3已被还原的现象是___________________ 。
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是__________________ 。
设计并完成实验如下:
①根据实验现象,则猜想_________ 成立。
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为__________________ 。
(4)上述装置还有不妥之处,改进措施为____________________ 。
请回答问题:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→
(2)证明Fe2O3已被还原的现象是
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是
设计并完成实验如下:
步骤 | 操作 | 现象 |
1 | 加入稀盐酸 | 溶解,无气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 |
3 | 变红 |
①根据实验现象,则猜想
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为
(4)上述装置还有不妥之处,改进措施为
您最近一年使用:0次
解题方法
6 . 树德中学高2016级研究性学习小组请你参与“研究铁与水反应所得固体物质的成分,性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验
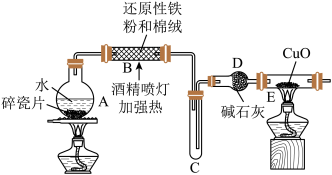
(1)硬质玻璃管中发生反应的化学方程式为__________________ 。
(2)反应前A中投放碎瓷片的目的是__________________ 。
(3)装置E中的现象是__________________ 。
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)硬质玻璃管B冷却后,取少许其中的固体物质溶于_____ 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为______________ (选填序号,①一定有Fe3O4 ②一定有Fe ③只有Fe3O4④只有Fe,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为______________ 。
(6)另—份用胶头滴管加入_______________ ,若出现______________ 现象,可以证明溶液中存在Fe2+,其反应的离子方程式是_____________ 。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
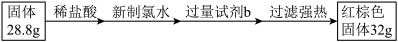
(7)试剂b的化学式是_________ 。
(8)计算反应后B装置中铁元素的质量分数为_______________ 。(保留小数点后—位)
探究一 设计如图所示装置进行“铁与水反应”的实验

(1)硬质玻璃管中发生反应的化学方程式为
(2)反应前A中投放碎瓷片的目的是
(3)装置E中的现象是
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)硬质玻璃管B冷却后,取少许其中的固体物质溶于
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
(6)另—份用胶头滴管加入
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(7)试剂b的化学式是
(8)计算反应后B装置中铁元素的质量分数为
您最近一年使用:0次
7 . 能跟Fe3+作用,且可证明Fe3+具有氧化性的是
①SCN— ②Fe ③Fe2+ ④Cu ⑤ OH—
①SCN— ②Fe ③Fe2+ ④Cu ⑤ OH—
| A.②④ | B.①③ | C.②⑤ | D.①②④ |
您最近一年使用:0次
名校
解题方法
8 . 能与Fe3+反应,且能证明Fe3+具有氧化性的是
①SCN-;②Fe;③Fe2+;④Cu;⑤I-;⑥OH-;⑦Cl2
①SCN-;②Fe;③Fe2+;④Cu;⑤I-;⑥OH-;⑦Cl2
| A.①②④ | B.②④⑤ | C.①③⑥ | D.②⑤⑦ |
您最近一年使用:0次
2016-12-29更新
|
211次组卷
|
2卷引用:2016-2017学年浙江省诸暨中学高一上期中化学试卷
名校
9 . 将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,能证明SO2与FeCl3溶液发生氧化还原反应的是
| 操作 | 现象 | |
| A | 加入NaOH溶液 | 有红褐色沉淀 |
| B | 加入Ba(NO3)2溶液 | 有白色沉淀 |
| C | 加入酸性KMnO4溶液 | 紫色褪去 |
| D | 加入KSCN溶液 | 无明显现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
175次组卷
|
3卷引用:2017届山东省新泰市高三上学期第一次阶段考化学试卷
名校
10 . 下列实验操作及现象和后面结论对应正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液紫色褪色 | SO2具有漂白性 |
| B | 向某溶液中滴加KSCN溶液 | 溶液显红色 | 原溶液中有Fe3+无Fe2+ |
| C | 将稀硫酸滴入碳酸钠溶液中产生的气体通入硅酸钠溶液 | 有白色沉淀生成 | 证明非金属性S>C>Si |
| D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
197次组卷
|
6卷引用:2017届黑龙江省大庆市高三上学期第一次模拟考试化学试卷



