2013·上海·一模
解题方法
1 . 今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3溶液(其他用品略),某课外活动小组同学的实验结果如下(假定反应前后溶液体积不变)。
(1)试判断第④组剩余固体质量x为_________ 。第②组实验中,发生反应的离子方程式为____________________________________ 。
(2)通过计算判断第②组剩余固体的成分_____________ 。
(3)求原混合粉末中Fe、Cu的物质的量之比______________ 。
| 组别 | ① | ② | ③ | ④ |
| 混合粉末质量/g | 40 | 40 | 40 | 40 |
| FeCl3溶液体积/mL | 150 | 300 | 330 | 350 |
| 反应后剩余固体质量/g | 23.2 | 6.4 | 2.56 | x |
(1)试判断第④组剩余固体质量x为
(2)通过计算判断第②组剩余固体的成分
(3)求原混合粉末中Fe、Cu的物质的量之比
您最近一年使用:0次
2010·上海宝山·二模
解题方法
2 . 将Na2S 溶液逐滴加入等物质的量浓度的FeCl3溶液中,发生反应:2Fe3+ + S2- → 2Fe2+ + S ↓;将FeCl3溶液逐滴加入等物质的量浓度的Na2S溶液中,发生反应:2Fe3+ + 3S2- → Fe2S3↓ 。则以下叙述错误的是
| A.Fe3+在酸性环境中氧化性较强 | B.S2-在碱性环境中还原性较强 |
| C.相同温度下Fe(OH)3的溶解度比Fe2S3大 | D.往FeCl3溶液中通入H2S,有硫析出 |
您最近一年使用:0次
2010·上海松江·二模
解题方法
3 . 某化学兴趣小组探究氯化铁溶液的某些性质,将一定量氯化铁固体先加入含1molHCl的浓盐酸中,再加水配制成1L溶液A。
(1)若在A溶液中加入一块铜片,一段时间后得溶液B。写出铜片在FeCl3溶液中反应的离子方程式:___ ;
(2)若在B中加铁粉mg,充分反应后剩余固体ng;过滤,从1L滤液中取出20mL,向其中滴入40mL2mol/LAgNO3溶液时,Cl-恰好完全沉淀。则溶液A中FeCl3的物质的量浓度是__ ;
(3)若在A溶液中加铁粉至不再溶解,则需铁粉__ 克。
(1)若在A溶液中加入一块铜片,一段时间后得溶液B。写出铜片在FeCl3溶液中反应的离子方程式:
(2)若在B中加铁粉mg,充分反应后剩余固体ng;过滤,从1L滤液中取出20mL,向其中滴入40mL2mol/LAgNO3溶液时,Cl-恰好完全沉淀。则溶液A中FeCl3的物质的量浓度是
(3)若在A溶液中加铁粉至不再溶解,则需铁粉
您最近一年使用:0次
2010·上海松江·二模
解题方法
4 . 离子方程式书写正确的是( )
| A.饱和Na2SO3溶液中通入过量SO2:2Na++SO32-+SO2+H2O→2NaHSO3↓ |
| B.用NaOH溶液吸收少量的二氧化硫:OH-+SO2→HSO3- |
| C.次氯酸钙溶液中通入过量的二氧化碳:ClO-+CO2+H2O→HCO3-+HClO |
| D.氢氧化铁溶于过量的氢碘酸中:Fe(OH)3+3H+→Fe3++3H2O |
您最近一年使用:0次
2011·上海普陀·零模
解题方法
5 . 除去括号内的杂质,所用试剂和方法均正确的是
| A.苯(苯酚),加入Br2水后,过滤 |
| B.CO (O2),通过灼热的Cu网后收集气体 |
| C.CaCO3 [Ca(HCO3) 2],置于坩埚中强热 |
| D.FeCl3溶液(FeCl2),加入稍过量的H2O2后放置 |
您最近一年使用:0次
2012·上海杨浦·二模
名校
解题方法
6 . 氯化铁是常见的水处理剂。某氯化铁(FeCl3·6H2O)样品含有少量FeCl2杂质。现要测定其中FeCl3·6H2O的质量分数,实验按以下步骤进行:
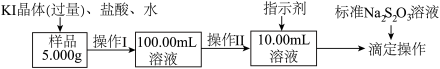
已知有关离子方程式为:2Fe3+ +2I- 2Fe2++ I2 , I2+2S2O32-2I- +S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:____________________ 。
(2)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有_______ 、_______ (填仪器名称)。
(3)操作Ⅱ必须 用到的仪器是_______ (选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是________________________________ 。
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3 溶液18.17mL。该样品中FeCl3·6H2O的质量分数为_______________ 。
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是_______ (选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品中铁元素 的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是_________ ;在过滤前,需要检验是否沉淀完全,其操作是_____________ ;判断是否恒重的标准是__________________________________________ 。

已知有关离子方程式为:2Fe3+ +2I- 2Fe2++ I2 , I2+2S2O32-2I- +S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:
(2)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(3)操作Ⅱ
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3 溶液18.17mL。该样品中FeCl3·6H2O的质量分数为
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品中
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是
您最近一年使用:0次
2011·上海松江·二模
解题方法
7 . 关于物质的检验,下列判断正确的是
| A.在溶液中加入盐酸酸化,无现象;再加入BaCl2溶液,如果生成白色沉淀,则原溶液中一定有大量的SO42-存在 |
| B.在溶液中加入AgNO3溶液,生成不溶于硝酸的沉淀,则原溶液中一定有Cl-存在 |
| C.在溶液中加入浓NaOH溶液,加热后如果生成气体使湿润的红色石蕊试纸变蓝,则原溶液一定是铵盐溶液 |
| D.在溶液中加入KSCN溶液,无现象;再加入稀硝酸,溶液变血红色,则原溶液中一定有Fe2+存在 |
您最近一年使用:0次
2011·上海松江·二模
解题方法
8 . 将20mL2mol/LFeCl3溶液中,加入30mL6mol/L NaOH溶液充分反应后,将其蒸干并灼烧,最后得到固体的质量是
| A.3.20g | B.10.22g | C.12.62g | D.13.70g |
您最近一年使用:0次
2012·上海松江·三模
解题方法
9 . 证明FeCl3溶液显黄色不是氯离子造成的,不可靠的实验是
| A.观察KCl溶液没有颜色 |
| B.加水稀释后FeCl3溶液黄色变浅 |
| C.向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失 |
| D.向FeCl3溶液中加入适量铁,振荡后静置,溶液黄色消失 |
您最近一年使用:0次
13-14高三上·上海·阶段练习
解题方法
10 . 学生甲和学生乙完成了下列实验,其中实验现象完全相同的是
| 学生甲 | 学生乙 | |
| A. | 向碳酸氢钠溶液中逐滴加入盐酸 | 向盐酸中逐滴加入碳酸氢钠溶液 |
| B. | 向三氯化铝溶液中滴加氢氧化钠溶液 | 向氢氧化钠溶液中滴加入三氯化铝溶液 |
| C. | 向FeCl2溶液中滴加KSCN溶液,再通入Cl2 | 向FeCl2溶液中通入Cl2,再滴加KSCN溶液 |
| D. | 向BaCl2溶液中通入SO2 | 向BaCl2溶液中通入SO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



