1 . 下列物质的检验操作或试剂正确的是
| A.检验乙醛中的醛基,可以用银氨溶液小火加热得到银镜 |
| B.纸层析法检验试剂时,试样浸在展开剂中 |
| C.检验Na2SO3是否变质,可以用BaCl2溶液 |
| D.检验FeSO4是否被氧化,使用硫氰化钾溶液 |
您最近一年使用:0次
名校
2 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
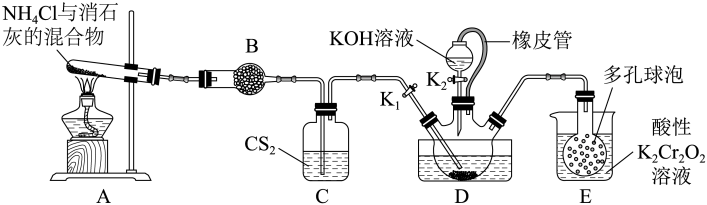
已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂。
回答下列问题:
(1)制备NH4SCN溶液:
①实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应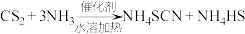 ,该反应比较缓慢,反应至CS2消失。
,该反应比较缓慢,反应至CS2消失。
②装置C的主要作用是_____ ,三颈烧瓶的下层CS2液体必须浸没导气管口,主要原因是_____ 。
(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K1和K2,移开水浴,将装置D继续加热至105℃,NH4HS完全分解后( ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为_____ 。
②装置E的作用除可以吸收NH3外,还能吸收产生的_____ 。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、_____ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取10.0 g样品,配成1000 mL溶液,量取20.00 mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000 mol/L AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液20.00 mL。
①滴定时发生的反应: (白色)则判断到达滴定终点时溶液颜色的变化为
(白色)则判断到达滴定终点时溶液颜色的变化为_____ 。
②晶体中KSCN的质量分数为_____ 。(计算结果精确至0.1%)。

已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂。
回答下列问题:
(1)制备NH4SCN溶液:
①实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应
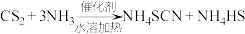 ,该反应比较缓慢,反应至CS2消失。
,该反应比较缓慢,反应至CS2消失。②装置C的主要作用是
(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K1和K2,移开水浴,将装置D继续加热至105℃,NH4HS完全分解后(
 ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为②装置E的作用除可以吸收NH3外,还能吸收产生的
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、
(4)测定晶体中KSCN的含量:称取10.0 g样品,配成1000 mL溶液,量取20.00 mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000 mol/L AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液20.00 mL。
①滴定时发生的反应:
 (白色)则判断到达滴定终点时溶液颜色的变化为
(白色)则判断到达滴定终点时溶液颜色的变化为②晶体中KSCN的质量分数为
您最近一年使用:0次
2010·上海宝山·二模
解题方法
3 . 将Na2S 溶液逐滴加入等物质的量浓度的FeCl3溶液中,发生反应:2Fe3+ + S2- → 2Fe2+ + S ↓;将FeCl3溶液逐滴加入等物质的量浓度的Na2S溶液中,发生反应:2Fe3+ + 3S2- → Fe2S3↓ 。则以下叙述错误的是
| A.Fe3+在酸性环境中氧化性较强 | B.S2-在碱性环境中还原性较强 |
| C.相同温度下Fe(OH)3的溶解度比Fe2S3大 | D.往FeCl3溶液中通入H2S,有硫析出 |
您最近一年使用:0次
名校
解题方法
4 . 食盐中含有一定量的镁、铁等杂质,加碘盐可能含有K+、IO3-、I-、Mg2+.加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热引起的。
已知:IO3-+5I-+6H+→3I2+3H2O,2Fe3++2I-→2Fe2++I2,KI+I2⇌KI3;氧化性:IO3->Fe3+>I2。
(1)学生甲对某加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,加入CCl4,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①第一份试液中,加KSCN溶液显红色,该红色物质是______ (用化学式表示)。
②第二份试液中“加入CCl4”的实验操作名称为______ ,CCl4中显紫红色的物质是______ (用化学式表示)。
③根据这三次实验,学生甲得出以下结论:
在加碘盐中,除了Na+、Cl-以外,一定存在的离子是______ ,可能存在的离子是______ ,一定不存在的离子是______ 。由此可确定,该加碘盐中碘元素是______ 价(填化合价)的碘。
(2)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?______ (填“是”或“否”),并说明理由______ 。
(3)已知:I2+2S2O32-→2I-+S4O62-.学生乙用上述反应方程式测定食用精制盐的碘含量(假设不含Fe3+),其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
根据以上实验,学生乙所测精制盐的碘含量(以I元素计)是______ mg/kg(以含w的代数式表示)。
已知:IO3-+5I-+6H+→3I2+3H2O,2Fe3++2I-→2Fe2++I2,KI+I2⇌KI3;氧化性:IO3->Fe3+>I2。
(1)学生甲对某加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,加入CCl4,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①第一份试液中,加KSCN溶液显红色,该红色物质是
②第二份试液中“加入CCl4”的实验操作名称为
③根据这三次实验,学生甲得出以下结论:
在加碘盐中,除了Na+、Cl-以外,一定存在的离子是
(2)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?
(3)已知:I2+2S2O32-→2I-+S4O62-.学生乙用上述反应方程式测定食用精制盐的碘含量(假设不含Fe3+),其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
根据以上实验,学生乙所测精制盐的碘含量(以I元素计)是
您最近一年使用:0次
2020-02-14更新
|
210次组卷
|
2卷引用:上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题
5 . 一定能实现铁元素之间相互转化的措施是
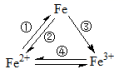

| A.实现①的转化,用比铁活泼的金属 |
| B.实现②的转化,通过钢铁电化腐蚀 |
| C.实现③的转化,加入少量稀硝酸 |
| D.实现④的转化,加入过量氯气 |
您最近一年使用:0次
2019-01-07更新
|
211次组卷
|
2卷引用:上海市宝山区2021届高三下学期二模化学试题
6 . 孔雀石主要含Cu2(OH)2CO3以及少量Fe、Si的化合物。可以用孔雀石为原料制备胆矾(CuSO4·5H2O) 步骤如下:
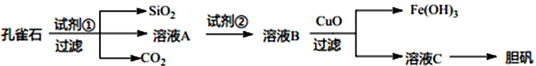
请回答下列问题:
(1)试剂①是一种常见的酸,写出其化学式__________ 。过滤所需要的玻璃仪器有__________ 。
(2)实验室检验Fe3+的常用方法是________________ 。
(3)溶液A中的金属离子有Cu2+、Fe2+、Fe3+上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+,从而形成溶液B,则试剂②能否用氯水________________ (填“能”或“不能”若“不能”,请解释原因)。
(4)由溶液C获得胆矾,需要经过________ 、__________ 、过滤等操作。
(5)取25.00mL溶液A,用1.000×10-2mol/LKMnO4标准溶液滴定。反应离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O,若消耗标准溶液20.00mL,则溶液A中Fe2+的浓度为_______________ 。

请回答下列问题:
(1)试剂①是一种常见的酸,写出其化学式
(2)实验室检验Fe3+的常用方法是
(3)溶液A中的金属离子有Cu2+、Fe2+、Fe3+上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+,从而形成溶液B,则试剂②能否用氯水
(4)由溶液C获得胆矾,需要经过
(5)取25.00mL溶液A,用1.000×10-2mol/LKMnO4标准溶液滴定。反应离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O,若消耗标准溶液20.00mL,则溶液A中Fe2+的浓度为
您最近一年使用:0次
2017-04-08更新
|
417次组卷
|
4卷引用:上海市宝山区2017年高考化学二模试卷



