1 . 下列各组物质反应后,滴入KSCN溶液一定显红色的是( )
| A.生了锈的铁块放入稀H2 SO4中 |
| B.FeCl3、CuCl2的混合液中加入过量的铁粉 |
| C.FeO放入稀HNO3中 |
| D.Fe放入HNO3溶液中 |
您最近一年使用:0次
2016-12-09更新
|
141次组卷
|
2卷引用:2015-2016学年山东省临沂十八中高二下学期六月月考化学试卷
解题方法
2 . 现有金属单质A、B、C、D和气体甲、乙、丙及物质E、F、G、H、I,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
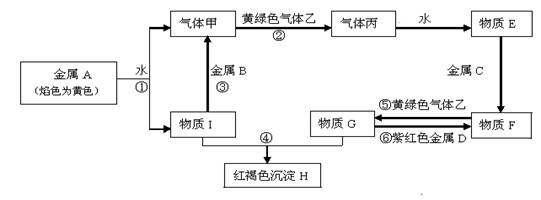
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: B____________ ; F_____________ ;
(2)已知A的一种氧化物可以做核潜艇的供氧剂,则其氧化物供氧时的化学方程式为_____________
(3)①、④离子方程式:________________ ;________________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: B
(2)已知A的一种氧化物可以做核潜艇的供氧剂,则其氧化物供氧时的化学方程式为
(3)①、④离子方程式:
您最近一年使用:0次
2016-12-09更新
|
337次组卷
|
2卷引用:山东省微山县第二中学2020届高三上学期第三学段质量检测化学试题
12-13高一上·山东济宁·期末
解题方法
3 . 下列操作中,溶液的颜色不发生变化的是
| A.氯化铁溶液中加入足量铁粉,充分振荡 |
| B.氯化铁溶液中滴加硫氰化钾(KSCN)溶液 |
| C.氧化铜固体加入稀盐酸中,完全溶解 |
| D.碳酸氢钠溶液中滴加稀盐酸 |
您最近一年使用:0次
4 . 把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+浓度之比为3︰2。则已反应的Fe3+和未反应的Fe3+的物质的量之比为
| A.1︰2 | B.2︰3 | C.3︰2 | D.1︰1 |
您最近一年使用:0次
2016-12-09更新
|
394次组卷
|
3卷引用:2015-2016学年山东省淄博市淄川一中高一上学期1月月考化学试卷
5 . 某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等。水垢会形成安全隐患,需及时清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
(1)用NaOH溶解二氧化硅的化学方程式是__________________________________ 。
(2)已知:20℃时溶解度/g
根据数据,结合化学平衡原理解释清洗CaSO4的过程________________________ 。
(3)在步骤Ⅱ中:
① 被除掉的水垢除铁锈外,还有_______________________________________ 。
② 清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因________ 。
(4)步骤Ⅲ中,加入Na2SO3的目的是_______________________ 。
(5)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe2O3保护膜。
① 完成并配平其反应的离子方程式:______

②下面检测钝化效果的方法合理的是______ 。
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
d.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
(1)用NaOH溶解二氧化硅的化学方程式是
(2)已知:20℃时溶解度/g
| CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| 1.4×10-3 | 2.55×10-2 | 9×10-4 | 1.1×10-2 |
(3)在步骤Ⅱ中:
① 被除掉的水垢除铁锈外,还有
② 清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因
(4)步骤Ⅲ中,加入Na2SO3的目的是
(5)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe2O3保护膜。
① 完成并配平其反应的离子方程式:

②下面检测钝化效果的方法合理的是
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
d.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
您最近一年使用:0次
2016-12-09更新
|
967次组卷
|
3卷引用:山东省新泰二中2020届高三上学期第一阶段性测试化学试题
解题方法
6 . 在FeCl3和CuCl2的混合溶液中加入过量铁粉,反应完全后剩余固体的质量大于加入的铁粉质量。已知原混合溶液中FeCl3为0.4 mol,则CuCl2的物质的量可能是
| A.0.2 mol | B.0.6 mol | C.1.2 mol | D.2 mol |
您最近一年使用:0次
7 . 一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+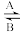 Fe3+。
Fe3+。
在过程A中,Fe2+作________ 剂。
维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有_______ 性。
(2)某些补铁剂的成分是硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是______________ (填序号)。
①稀盐酸 ②石蕊溶液 ③KSCN溶液
(3)要除去FeCl3溶液中少量的氯化亚铁,可行的办法是_______________ (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出该过程中发生反应的离子方程式_______________ 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式____________________________________________________ 。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+
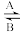 Fe3+。
Fe3+。在过程A中,Fe2+作
维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有
(2)某些补铁剂的成分是硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是
①稀盐酸 ②石蕊溶液 ③KSCN溶液
(3)要除去FeCl3溶液中少量的氯化亚铁,可行的办法是
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出该过程中发生反应的离子方程式
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式
您最近一年使用:0次
名校
解题方法
8 . 把铁片分别放入下列物质的溶液中,充分反应后,溶液质量比反应前减轻的是
| A.CuSO4 | B.Fe2(SO4)3 | C.HCl | D.FeSO4 |
您最近一年使用:0次
2016-12-09更新
|
401次组卷
|
5卷引用:2015-2016学年山东省滕州市第二中学高一上学期12月月考化学试卷
2015-2016学年山东省滕州市第二中学高一上学期12月月考化学试卷(已下线)2015届河北省衡水市冀州中学高三上学期第一次月考化学试卷2014-2015山西省太原市五中高一12月月考化学试卷上海市长宁区2020届高三第二次模拟化学试题云南省宣威市第三中学2022-2023学年高一下学期第一次月考化学试题
9 . 某溶液中除H+、OH-外,还含有大量的Mg2+、Fe3+、Cl-,且这三种离子物质的量浓度之比为1:1:6。下列有关该溶液的判断正确的是
| A.向该溶液中加入KI溶液后,原有的五种离子物质的量不变 |
| B.向该溶液中滴加稀NaOH溶液,立即出现白色沉淀 |
| C.若溶液中c(Cl-)=0.6mol/L,则该溶液的pH为1 |
| D.向该溶液中加入过量铁粉,只发生置换反应 |
您最近一年使用:0次
2016-12-09更新
|
310次组卷
|
8卷引用:2016届山东省烟台市高三上学期期中测试化学试卷
2016届山东省烟台市高三上学期期中测试化学试卷(已下线)2012届江西省吉安一中高三上学期期中考试化学试卷(已下线)2014届高考化学二轮专题冲刺第3讲 离子反应氧化还原反应练习卷2013—2014福建省闽侯一中高三上学期10月月考化学试卷2016届湖北省宜昌一中高三上学期12月月考理综化学试卷2016届黑龙江省牡丹江高级中学高三上学期期末理综化学试卷辽宁省大连市旅顺口区2020届高三上学期期中考试化学试题黑龙江省密山市第四中学2021-2022学年高三上学期第二次月考化学试题
11-12高三上·甘肃兰州·期中
名校
10 . 下列物质能通过化合反应直接制得的是
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl
| A.只有①②③ | B.只有②③ | C.只有①③④ | D.全部 |
您最近一年使用:0次
2016-12-09更新
|
521次组卷
|
9卷引用:2014-2015学年山东桓台第二中学高二上学期(10月)检测化学试卷
(已下线)2014-2015学年山东桓台第二中学高二上学期(10月)检测化学试卷(已下线)2012届甘肃省兰州市第三十一中学高三上学期期中考试化学试卷(已下线)2011-2012学年河北省衡水中学高一上学期期末考试化学试卷黑龙江省伊春市第二中学2016-2017学年高二下学期期末考试化学试题上海市长宁、嘉定区2015届高三第二次质量调研(二模)化学试题2019年广东省清远市高三上学期期末调研考试化学试题上海市2016届高考化学模拟试卷(压轴卷)上海市金山中学2018-2019学年高二下学期期末等级考试化学试题上海市上海中学2021-2022学年高二下学期期末阶段练习化学试题



