1 . 某铜矿石的主要成分为Cu2O,还含有少量Al2O3、Fe2O3、SiO2。工业上用该矿石获取铜和胆矾的操作流程如下:
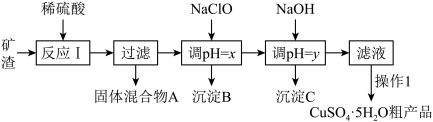
已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)实际生产中将矿石粉碎为矿渣的目的是___________ 。
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为___________ 。
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为___________ (填离子符号),检验该离子常用的试剂为___________ ,生成该离子的离子方程式为___________ 。
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围___________ 。
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品___________ 。

已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全的pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)实际生产中将矿石粉碎为矿渣的目的是
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品
您最近一年使用:0次
2023-04-17更新
|
262次组卷
|
2卷引用:黑龙江省哈尔滨市第四中学校2022-2023学年高一下学期4月月考化学试题
名校
解题方法
2 . 下列是两种制备 的方式
的方式
甲: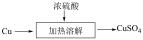
乙: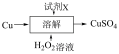
下列说法正确的是
 的方式
的方式甲:

乙:

下列说法正确的是
| A.从环境保护角度分析方案甲更好 |
| B.乙方案中试剂X为稀盐酸 |
C.若用方案甲制备 会产生 会产生 |
D.方案乙“溶解”时发生反应的离子方程式为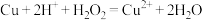 |
您最近一年使用:0次
2023-04-16更新
|
97次组卷
|
2卷引用:湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。实验室用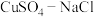 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:

回答以下问题:
(1)图甲中仪器1的名称是___________ ;制备过程中 过量会发生副反应生成
过量会发生副反应生成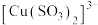 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为___________ 。
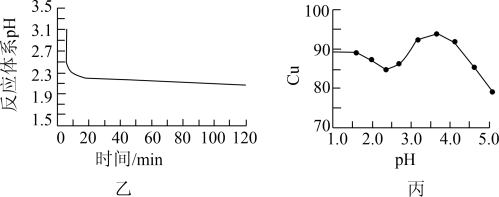
(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式___________ 。丙图是产率随pH变化关系图,实验过程中往往用 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是___________ ,为保证较高产率pH应维持在___________ 左右。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___________ 。
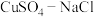 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:
回答以下问题:
(1)图甲中仪器1的名称是
 过量会发生副反应生成
过量会发生副反应生成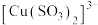 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式
 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是
您最近一年使用:0次
4 . 工业上由含铜废料(含有Cu、CuS、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
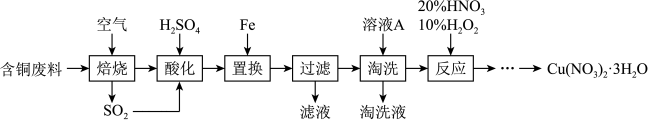
(1)写出CuS“焙烧”生成 和CuO的化学反应方程式:
和CuO的化学反应方程式:___________ 。
(2)图中 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数___________ (填“大于2 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于___________ (填“酸性”或“碱性”)氧化物。
(3)“过滤”所得的滤液中溶质的主要成分为___________ 。
(4)“淘洗”所用的溶液A应选用___________ (填序号)
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:___________ 。
(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中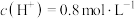 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为___________ 。
 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)写出CuS“焙烧”生成
 和CuO的化学反应方程式:
和CuO的化学反应方程式:(2)图中
 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于(3)“过滤”所得的滤液中溶质的主要成分为
(4)“淘洗”所用的溶液A应选用
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的
 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中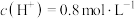 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为
您最近一年使用:0次
名校
解题方法
5 . 学生设计出四种实验方案(如图)用以验证浓硫酸的吸水性,在理论上可行的是


| A.仅①②③ | B.仅①③④ | C.①②③④ | D.仅②③④ |
您最近一年使用:0次
名校
解题方法
6 . CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
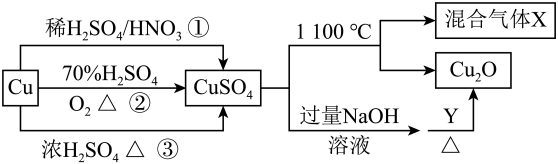

| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1mol CuSO4在1100℃所得混合气体X中O2可能为0.75mol |
| D.Y应该是一种还原剂 |
您最近一年使用:0次
名校
解题方法
7 . 随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了防止食品受潮及氧化变质,在包装内放置的起保护作用的小纸袋中应放入的化学物质是
| A.无水硫酸铜、蔗糖 | B.硅胶、硫酸亚铁 |
| C.食盐、硫酸亚铁 | D.生石灰、食盐 |
您最近一年使用:0次
2023-04-01更新
|
295次组卷
|
2卷引用:天津市第三中学2022-2023学年高一下学期期中质量检测化学试题
名校
解题方法
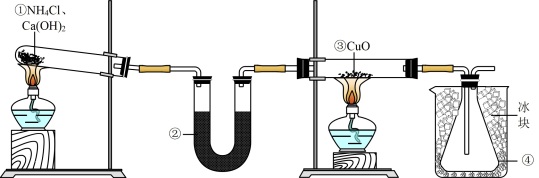
8 . 某实验小组利用如图装置制备 并探究其性质。下列说法正确的是
并探究其性质。下列说法正确的是
 并探究其性质。下列说法正确的是
并探究其性质。下列说法正确的是
A.①中固体可换为 分解制备氨气 分解制备氨气 |
B.②中药品可为无水 |
| C.反应一段时间后,可取③中的固体溶解于稀硝酸中确认反应是否完全 |
| D.反应一段时间后,④中锥形瓶收集到的液体呈碱性 |
您最近一年使用:0次
名校
9 . Cl2、H2SO4、SO2都是化工生产中的重要物质。请回答下列问题:
(1)化工厂可用浓氨水来检验 是否泄漏,当有少量
是否泄漏,当有少量 泄漏时,发生反应的化学方程式为
泄漏时,发生反应的化学方程式为__________ ,若反应中有0.08mol的氨气被氧化,则转移的电子数目是____________ 。
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为_________ 。上述两种方法中,制取硫酸铜的最佳方法是_______ (填“①”或“②”),理由是___________ 。
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
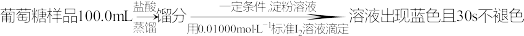 (已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液20.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________ g∙L−1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________ (填“偏高”、“偏低”或“不变”)
(1)化工厂可用浓氨水来检验
 是否泄漏,当有少量
是否泄漏,当有少量 泄漏时,发生反应的化学方程式为
泄漏时,发生反应的化学方程式为(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
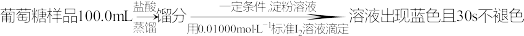 (已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)①按上述方案实验,消耗标准I2溶液20.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为
②在上述实验过程中,若有部分HI被空气氧化,则测定结果
您最近一年使用:0次
名校
解题方法
10 . 从古至今化学均与生活、生产密切相关,化学工业在各国的国民经济中占有重要地位,是许多国家的基础产业和支柱产业。下列有关说法错误的是
| A.大兴机场的隔震支座由橡胶和钢板相互叠加黏结而成,不属于新型无机材料 |
| B.敦煌莫高窟壁画中绿色颜料铜绿的主要成分是碳酸铜 |
| C.南孚干电池低汞化、无汞化,有利于减少废电池造成的土壤污染 |
| D.战国曾侯乙编钟属于青铜制品,青铜是一种合金 |
您最近一年使用:0次



