解题方法
1 . 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值。但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为___________ 。
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为___________ 。
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
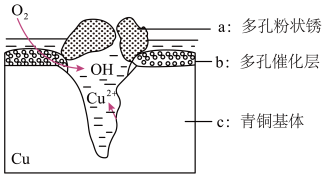
①腐蚀过程中, 负极是___________ (填“a”或“b”或“c”);
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为___________ 。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中, 负极是
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为
您最近一年使用:0次
名校
2 . 为探究固体化合物X(仅含两种元素,100 g/mol<M<200 g/mol)的组成和性质,设计并完成如下实验:
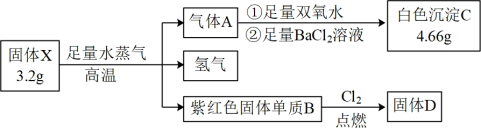
已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是___________ 。
(2)固体X的所含的元素是___________ 。(填元素符号)
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是___________ 。
(4)写出气体A与双氧水反应的化学方程式___________ 。

已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是
(2)固体X的所含的元素是
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是
(4)写出气体A与双氧水反应的化学方程式
您最近一年使用:0次
名校
3 . 秦始皇兵马俑是世界文化遗产,兵马俑表面的彩绘体现了当时彩绘工艺和颜料制作工艺水平,具有极高的历史价值和艺术价值。下列对于兵马俑使用颜料的主要成分与其类别的对应关系正确的是


| 选项 | A | B | C | D |
| 颜色 | 绿色 | 棕红色 | 大红色 | 黑色 |
| 主要成分 | 石绿 | 赭石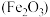 | 朱砂( ) ) | 炭黑(C) |
| 类别 | 碱 | 酸性氧化物 | 电解质 | 有机物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-16更新
|
356次组卷
|
3卷引用:北京市中国人民大学附属中学2022-2023学年高一下学期期末考试化学试题
4 . 下列各组物质之间可以按“物质A→物质B→物质C→物质D”关系直接转化的是
A.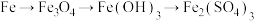 |
B.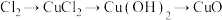 |
C. |
D. |
您最近一年使用:0次
5 . 在一支试管中加入2 mL CuSO4溶液,再将一段光洁的铁丝插入CuSO4溶液中。有说法错误的是
| A.铁丝表面变红 | B.铁丝作还原剂 |
| C.铜比铁更活泼 | D.古时用此反应炼铜 |
您最近一年使用:0次
6 . 某同学对煤进行干馏并检验其中部分产物,装置(夹持装置已略)如图所示。下列说法正确的是
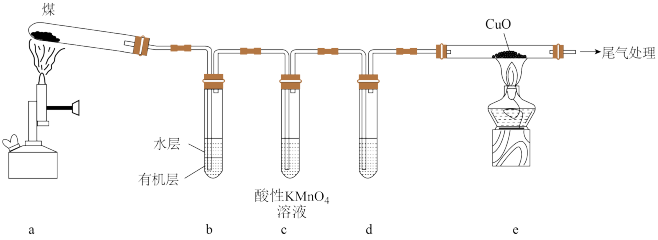

| A.连接装置,检查装置气密性后装入药品,直接加热a装置 |
| B.向b装置的水层中滴入紫色石蕊溶液,溶液变蓝 |
C.c装置可验证产生的气体中一定含有 |
| D.e装置中固体始终为黑色 |
您最近一年使用:0次
名校
7 . 硫及其化合物的“价-类二维图”体现了化学变化之美。下列有关说法正确的是
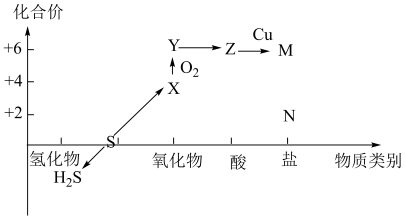

| A.硫在过量的氧气中燃烧直接生成Y |
| B.将X通入BaCl2溶液中先有白色沉淀生成后白色沉淀溶解 |
| C.M的无水固体粉末显蓝色 |
| D.N与Z反应可生成X |
您最近一年使用:0次
2023-07-11更新
|
248次组卷
|
2卷引用:新疆维吾尔自治区昌吉回族自治州2022-2023学年高一下学期期末考试化学试题
名校
8 . 学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
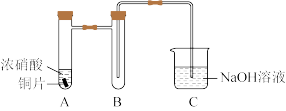
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为______ ,装置B的作用为______ 。
(2)铜与过量 反应的探究如下:
反应的探究如下:

实验②中Cu溶解的离子方程式为______ ;产生的气体为______ 。比较实验①和②,从氧化还原角度说明H⁺的作用是______ 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,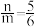 。X的化学式为
。X的化学式为______ 。
(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量______ %。
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为

(2)铜与过量
 反应的探究如下:
反应的探究如下:
实验②中Cu溶解的离子方程式为
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,
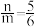 。X的化学式为
。X的化学式为(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L

 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量
您最近一年使用:0次
9 . 下列关于硫酸及硫酸盐的说法错误的是
| A.重晶石的主要成分为BaSO4,医疗上常用做“钡餐” |
| B.检验浓硫酸与木炭反应的全部气体产物,可依次通过无水CuSO4、品红溶液和澄清石灰水 |
| C.胆矾与石灰乳混合可配制农药波尔多液 |
| D.收集的硫酸型酸雨久置后pH减小 |
您最近一年使用:0次
名校
10 . 下列有关物质的性质与用途具有对应关系的是
A. 具有漂白性,可作食品的抗氧化剂 具有漂白性,可作食品的抗氧化剂 |
B. 溶液呈酸性,可用作杀菌剂 溶液呈酸性,可用作杀菌剂 |
| C.浓硫酸具有脱水性,可用来干燥气体 |
| D.木炭具有还原性,可用来冶炼铁矿石 |
您最近一年使用:0次



