名校
1 . 肼(N2H4)是一种无色易溶于水的油状液体,具有碱性和极强的还原性,在工业生产中应用非常广泛。

(1)已知肼的球棍模型如图所示,写出肼的电子式:____________ 。
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。写出该反应的热化学方程式:______________ 。
(3)目前正在研发的一-种肼燃料电池的结构如下图所示。
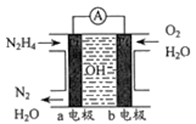
①该电池的负极是______ (填“a”或“b”)电极。
②写出正极的电极反应式:_____________ 。
(4)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生反应:N2H4(l) N2(g)+2H2(g)。测得容器中
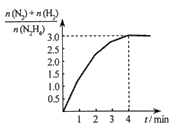
N2(g)+2H2(g)。测得容器中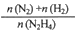 与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=______ 。

(1)已知肼的球棍模型如图所示,写出肼的电子式:
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。写出该反应的热化学方程式:
(3)目前正在研发的一-种肼燃料电池的结构如下图所示。

①该电池的负极是
②写出正极的电极反应式:
(4)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生反应:N2H4(l)
 N2(g)+2H2(g)。测得容器中
N2(g)+2H2(g)。测得容器中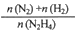 与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=
您最近一年使用:0次
2018-07-04更新
|
367次组卷
|
3卷引用:【全国百强校】江苏省常熟中学2017-2018学年高一下学期期末调研测试化学试题
解题方法
2 . 氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。回答下列问题:
(1)氧化还原法消除NOx的转化如下:
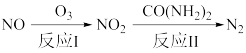
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为_______________ 。
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。
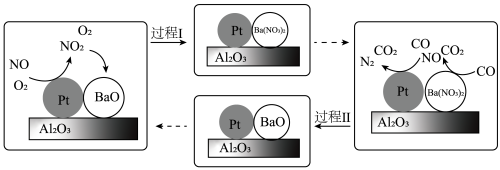
①BaO吸收NO2的化学方程式是______________ 。
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是_______________ 。
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
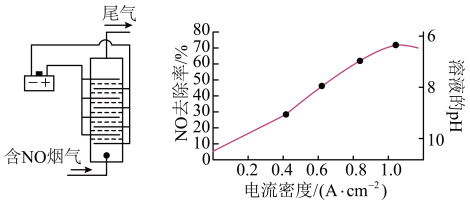
①NO被阳极产生的氧化性物质氧化为 反应的离子方程式为
反应的离子方程式为_______________ 。
②溶液的pH对NO去除率影响的原因是_______________ 。
(1)氧化还原法消除NOx的转化如下:
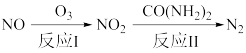
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。

①BaO吸收NO2的化学方程式是
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
①NO被阳极产生的氧化性物质氧化为
 反应的离子方程式为
反应的离子方程式为②溶液的pH对NO去除率影响的原因是
您最近一年使用:0次
2020-09-25更新
|
442次组卷
|
2卷引用:山东省青岛通济实验学校学校2021届高三上学期10月月考化学试题
3 . 镓(Ga)与铝位于同一主族,金属镓的熔点是29.8℃,沸点是2403℃,是一种广泛用于电子工业和通讯领域的重要金属。
(1)工业上利用镓与NH3在1000℃高温下合成固体半导体材料氮化镓(GaN),同时生成氢气,每生成lmol H2时放出10.3 kJ热量。写出该反应的热化学方程式_________ 。
(2)在密闭容器中充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图所示。
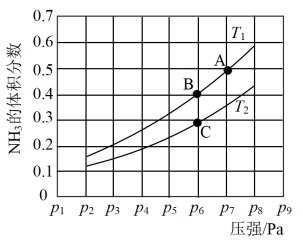
①图中A点和C点化学平衡常数的大小关系是:KA_____ KC,(填“<”、“=”或“>”),理由是___________________ 。
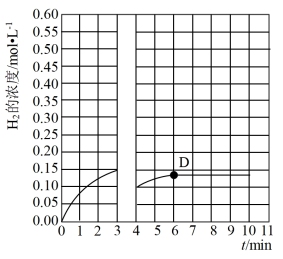
②在T1和P6条件下反应至3min时达到平衡,此时改变条件并于D点处重新达到平衡,H2
的浓度随反应时间的变化如下图所示(3〜4 min的浓度变化未表示出来),则改变的条件为___________ (仅改变温度或压强中的一种)。
(3)气相平衡中用组分的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作
Kp),用含P6的式子表示B点的Kp=_____________ 。
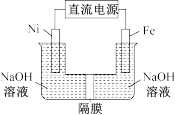
(4)电解精炼法提纯镓的具体原理如下:以粗镓(含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH溶液为电解质,在电流作用下使粗镓溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+。则电解精炼镓时阳极泥的成分是_____ 。
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2—,该反应的离子方程式为______ GaO2— 在阴极放电的电极反应式是_______________ 。
(1)工业上利用镓与NH3在1000℃高温下合成固体半导体材料氮化镓(GaN),同时生成氢气,每生成lmol H2时放出10.3 kJ热量。写出该反应的热化学方程式
(2)在密闭容器中充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图所示。

①图中A点和C点化学平衡常数的大小关系是:KA
②在T1和P6条件下反应至3min时达到平衡,此时改变条件并于D点处重新达到平衡,H2
的浓度随反应时间的变化如下图所示(3〜4 min的浓度变化未表示出来),则改变的条件为

(3)气相平衡中用组分的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作
Kp),用含P6的式子表示B点的Kp=
(4)电解精炼法提纯镓的具体原理如下:以粗镓(含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH溶液为电解质,在电流作用下使粗镓溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+。则电解精炼镓时阳极泥的成分是
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2—,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 金属镓是广泛用于电子工业和通讯领域的重要金属,化学性质与铝元素相似。
(1)工业上提纯镓的方法很多,其中以电解精炼法为多。具体原理如下:以待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH水溶液为电解质溶液。在电流作用下使粗镓在阳极溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是_______ 。
②GaO2-在阴极放电的电极方程式是__________________________ 。
(2)工业上利用固态Ga与NH3高温条件下合成固体半导体材料氮化镓(GaN)同时又有氢气生成。反应中每生成3 mol H2时就会放出30.8 kJ热量。
①该反应的热化学方程式为__________________________ 。
②一定条件下,加入一定量的Ga与NH3进行上述反应,下列叙述符合事实且可作为判断反应已达到平衡状态的标志的是_______________ 。
A.恒温恒压下,混合气体的密度不变
B.断裂3 mol H—H键,同时断裂2 mol N—H键
C.恒温恒压下达平衡后再加入2 mol H2使平衡移动,NH3消耗速率等于原平衡时NH3的消耗速率
D.升高温度,氢气的生成速率先增大再减小
(1)工业上提纯镓的方法很多,其中以电解精炼法为多。具体原理如下:以待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH水溶液为电解质溶液。在电流作用下使粗镓在阳极溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是
②GaO2-在阴极放电的电极方程式是
(2)工业上利用固态Ga与NH3高温条件下合成固体半导体材料氮化镓(GaN)同时又有氢气生成。反应中每生成3 mol H2时就会放出30.8 kJ热量。
①该反应的热化学方程式为
②一定条件下,加入一定量的Ga与NH3进行上述反应,下列叙述符合事实且可作为判断反应已达到平衡状态的标志的是
A.恒温恒压下,混合气体的密度不变
B.断裂3 mol H—H键,同时断裂2 mol N—H键
C.恒温恒压下达平衡后再加入2 mol H2使平衡移动,NH3消耗速率等于原平衡时NH3的消耗速率
D.升高温度,氢气的生成速率先增大再减小
您最近一年使用:0次
2018-10-28更新
|
796次组卷
|
5卷引用:【全国百强校】山东省博兴县第一中学2019届高三上学期第三次月考化学试题
名校
5 . 合成氨在工业生产中具有重要意义。
(1)在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s)△H=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g)△H=-566kJ·mol-1。则该测定反应的热化学方程式为____________________________________ 。
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数φ (CO2)随时间t变化曲线如图。

①温度T1时,0~0.5 min内的反应速率v(CO)=________________ 。
②b点CO的平衡转化率α为____________ ,c点的平衡常数K为________________ 。
③下列措施能提高该反应CO转化率的是________ (填字母)
a.升高温度b.增大压强c.加入催化剂d.移走CO2
(3)若氨水与SO2恰好生成正盐,则此时溶液呈_________ (填“酸性”或“碱性”),向上述溶液中通入___________ (填“NH3”或“SO2”)可使溶液呈中性,此时溶液中含硫微粒浓度的大小关系为________________ 。(已知常温下NH3·H2O的Kb=1.8×10-5mol·L-1,H2SO3的Ka1=1.5×10-2mol·L-1,Ka2=6.3×10-8mol·L-1)
(1)在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s)△H=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g)△H=-566kJ·mol-1。则该测定反应的热化学方程式为
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数φ (CO2)随时间t变化曲线如图。

①温度T1时,0~0.5 min内的反应速率v(CO)=
②b点CO的平衡转化率α为
③下列措施能提高该反应CO转化率的是
a.升高温度b.增大压强c.加入催化剂d.移走CO2
(3)若氨水与SO2恰好生成正盐,则此时溶液呈
您最近一年使用:0次
2018-05-20更新
|
476次组卷
|
3卷引用:【全国市级联考】山东省烟台市2018年高考适应性练习(二)理综化学试题
【全国市级联考】山东省烟台市2018年高考适应性练习(二)理综化学试题江西省抚州市临川第一中学2019-2020学年高二下学期第十次周测化学试题(已下线)本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
名校
解题方法
6 . 已知常温下部分弱电解质的电离平衡常数如下表:
(1)常温下,pH相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其物质的量溶度由大到小的顺序是___________ (填序号)
(2)25°C时,pH=4的NH4Cl溶液中各离子浓度的大小关系为____________________ 。
(3)0.1 mol/L的NaClO溶液和0.1 mol/L的NaHCO3溶液中,c(ClO‒)________ c(HCO3‒)(填“>,<,=”)可使上述两种溶液PH相等的方法是___________ (填代号)
a.向NaClO溶液中加适量的水b.向NaClO溶液中加适量的NaOH
c.向NaHCO3溶液中加适量的水d.向NaHCO3溶液中加适量的NaOH
(4)向NaClO溶液中通入少量的CO2,所发生的离子方程式为______________________ 。
(5)常温下,0.1mol/L的氨水和0.1mol/L的NH4Cl溶液等体积混合,判断混合溶液的酸碱性____________ (填“酸性”“碱性”“中性”)
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10−4 | 4.7×10−8 | K1=4.3×10−7 K2=5.6×10−11 | Kb=1.7×10−5 |
(2)25°C时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)0.1 mol/L的NaClO溶液和0.1 mol/L的NaHCO3溶液中,c(ClO‒)
a.向NaClO溶液中加适量的水b.向NaClO溶液中加适量的NaOH
c.向NaHCO3溶液中加适量的水d.向NaHCO3溶液中加适量的NaOH
(4)向NaClO溶液中通入少量的CO2,所发生的离子方程式为
(5)常温下,0.1mol/L的氨水和0.1mol/L的NH4Cl溶液等体积混合,判断混合溶液的酸碱性
您最近一年使用:0次
2018-02-25更新
|
305次组卷
|
6卷引用:山东省济南市第一中学2017-2018学年高二上学期期末考试化学试题
名校
7 . 尿素/H2O2溶液可用于烟气的脱硫脱硝。
(1)已知T℃时,2SO2(g)+O2(g) 2SO3(g) △H1
2SO3(g) △H1
2H2O2(I)=2H2O(I)+O2(g) △H2
SO3(g)+H2O(I))=H2SO4(I) △H3
则SO2(g)+H2O2(I))=H2SO4(I) △H4=__________ (用含△H1、△H2、△H3的代数式表示)
(2)尿素[CO(NH2)2]溶液对NOx及SO2有一定的脱除率。将SO2和NOx (N〇约占90%)通入氧气的体积分数为7%、尿素浓度为5%的反应器中进行反应。
①烟气中SO2最终转化为一种正盐,其化学式为______________ ;NO和NO2以物质的量之比1:1与CO(NH2)2反应生成无毒气体的化学方程式为_______________ 。
②氨基甲酸铵(H2NCOONH4)是尿素的水解产物,将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应:NH2COONH4(s) 2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
该反应的△H__________ (填“>”或“<”)0;348K时,该反应的平衡常数K__________________ 。
(3)其他条件不变,向尿素溶液中添加H2O2溶液,测得不同 pH下氮氧化物的脱除率与时间的关系如图所示。
①NO与H2O2发生反应生成亚硝酸时,氧化剂与还原剂的物质的量之比为____________ 。
(2)脱硝时,最佳pH为_________ ;在碱性较强时,NOx脱除率降低,其原因是___________ (任写一点)。
(1)已知T℃时,2SO2(g)+O2(g)
 2SO3(g) △H1
2SO3(g) △H12H2O2(I)=2H2O(I)+O2(g) △H2
SO3(g)+H2O(I))=H2SO4(I) △H3
则SO2(g)+H2O2(I))=H2SO4(I) △H4=
(2)尿素[CO(NH2)2]溶液对NOx及SO2有一定的脱除率。将SO2和NOx (N〇约占90%)通入氧气的体积分数为7%、尿素浓度为5%的反应器中进行反应。
①烟气中SO2最终转化为一种正盐,其化学式为
②氨基甲酸铵(H2NCOONH4)是尿素的水解产物,将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应:NH2COONH4(s)
 2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:温度/K | 338 | 343 | 348 | 353 |
平衡时气体的总浓度/mol • L-1 | 0.36 | 0.48 | 0.60 | 0.72 |
该反应的△H
(3)其他条件不变,向尿素溶液中添加H2O2溶液,测得不同 pH下氮氧化物的脱除率与时间的关系如图所示。
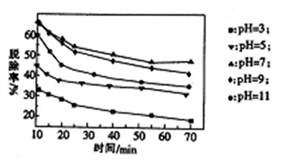
①NO与H2O2发生反应生成亚硝酸时,氧化剂与还原剂的物质的量之比为
(2)脱硝时,最佳pH为
您最近一年使用:0次
2017-03-14更新
|
596次组卷
|
2卷引用:2017届山东省菏泽市高三一模理综化学试卷
8 . 金属钒被誉为“合金的维生素”,常用于催化剂和新型电池。钒(V)在溶液中主要以VO43-(黄色)、VO2+(浅黄色)、VO2+(蓝色)、V3+(绿色)、V2+(紫色)等形式存在。回答下列问题:
(1)工业中利用V2O5制备金属钒。
4Al(s)+3O2(g)=2Al2O3(s) △H1=-2834kJ/mol
4V(s)+5O2(g)=2V2O5(s) △H2=-3109kJ/mol
写出V2O5与A1反应制备金属钒的热化学方程式____________________ 。
(2)V2O5是一种重要的氧化物,具有以下性质:
①V2O5在强碱性溶液中以VO43-形式存在,试写出V2O5溶于NaOH溶液的离子方程式:___________________________________________ 。
②V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液,试写出V2O5与浓盐酸反应的化学反应方程式:________________________________ 。
(3)VO43-和V2O74-在PH≥13的溶液中可相互转化。室温下,1.0 mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。
①写出溶液中Na3VO4转化为Na4V2O7的离子方程式__________________ 。
②由图可知,溶液中c(H+)增大,VO43-的平衡转化率______ (填“增大”“减小”或“不变”)。根据A点数据,计算该转化反应的平衡常数的数值为_____________ 。
(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图所示:
①放电过程中A电极的反应式为__________________ 。
②充电过程中,B电极附近溶液颜色变化为___________________ 。
(1)工业中利用V2O5制备金属钒。
4Al(s)+3O2(g)=2Al2O3(s) △H1=-2834kJ/mol
4V(s)+5O2(g)=2V2O5(s) △H2=-3109kJ/mol
写出V2O5与A1反应制备金属钒的热化学方程式
(2)V2O5是一种重要的氧化物,具有以下性质:
①V2O5在强碱性溶液中以VO43-形式存在,试写出V2O5溶于NaOH溶液的离子方程式:
②V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液,试写出V2O5与浓盐酸反应的化学反应方程式:

(3)VO43-和V2O74-在PH≥13的溶液中可相互转化。室温下,1.0 mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。
①写出溶液中Na3VO4转化为Na4V2O7的离子方程式
②由图可知,溶液中c(H+)增大,VO43-的平衡转化率
(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图所示:

①放电过程中A电极的反应式为
②充电过程中,B电极附近溶液颜色变化为
您最近一年使用:0次
9 . 铁、铜及其化合物在工农业生产中应用广泛。
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为_______ 。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是____________ (用序号填写)。
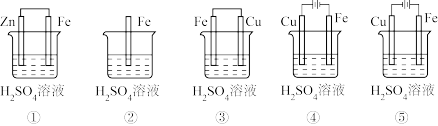
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s) H=-1118 kJ·mol-1
H=-1118 kJ·mol-1
②2Al(s)+3/2O2(g)=A12O3(s) H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1
则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为______________ 。
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式______ 。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是______________ 。
(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是____________ 。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为____ 。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=______ 。
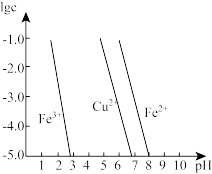
已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度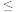 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为
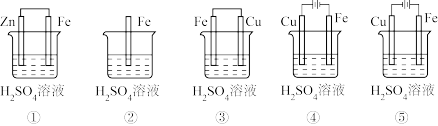
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)
 H=-1118 kJ·mol-1
H=-1118 kJ·mol-1②2Al(s)+3/2O2(g)=A12O3(s)
 H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式

(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是

已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度
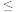 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
您最近一年使用:0次
2016-12-09更新
|
822次组卷
|
3卷引用:2015届山东省枣庄市六中高三下学期开学初检测试题理综化学试卷
真题
10 . 化学反应原理在科研和生产中有广泛应用
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应TaS2(s)+2I2(g) TaI4(g)+S2(g) △H>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=
TaI4(g)+S2(g) △H>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=______ ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为______ 。
(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1______ T2(填“>”“<”或“=”)。上述反应体系中循环使用的物质是______ 。

(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为______ ,滴定反应的离子方程式为______ 。
(4)25℃时,H2SO3
 +H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=
+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=______ mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中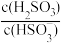 将
将______ (填“增大”“减小”或“不变”)。
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应TaS2(s)+2I2(g)
 TaI4(g)+S2(g) △H>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=
TaI4(g)+S2(g) △H>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1

(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为
(4)25℃时,H2SO3

 +H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=
+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=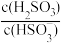 将
将
您最近一年使用:0次



