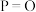1 . Ⅰ.汽车让人们的生活越来越便捷。请回答以下问题:
(1)汽车尾气主要含有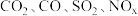 等物质,是造成城市空气污染的主要因素之一;
等物质,是造成城市空气污染的主要因素之一;  和
和 反应生成
反应生成 的能量变化如下图所示,则该反应的热化学方程式为
的能量变化如下图所示,则该反应的热化学方程式为_______________ 。 可作氧化剂,用于氧化火箭推进器中的强还原剂肼
可作氧化剂,用于氧化火箭推进器中的强还原剂肼 ,释放大量的能量,其热化学方程式为:
,释放大量的能量,其热化学方程式为:
①若进行上述反应,放出热量为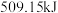 ,则转移电子数目为
,则转移电子数目为_______________  。
。
②已知: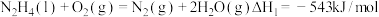

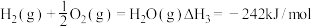
若用氟气代替二氧化氮作氧化剂,则反应释放能量更多,请写出液态肼和氟气反应的热化学方程式:_______________ 。
(3)汽车受到猛烈碰撞时,安全气囊内的 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
Ⅱ.污染性气体的处理:
(4)以 溶液作为吸收剂,控制溶液的
溶液作为吸收剂,控制溶液的 ,将二氧化硫和一氧化氮转化为
,将二氧化硫和一氧化氮转化为 和
和 去除。
去除。
①在酸性 溶液中,
溶液中, 氧化
氧化 的离子方程式为
的离子方程式为_______________ 。
② 的去除率高于
的去除率高于 的可能原因是
的可能原因是_______________ 。(任写一条)
(5)将 的混合气体共
的混合气体共 (已换算为标准状况,下同)通入水中,气体体积减小
(已换算为标准状况,下同)通入水中,气体体积减小 ,若将该混合气体与一定量
,若将该混合气体与一定量 混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是
混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是_______________ (填序号)。
①混合气体中 的体积分数为
的体积分数为
②所得硝酸溶液物质的量浓度为
③用足量 溶液可将该混合气体完全吸收
溶液可将该混合气体完全吸收
④消耗的 在标准状况下的体积为
在标准状况下的体积为
(1)汽车尾气主要含有
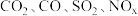 等物质,是造成城市空气污染的主要因素之一;
等物质,是造成城市空气污染的主要因素之一;  和
和 反应生成
反应生成 的能量变化如下图所示,则该反应的热化学方程式为
的能量变化如下图所示,则该反应的热化学方程式为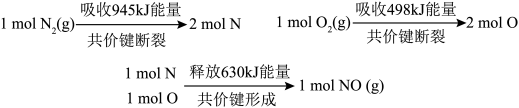
 可作氧化剂,用于氧化火箭推进器中的强还原剂肼
可作氧化剂,用于氧化火箭推进器中的强还原剂肼 ,释放大量的能量,其热化学方程式为:
,释放大量的能量,其热化学方程式为:
①若进行上述反应,放出热量为
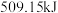 ,则转移电子数目为
,则转移电子数目为 。
。②已知:
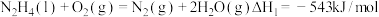

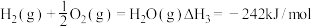
若用氟气代替二氧化氮作氧化剂,则反应释放能量更多,请写出液态肼和氟气反应的热化学方程式:
(3)汽车受到猛烈碰撞时,安全气囊内的
 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。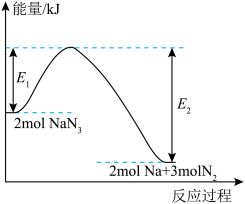
A. 属于离子化合物 属于离子化合物 |
B. 的分解反应属于吸热反应 的分解反应属于吸热反应 |
C. 表示 表示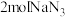 固体具有的能量 固体具有的能量 |
D. 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
Ⅱ.污染性气体的处理:
(4)以
 溶液作为吸收剂,控制溶液的
溶液作为吸收剂,控制溶液的 ,将二氧化硫和一氧化氮转化为
,将二氧化硫和一氧化氮转化为 和
和 去除。
去除。①在酸性
 溶液中,
溶液中, 氧化
氧化 的离子方程式为
的离子方程式为②
 的去除率高于
的去除率高于 的可能原因是
的可能原因是(5)将
 的混合气体共
的混合气体共 (已换算为标准状况,下同)通入水中,气体体积减小
(已换算为标准状况,下同)通入水中,气体体积减小 ,若将该混合气体与一定量
,若将该混合气体与一定量 混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是
混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是①混合气体中
 的体积分数为
的体积分数为
②所得硝酸溶液物质的量浓度为

③用足量
 溶液可将该混合气体完全吸收
溶液可将该混合气体完全吸收④消耗的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
解题方法
2 . 氢能源是最具前景的应用能源之一,氢气的制备和应用是目前的研究热点。回答下列问题:氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。 键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为
键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为_______ kJ。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:_______ ,在导线中电子流动方向为_______ (用a、b表示)。
②负极反应式为_______ 。
(3)电池工作时, 和
和 连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.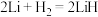
Ⅱ.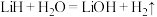
①反应Ⅰ中的还原剂是_______ ,反应Ⅱ中的氧化剂是_______ 。
②金属锂吸收的氢气与放出的氢气的物质的量之比为_______ 。
 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。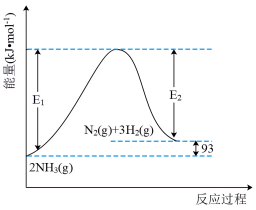
 键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为
键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
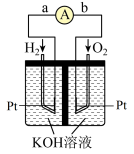
②负极反应式为
(3)电池工作时,
 和
和 连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ.
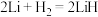
Ⅱ.
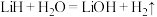
①反应Ⅰ中的还原剂是
②金属锂吸收的氢气与放出的氢气的物质的量之比为
您最近一年使用:0次
3 . 氢燃料电池汽车是未来汽车发展的重要方向之一。二甲醚重整制氢技术是一种理想制氢方案。
(1)1mol二甲醚CH3OCH3(g)与水蒸气发生可逆反应,生成CO2(g)和H2(g)的化学方程式为________________ 。
(2)根据下列两个热化学方程式,计算上述反应的反应热∆H=__________ kJ·mol-1。
反应I:CH3OCH3(g)+H2O(g)⇌2CH3OH(g) ∆H1=+37 kJ·mol-1
反应Ⅱ:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ∆H2=+49 kJ·mol-1
升高温度,反应速率_______ (填“变大”、“变小”或“不变”);根据以上反应判断,可采取_____________ (合理措施)来提高二甲醚的转化率(写一条)。
(3)在一个恒压 (起始体积为3 L)的密闭容器中充入2 mol CH3OH(g)和1 mol H2O(g),仅研究反应Ⅱ。CH3OH的平衡含量随温度、压强的变化如图所示。_______ P2(填“>”、“<”);B、C两点平衡常数KB_______ KC(填“>”、“<”或“=”);A点体积变为______ L,此时平衡常数KA的计算表达式为____________ (列式即可)。
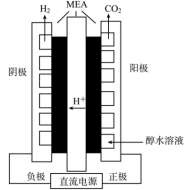
(4)我国科学家开发了一种运用质子交换膜的电解甲醇制氢装置(见图),甲醇的电解电压相对于水可降低近2/3,降低了制氢的能耗。写出阳极电极反应式______________ 。
(1)1mol二甲醚CH3OCH3(g)与水蒸气发生可逆反应,生成CO2(g)和H2(g)的化学方程式为
(2)根据下列两个热化学方程式,计算上述反应的反应热∆H=
反应I:CH3OCH3(g)+H2O(g)⇌2CH3OH(g) ∆H1=+37 kJ·mol-1
反应Ⅱ:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ∆H2=+49 kJ·mol-1
升高温度,反应速率
(3)在一个

(4)我国科学家开发了一种运用质子交换膜的电解甲醇制氢装置(见图),甲醇的电解电压相对于水可降低近2/3,降低了制氢的能耗。写出阳极电极反应式
您最近一年使用:0次
4 . 减少 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。
是我国能源领域的一个重要战略方向。
在 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:
反应i:
 kJ/mol
kJ/mol
反应ii:
 kJ/mol
kJ/mol
(1)反应iii: 的
的
___________ 。
(2)在 加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
(3)某温度下,向容积恒为1 L的密闭容器中通入1 mol 和5 mol
和5 mol  ,10 min后体系达到平衡,此时
,10 min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。[已知:
的选择性为50%。[已知: 的选择性:
的选择性: ]
]
①反应i的平衡常数
___________ (写出计算式即可)。
②反应ii的净速率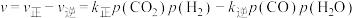 ,其中
,其中 、
、 分别为正、逆反应的速率常数,p为气体的分压。降低温度时,
分别为正、逆反应的速率常数,p为气体的分压。降低温度时,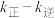
___________ (填“增大”“减小”或“不变”)。
③其他条件相同时,反应温度对 的平衡转化率和
的平衡转化率和 的选择性的影响如图甲所示,温度高于260°C时,
的选择性的影响如图甲所示,温度高于260°C时, 的平衡转化率变化的原因是
的平衡转化率变化的原因是___________ 。 的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:
的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:___________ 。
(4)利用如图所示原理去除NO:___________ ,每产生224 mL  (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为___________ mol。
 的排放、捕集并利用
的排放、捕集并利用 是我国能源领域的一个重要战略方向。
是我国能源领域的一个重要战略方向。在
 加氢合成甲醇的体系中,同时存在以下反应:
加氢合成甲醇的体系中,同时存在以下反应:反应i:

 kJ/mol
kJ/mol反应ii:

 kJ/mol
kJ/mol(1)反应iii:
 的
的
(2)在
 加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。
加氢合成甲醇的体系中,下列说法不正确的是___________(填序号)。| A.若在绝热恒容容器,反应i的平衡常数K保持不变,说明反应i、ii都已达平衡 |
| B.若气体的平均相对分子质量不变,说明反应i、ii都已达平衡 |
| C.体系达平衡后,若压缩体积,反应i平衡正向移动,反应i平衡不移动 |
| D.选用合适的催化剂可以提高甲醇在单位时间内的产量 |
(3)某温度下,向容积恒为1 L的密闭容器中通入1 mol
 和5 mol
和5 mol  ,10 min后体系达到平衡,此时
,10 min后体系达到平衡,此时 的转化率为20%。
的转化率为20%。 的选择性为50%。[已知:
的选择性为50%。[已知: 的选择性:
的选择性: ]
]①反应i的平衡常数

②反应ii的净速率
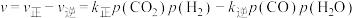 ,其中
,其中 、
、 分别为正、逆反应的速率常数,p为气体的分压。降低温度时,
分别为正、逆反应的速率常数,p为气体的分压。降低温度时,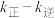
③其他条件相同时,反应温度对
 的平衡转化率和
的平衡转化率和 的选择性的影响如图甲所示,温度高于260°C时,
的选择性的影响如图甲所示,温度高于260°C时, 的平衡转化率变化的原因是
的平衡转化率变化的原因是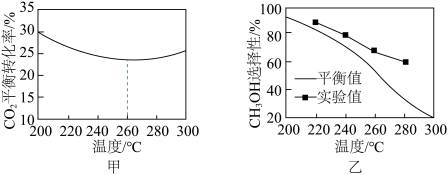
 的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:
的选择性:实验值略高于平衡值,从化学反应速率角度解释原因:(4)利用如图所示原理去除NO:
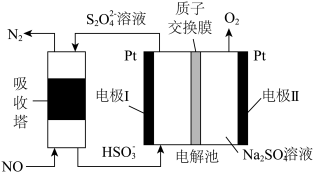
 (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为
您最近一年使用:0次
名校
5 . 煤炭是一种重要的化石能源,煤经过气化、水气变换等步骤得到合成气 、CO、
、CO、 的技术是当前研究的热点。涉及的反应如下:
的技术是当前研究的热点。涉及的反应如下:
(1)“煤经过气化”涉及反应: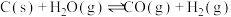
 ,通常该步骤中需要通入适量氧气与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的主要作用:
,通常该步骤中需要通入适量氧气与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的主要作用:___________ 。
(2)“水气变换”涉及如下反应:
反应Ⅰ:

反应Ⅱ:
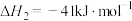
反应Ⅲ:

①
___________  。
。
②在某密闭容器中通入一定量的CO和 ,某纳米氟化物可用于制作光电材料对该反应进行催化,其晶胞结构如图。该晶体类型是
,某纳米氟化物可用于制作光电材料对该反应进行催化,其晶胞结构如图。该晶体类型是___________ ,该化合物的化学式为___________ 。 的平衡转化率,除改变温度外,还可以采取哪些措施
的平衡转化率,除改变温度外,还可以采取哪些措施___________ 。
④恒温恒容条件下,起始时CO和 的浓度分别为a
的浓度分别为a 和b
和b ,达平衡时
,达平衡时 和
和 的浓度分别为c
的浓度分别为c 和d
和d 。
。
i.达平衡时, 的浓度是
的浓度是___________  。
。
ii.反应Ⅰ的平衡常数K是___________ 。(用a、b、c、d表示)
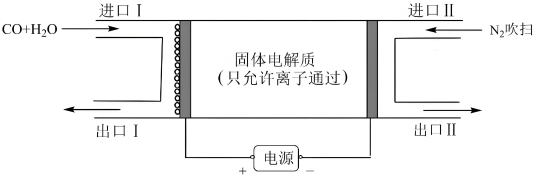
(3)“水气变换”中反应Ⅱ也可采用电化学方法实现,反应装置如图所示。___________ 。
 、CO、
、CO、 的技术是当前研究的热点。涉及的反应如下:
的技术是当前研究的热点。涉及的反应如下:(1)“煤经过气化”涉及反应:
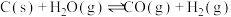
 ,通常该步骤中需要通入适量氧气与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的主要作用:
,通常该步骤中需要通入适量氧气与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的主要作用:(2)“水气变换”涉及如下反应:
反应Ⅰ:


反应Ⅱ:

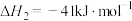
反应Ⅲ:


①

 。
。②在某密闭容器中通入一定量的CO和
 ,某纳米氟化物可用于制作光电材料对该反应进行催化,其晶胞结构如图。该晶体类型是
,某纳米氟化物可用于制作光电材料对该反应进行催化,其晶胞结构如图。该晶体类型是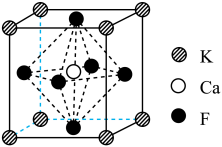
 的平衡转化率,除改变温度外,还可以采取哪些措施
的平衡转化率,除改变温度外,还可以采取哪些措施④恒温恒容条件下,起始时CO和
 的浓度分别为a
的浓度分别为a 和b
和b ,达平衡时
,达平衡时 和
和 的浓度分别为c
的浓度分别为c 和d
和d 。
。i.达平衡时,
 的浓度是
的浓度是 。
。ii.反应Ⅰ的平衡常数K是
(3)“水气变换”中反应Ⅱ也可采用电化学方法实现,反应装置如图所示。
您最近一年使用:0次
6 . 随着大气中 浓度增大带来了一系列环境问题,“负碳”技术开始备受各国关注,所谓“负碳”技术就是将
浓度增大带来了一系列环境问题,“负碳”技术开始备受各国关注,所谓“负碳”技术就是将 转化成甲醇、甲酸等可利用的资源的一系列技术。回答下列问题:
转化成甲醇、甲酸等可利用的资源的一系列技术。回答下列问题:
I. 催化加氢制甲醇
催化加氢制甲醇
以 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:
反应i:
 ;
;
反应ii:
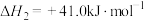 ;
;
反应iii:
 。
。
(1)反应i的
___________ 。
(2)一定温度和催化剂条件下,0.73mol 、0.24mol
、0.24mol 和0.03mol
和0.03mol (已知
(已知 不参与反应)在密闭容器中进行上述反应,平衡时
不参与反应)在密闭容器中进行上述反应,平衡时 的转化率、
的转化率、 和CO的选择性随温度的变化曲线如图。
和CO的选择性随温度的变化曲线如图。___________ (填“ ”“
”“ ”或“CO”)的变化。
”或“CO”)的变化。
②上述反应体系在一定条件下建立平衡后,下列说法错误的有___________ (填字母)。
A.降低温度,反应i~iii的正、逆反应速率都减小
B.恒压条件下,向容器中再通入少量 ,
, 的平衡转化率下降
的平衡转化率下降
C.移去部分 ,反应iii平衡不移动
,反应iii平衡不移动
D.选择合适的催化剂能减小反应iii的焓变
③某温度下(大于180℃), min反应到达平衡,测得容器中
min反应到达平衡,测得容器中 的体积分数为12.5%,容器内气体总压强为8.0MPa.此时用
的体积分数为12.5%,容器内气体总压强为8.0MPa.此时用 的分压表示
的分压表示 时间内的反应速率
时间内的反应速率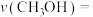
___________  ,此时
,此时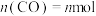 ,不发生反应iii,计算该温度下反应ii的压强平衡常数
,不发生反应iii,计算该温度下反应ii的压强平衡常数
___________ (用含有n的代数式表示,分压=总压×该组分物质的量分数)。
(3)科学家发现了一类金属卤化物钙钛矿材料有着出众的光电性质,有望在“负碳”技术上大放异彩,如图是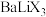 晶胞结构,晶胞参数为:apm,
晶胞结构,晶胞参数为:apm, 与
与 之间最短距离为
之间最短距离为___________ pm,若卤素X中 与
与 的比例为
的比例为 ,晶体密度为
,晶体密度为___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 浓度增大带来了一系列环境问题,“负碳”技术开始备受各国关注,所谓“负碳”技术就是将
浓度增大带来了一系列环境问题,“负碳”技术开始备受各国关注,所谓“负碳”技术就是将 转化成甲醇、甲酸等可利用的资源的一系列技术。回答下列问题:
转化成甲醇、甲酸等可利用的资源的一系列技术。回答下列问题:I.
 催化加氢制甲醇
催化加氢制甲醇以
 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:反应i:

 ;
;反应ii:

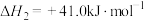 ;
;反应iii:

 。
。(1)反应i的

(2)一定温度和催化剂条件下,0.73mol
 、0.24mol
、0.24mol 和0.03mol
和0.03mol (已知
(已知 不参与反应)在密闭容器中进行上述反应,平衡时
不参与反应)在密闭容器中进行上述反应,平衡时 的转化率、
的转化率、 和CO的选择性随温度的变化曲线如图。
和CO的选择性随温度的变化曲线如图。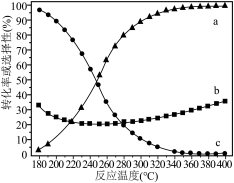
 ”“
”“ ”或“CO”)的变化。
”或“CO”)的变化。②上述反应体系在一定条件下建立平衡后,下列说法错误的有
A.降低温度,反应i~iii的正、逆反应速率都减小
B.恒压条件下,向容器中再通入少量
 ,
, 的平衡转化率下降
的平衡转化率下降C.移去部分
 ,反应iii平衡不移动
,反应iii平衡不移动D.选择合适的催化剂能减小反应iii的焓变
③某温度下(大于180℃),
 min反应到达平衡,测得容器中
min反应到达平衡,测得容器中 的体积分数为12.5%,容器内气体总压强为8.0MPa.此时用
的体积分数为12.5%,容器内气体总压强为8.0MPa.此时用 的分压表示
的分压表示 时间内的反应速率
时间内的反应速率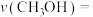
 ,此时
,此时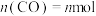 ,不发生反应iii,计算该温度下反应ii的压强平衡常数
,不发生反应iii,计算该温度下反应ii的压强平衡常数
(3)科学家发现了一类金属卤化物钙钛矿材料有着出众的光电性质,有望在“负碳”技术上大放异彩,如图是
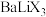 晶胞结构,晶胞参数为:apm,
晶胞结构,晶胞参数为:apm, 与
与 之间最短距离为
之间最短距离为 与
与 的比例为
的比例为 ,晶体密度为
,晶体密度为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。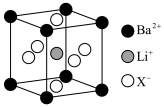
您最近一年使用:0次
7 . 烟气脱硝技术是环境科学研究的热点。实验室模拟臭氧深度氧化锅炉废气中的NO为 并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有:
并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有: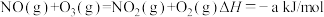
ii.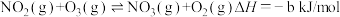
iii.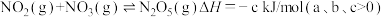
(1)NO被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:
___________ kJ/mol。
(2)80℃、NO初始浓度为200ppm,不同反应时间时深度氧化器中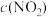 随
随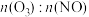 的变化如图所示(反应过程中检测到
的变化如图所示(反应过程中检测到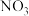 浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是
浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是_______ 。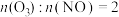 时,不同温度下
时,不同温度下 的浓度随时间变化曲线。
的浓度随时间变化曲线。 浓度不同的原因
浓度不同的原因___________ 。
②结合下图分析,100℃时2s后图中 浓度逐渐下降的可能原因
浓度逐渐下降的可能原因___________ 。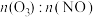 较高时,导致烟气中剩余
较高时,导致烟气中剩余 造成资源浪费和设备腐蚀,综合以上实验数据,常压下,
造成资源浪费和设备腐蚀,综合以上实验数据,常压下, 深度氧化NO的条件应选择
深度氧化NO的条件应选择___________ (填字母)。
A.80℃ B.100℃ C.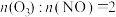 D.
D.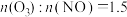
该条件下,烟气中含氮量达到排放标准所需深度氧化时间仍较长,提出解决这一问题可采取的措施及目的___________ 。
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。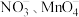 的还原产物分别是NO、
的还原产物分别是NO、 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为_________ mol/L。
 并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有:
并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有: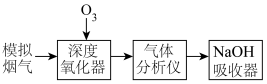
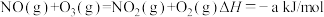
ii.
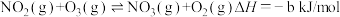
iii.
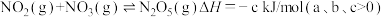
(1)NO被
 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:
(2)80℃、NO初始浓度为200ppm,不同反应时间时深度氧化器中
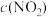 随
随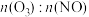 的变化如图所示(反应过程中检测到
的变化如图所示(反应过程中检测到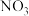 浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是
浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是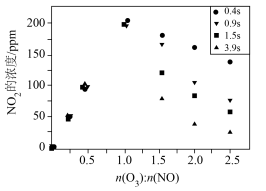
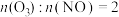 时,不同温度下
时,不同温度下 的浓度随时间变化曲线。
的浓度随时间变化曲线。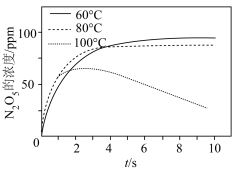
 浓度不同的原因
浓度不同的原因②结合下图分析,100℃时2s后图中
 浓度逐渐下降的可能原因
浓度逐渐下降的可能原因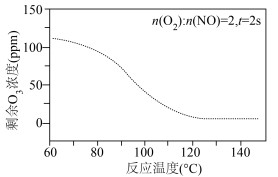
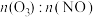 较高时,导致烟气中剩余
较高时,导致烟气中剩余 造成资源浪费和设备腐蚀,综合以上实验数据,常压下,
造成资源浪费和设备腐蚀,综合以上实验数据,常压下, 深度氧化NO的条件应选择
深度氧化NO的条件应选择A.80℃ B.100℃ C.
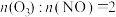 D.
D.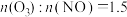
该条件下,烟气中含氮量达到排放标准所需深度氧化时间仍较长,提出解决这一问题可采取的措施及目的
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。
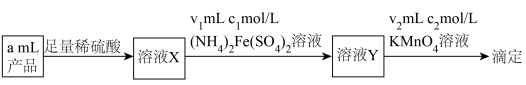
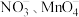 的还原产物分别是NO、
的还原产物分别是NO、 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
8 . 甲烷是重要的化石燃料,用途广泛。一定量的 在恒容密闭容器中发生反应:
在恒容密闭容器中发生反应:
 。平衡体系中各气体体积分数与温度的关系如图所示:
。平衡体系中各气体体积分数与温度的关系如图所示:
(1)已知甲烷、碳、氢气的燃烧热分别为890.31 、395.00
、395.00 、285.80
、285.80 ,则上述反应的反应热
,则上述反应的反应热 =
=___________  。
。
(2)下列不能说明反应达到平衡状态的是___________ (填字母)。
a.混合气体的密度不变 b.气体总压强不再变化
c.每消耗1mol 的同时有2mol
的同时有2mol 生成 d.碳的质量不再改变
生成 d.碳的质量不再改变
(3) ℃时,若在平衡体系中充入惰性气体,此时反应速率
℃时,若在平衡体系中充入惰性气体,此时反应速率___________ (填“变大”“变小”或“不变”),且
___________ (填“>”“<”或“=”) 。
。
(4) ℃时,若在平衡体系中充入等体积的
℃时,若在平衡体系中充入等体积的 和
和 则平衡
则平衡___________ (填“正向”“逆向”或“不”)移动其理由是___________ 。
(5) ℃时,反应达平衡后
℃时,反应达平衡后 的转化率为
的转化率为_________ (保留3位有效数字)。若平衡体系的总压强为xkPa, ℃时该反应的平衡常数
℃时该反应的平衡常数
________ kPa(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
 在恒容密闭容器中发生反应:
在恒容密闭容器中发生反应:
 。平衡体系中各气体体积分数与温度的关系如图所示:
。平衡体系中各气体体积分数与温度的关系如图所示: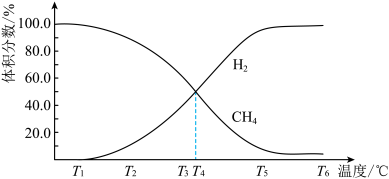
(1)已知甲烷、碳、氢气的燃烧热分别为890.31
 、395.00
、395.00 、285.80
、285.80 ,则上述反应的反应热
,则上述反应的反应热 =
= 。
。(2)下列不能说明反应达到平衡状态的是
a.混合气体的密度不变 b.气体总压强不再变化
c.每消耗1mol
 的同时有2mol
的同时有2mol 生成 d.碳的质量不再改变
生成 d.碳的质量不再改变(3)
 ℃时,若在平衡体系中充入惰性气体,此时反应速率
℃时,若在平衡体系中充入惰性气体,此时反应速率
 。
。(4)
 ℃时,若在平衡体系中充入等体积的
℃时,若在平衡体系中充入等体积的 和
和 则平衡
则平衡(5)
 ℃时,反应达平衡后
℃时,反应达平衡后 的转化率为
的转化率为 ℃时该反应的平衡常数
℃时该反应的平衡常数
您最近一年使用:0次
名校
解题方法
9 . 填空题
(1)下表是部分化学键的键能参数:
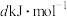 ,白磷及其完全燃烧的产物的结构如图所示,则表中
,白磷及其完全燃烧的产物的结构如图所示,则表中
________ kJ·mol-1(用含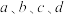 的代数式表示)
的代数式表示)
(2)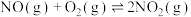 的反应机理和各基元反应的活化能为:
的反应机理和各基元反应的活化能为:
①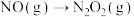
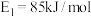
②
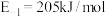
③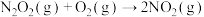
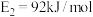
④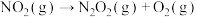
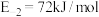
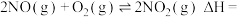
________ 。
(3)已知在 和
和 条件下,有如下反应:①
条件下,有如下反应:①
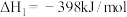
②
 ,若反应
,若反应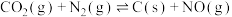 的活化能为
的活化能为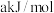 ,则反应
,则反应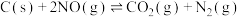 的活化能为
的活化能为________ 。
(4)已知充分燃烧乙炔 气体时,生成
气体时,生成 二氧化碳气体并生成液态水,放出热量
二氧化碳气体并生成液态水,放出热量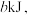 表示乙炔燃烧热的热化学方程式为
表示乙炔燃烧热的热化学方程式为____________________ 。
(5)I.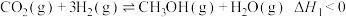
II.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2>0
由实验测得该反应II的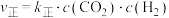 ,
, ,Arrhenius经验公式为
,Arrhenius经验公式为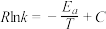 ,其中为
,其中为 活化能,
活化能, 为热力学温度,
为热力学温度, 、
、 、
、 为速率常数,
为速率常数, 和
和 为常数。则
为常数。则
________  (用含
(用含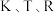 的代数式表示)。
的代数式表示)。
(1)下表是部分化学键的键能参数:
化学键 |
|
|
|
|
键能 |
|
|
|
|
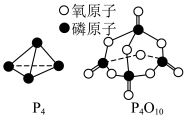
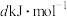 ,白磷及其完全燃烧的产物的结构如图所示,则表中
,白磷及其完全燃烧的产物的结构如图所示,则表中
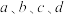 的代数式表示)
的代数式表示)(2)
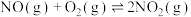 的反应机理和各基元反应的活化能为:
的反应机理和各基元反应的活化能为:①
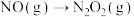
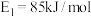
②

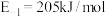
③
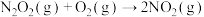
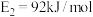
④
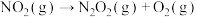
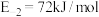
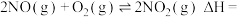
(3)已知在
 和
和 条件下,有如下反应:①
条件下,有如下反应:①
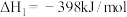
②

 ,若反应
,若反应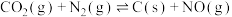 的活化能为
的活化能为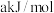 ,则反应
,则反应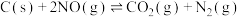 的活化能为
的活化能为(4)已知充分燃烧乙炔
 气体时,生成
气体时,生成 二氧化碳气体并生成液态水,放出热量
二氧化碳气体并生成液态水,放出热量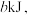 表示乙炔燃烧热的热化学方程式为
表示乙炔燃烧热的热化学方程式为(5)I.
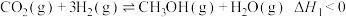
II.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2>0
由实验测得该反应II的
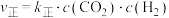 ,
, ,Arrhenius经验公式为
,Arrhenius经验公式为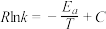 ,其中为
,其中为 活化能,
活化能, 为热力学温度,
为热力学温度, 、
、 、
、 为速率常数,
为速率常数, 和
和 为常数。则
为常数。则
 (用含
(用含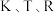 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
10 . 利用CH4与CO2进行催化重整,对温室气体的减排具有重要意义,催化重整时发生的反应: ,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
(1)已知: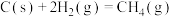
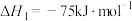

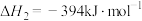
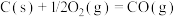
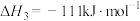
催化重整反应 的
的
______  。
。
(2)某温度下,向1 L的密闭容器中充入0.2 mol CH4与0.2 mol CO2,发生 催化重整反应,
催化重整反应, ;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为
;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为______ ;用H2表示的反应速率为______  。
。
(3)已知:常温下CH3COOH的电离常数 。常温下,在三元弱酸H3R的水溶液中H3R、
。常温下,在三元弱酸H3R的水溶液中H3R、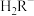 、
、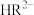 、
、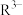 的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为:
的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为: 、
、 、
、 。则:Na2HR溶液显
。则:Na2HR溶液显______ 性(选填“酸”或“碱”或“中”),常温下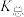 的数量级为
的数量级为______ 。 (
( 、
、 、
、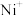 等)与O3反应可得
等)与O3反应可得 。
。 与CH4反应能高选择性地生成甲醇。总反应为:
与CH4反应能高选择性地生成甲醇。总反应为: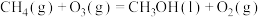 ;
;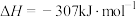 。分别在300K和310K下(其他反应条件相同)进行反应
。分别在300K和310K下(其他反应条件相同)进行反应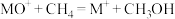 ,结果如下图(见下图1)所示。图中300K的曲线是
,结果如下图(见下图1)所示。图中300K的曲线是______ (填“a”或“b”)。300K、60 s时 的转化率为
的转化率为______ (列出算式)。 、
、 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(见上图2)(
关系图(见上图2)(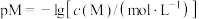 ;
; 可认为
可认为 离子沉淀完全)。则:
离子沉淀完全)。则:
______ 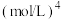 。
。
 ,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:(1)已知:
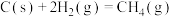
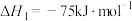

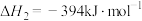
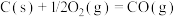
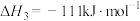
催化重整反应
 的
的
 。
。(2)某温度下,向1 L的密闭容器中充入0.2 mol CH4与0.2 mol CO2,发生
 催化重整反应,
催化重整反应, ;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为
;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为 。
。(3)已知:常温下CH3COOH的电离常数
 。常温下,在三元弱酸H3R的水溶液中H3R、
。常温下,在三元弱酸H3R的水溶液中H3R、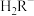 、
、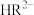 、
、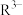 的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为:
的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为: 、
、 、
、 。则:Na2HR溶液显
。则:Na2HR溶液显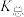 的数量级为
的数量级为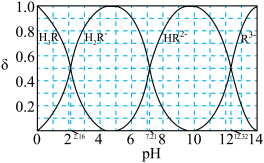
 (
( 、
、 、
、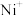 等)与O3反应可得
等)与O3反应可得 。
。 与CH4反应能高选择性地生成甲醇。总反应为:
与CH4反应能高选择性地生成甲醇。总反应为: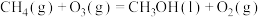 ;
;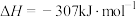 。分别在300K和310K下(其他反应条件相同)进行反应
。分别在300K和310K下(其他反应条件相同)进行反应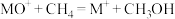 ,结果如下图(见下图1)所示。图中300K的曲线是
,结果如下图(见下图1)所示。图中300K的曲线是 的转化率为
的转化率为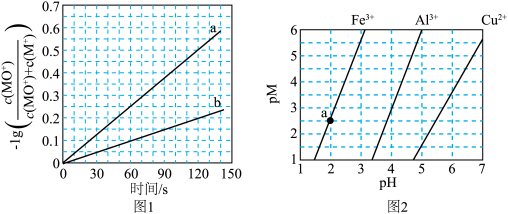
 、
、 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(见上图2)(
关系图(见上图2)(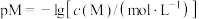 ;
; 可认为
可认为 离子沉淀完全)。则:
离子沉淀完全)。则:
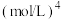 。
。
您最近一年使用:0次