解题方法
1 . 按要求回答下列问题:
(1)Fe元素在周期表中的位置为___________ ,基态Cu原子价层电子轨道式为___________ 。
(2)氯化铵溶液可以用来除铁锈,请用离子方程式 解释原因___________ 。
(3)向 沉淀中加入足量
沉淀中加入足量 溶液,固体由白色逐渐变为黄色,请写出该过程的
溶液,固体由白色逐渐变为黄色,请写出该过程的离子方程式 ___________ 。
(4)①已知25℃和 时,液态甲醇(
时,液态甲醇( )的燃烧热
)的燃烧热 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式___________ 。
②根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是___________ 。
(1)Fe元素在周期表中的位置为
(2)氯化铵溶液可以用来除铁锈,请用
(3)向
 沉淀中加入足量
沉淀中加入足量 溶液,固体由白色逐渐变为黄色,请写出该过程的
溶液,固体由白色逐渐变为黄色,请写出该过程的(4)①已知25℃和
 时,液态甲醇(
时,液态甲醇( )的燃烧热
)的燃烧热 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式②根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是
您最近一年使用:0次
名校
2 . 请分析如下电化学装置,回答下列问题:
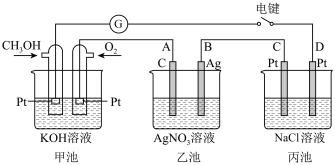
(1)甲池为___________ (填“原电池”“电解池”或“电镀池”),通入 电极的电极反应式为
电极的电极反应式为___________ 。
(2)当甲池中消耗 为2.24L(标准状况下)时,理论上乙池中B极质量增加
为2.24L(标准状况下)时,理论上乙池中B极质量增加___________ g。
(3)丙池溶液体积为300mL,写出其总反应的化学方程式___________ ;为了防止丙池中两极产物相互反应,实际生产中在两极之间设有___________ 离子交换膜(填“阴”或“阳”或“质子”)。电解一段时间后,当溶液的pH为13时,消耗 的质量为
的质量为___________ g(忽略溶液体积变化,不考虑损耗)。
(4)甲醇的燃烧热为725.76KJ/mol,写出甲醇燃烧热的热化学方程式___________ 。

(1)甲池为
 电极的电极反应式为
电极的电极反应式为(2)当甲池中消耗
 为2.24L(标准状况下)时,理论上乙池中B极质量增加
为2.24L(标准状况下)时,理论上乙池中B极质量增加(3)丙池溶液体积为300mL,写出其总反应的化学方程式
 的质量为
的质量为(4)甲醇的燃烧热为725.76KJ/mol,写出甲醇燃烧热的热化学方程式
您最近一年使用:0次
名校
解题方法
3 . 已知反应:①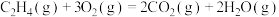

②
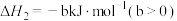
其他数据如表所示,下列说法正确的是
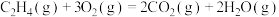

②

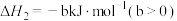
其他数据如表所示,下列说法正确的是
| 化学键 |  |  |  |  |  |
键能/ | 798 |  | 413 | 463 | 615 |
A.乙烯的燃烧热为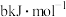 |
B.上表中的x用a的代数式表示为 |
C.当有 个C—H键断裂时,反应②放出热量一定为bkJ 个C—H键断裂时,反应②放出热量一定为bkJ |
D.反应 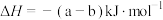 |
您最近一年使用:0次
4 . 已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l)  =-890kJ/mol
=-890kJ/mol
CO(g)+1/2O2(g)=CO2(g) =-282.5kJ/mol。
=-282.5kJ/mol。
假如标准状况下由CH4、CO、CO2组成的89.6升混和气体完全燃烧时能放出1010千焦的热量,并生成18克液态水,那么燃烧前混和气体中CO占的体积百分含量约为
 =-890kJ/mol
=-890kJ/molCO(g)+1/2O2(g)=CO2(g)
 =-282.5kJ/mol。
=-282.5kJ/mol。假如标准状况下由CH4、CO、CO2组成的89.6升混和气体完全燃烧时能放出1010千焦的热量,并生成18克液态水,那么燃烧前混和气体中CO占的体积百分含量约为
| A.40% | B.50% | C.60% | D.70% |
您最近一年使用:0次
名校
解题方法
5 . 下列涉及的方程式表示正确的是
A.亚硫酸氢钠溶液呈酸性的主要原因: |
B.铅酸电池的正极在充电时的电极反应式: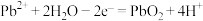 |
C. 的燃烧热为 的燃烧热为 ,则 ,则 燃烧的热化学方程式为: 燃烧的热化学方程式为: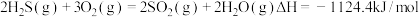 |
D. 溶液与足量的 溶液与足量的 溶液反应: 溶液反应: |
您最近一年使用:0次
名校
解题方法
6 . 下列叙述正确的是
A. 的燃烧热为 的燃烧热为 ,则 ,则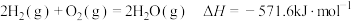 |
B. ,则 ,则 和 和 充分反应放热 充分反应放热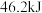 |
C.反应 的 的 且 且 ,该反应在较低温度下可自发反应 ,该反应在较低温度下可自发反应 |
D. ,改变条件使 ,改变条件使 浓度增大时,平衡一定发生移动 浓度增大时,平衡一定发生移动 |
您最近一年使用:0次
2024-02-27更新
|
76次组卷
|
2卷引用:河北省唐山市2023-2024学年高二上学期期末考试化学试题
解题方法
7 . Ⅰ.已知下列热化学方程式:①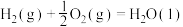
 kJ/mol,
kJ/mol,
②
 kJ/mol,
kJ/mol,
③
 kJ/mol,
kJ/mol,
④
 kJ/mol,回答下列问题:
kJ/mol,回答下列问题:
(1)C燃烧热的热化学方程式为___________ ;(填序号)
(2)燃烧1 g 生成气态水,放出的热量为
生成气态水,放出的热量为___________ 。
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为
 kJ/mol。
kJ/mol。
(3)下列各组试剂混合发生反应的离子方程式为 的是
的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1mol ,则反应放出的热量
,则反应放出的热量___________ (填“大于”“等于”或“小于”)57.3kJ。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热
___________ 0。
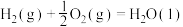
 kJ/mol,
kJ/mol,②

 kJ/mol,
kJ/mol,③

 kJ/mol,
kJ/mol,④

 kJ/mol,回答下列问题:
kJ/mol,回答下列问题:(1)C燃烧热的热化学方程式为
(2)燃烧1 g
 生成气态水,放出的热量为
生成气态水,放出的热量为Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为

 kJ/mol。
kJ/mol。(3)下列各组试剂混合发生反应的离子方程式为
 的是
的是A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1mol
 ,则反应放出的热量
,则反应放出的热量Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能

您最近一年使用:0次
名校
8 . 下列能正确表示甲醇燃烧热的热化学方程式的是
A.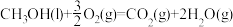  |
B.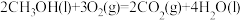 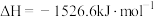 |
C.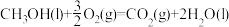  |
D.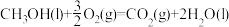 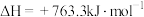 |
您最近一年使用:0次
2024-02-25更新
|
154次组卷
|
2卷引用:湖南省长沙市弘益高级中学2022-2023学年高一下学期期末考试化学试题
名校
9 . 完成下列问题
(1)已知:①

②

则

___________ 。
(2)已知:①

②

则表示氨气燃烧热的热化学方程式为___________ ,该反应可设计为碱性条件下的燃料电池,负极电极反应式为___________ 。
(3)已知几种化学键的键能和热化学方程式如下:

 ,则a=
,则a=___________ 。
(4)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是
)的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是___________ ;反应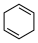 (l)=
(l)=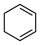 (l)的
(l)的
___________ 。

(1)已知:①


②


则


(2)已知:①


②


则表示氨气燃烧热的热化学方程式为
(3)已知几种化学键的键能和热化学方程式如下:
| 化学键 |  |  |  |  |  |
键能/( ) ) | 391 | 193 | 243 | a | 432 |

 ,则a=
,则a=(4)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(
 )的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是
)的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是 (l)=
(l)= (l)的
(l)的

您最近一年使用:0次
名校
10 . 氨气的燃烧热316.25kJ·mol-1.肼(N2H4)为无色油状液体,有类似于氨的刺鼻气味,是一种强极性化合物。下列说法正确的是
| A.氨气燃烧的热化学方程式:4NH3(g)+3O2(g)=6H2O(g)+2N2(g) ΔH=-1265kJ·mol-1 |
B.HNO2与KMnO4酸性溶液反应:5 +2 +2 +6H+=5 +6H+=5 +2Mn2++3H2O +2Mn2++3H2O |
| C.肼(N2H4)—空气碱性燃料电池的负极反应:N2H4+4e-=4H++N2↑ |
| D.氢氧化铜溶于氨水的化学方程式:Cu(OH)2+4NH3=[Cu(NH3)4](OH)2 |
您最近一年使用:0次



