1 . 已知反应:
①C(s)+1/2O2(g)=CO(g) ΔH1=-110.5kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3kJ/mol
下列结论正确的是( )
①C(s)+1/2O2(g)=CO(g) ΔH1=-110.5kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3kJ/mol
下列结论正确的是( )
| A.若碳的燃烧热用ΔH3来表示,则ΔH3<ΔH1 |
| B.H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3) kJ·mol-1 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.稀醋酸与稀NaOH溶液反应生成 1mol水,放出的热量小于57.3kJ |
您最近一年使用:0次
2 . 物质燃烧的条件是
| A.与大量空气接触 | B.与空气接触 |
| C.与空气的接触面要大 | D.温度要达到可燃物的着火点 |
您最近一年使用:0次
2020-02-12更新
|
134次组卷
|
2卷引用:人教版 高中化学 必修2 第二章 《化学反应与能量》 单元能力检测
3 . 欲使煤在煤炉中充分燃烧,下列措施可行的是
| A.向炉内喷吹空气 | B.把大块状煤碾成粉末 |
| C.使用MnO2做催化剂 | D.提高炉内体系的温度 |
您最近一年使用:0次
名校
4 . 下列说法正确的是( )
| A.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是放热反应 |
| B.在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C.物质燃烧都需要氧气 |
| D.物质燃烧放出热量的多少与外界条件有关 |
您最近一年使用:0次
名校
5 . 已知取H2(g)+2ICl(g)=I2(g)+2HCl(g),该反应分①②两步进行,其能量曲线如图所示,下列有关说法正确的是( )
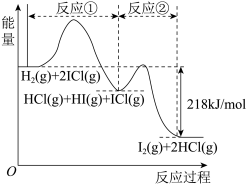

| A.反应①为吸热反应 |
| B.反应①和②均是同种元素间发生的氧化还原反应 |
| C.反应①比反应②的速率慢,与相应正反应的活化能有关 |
| D.H2(g) +2ICl(g)=I2(g)+2HCl(g) △H=-218kJ/mol |
您最近一年使用:0次
2019-12-15更新
|
181次组卷
|
3卷引用:湖南省长沙市雅礼中学2018-2019高二12月月考化学试题
解题方法
6 . 下列描述中正确的是
| A.反应2H2(g)+O2(g) =2H2O(g)的ΔH可通过下式估算: ∆H=反应中断裂旧共价键的键能之和-反应中形成新共价键的键能之和 |
| B.在25 ℃、101 kPa时,1 mol碳燃烧所放出的热量为碳的标准燃烧热 |
| C.从C(石墨,s) = C(金刚石,s) ΔH=+1.9 kJ·mol-1,可知石墨比金刚石更稳定 |
| D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次
2019-11-24更新
|
93次组卷
|
2卷引用:江苏省苏北县2019-2020学年高二上学期学情调研化学(选择考)试题
名校
7 . 已知: ①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1 ②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1下列说法正确的是
| A.常温常压时,燃烧1mol氢气放热为241.8 kJ |
| B.由①可知,1 mol CO(g)和1/2mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量 |
C.可用下图表示CO2(g)→CO(g)+ O2(g)反应是吸热反应 O2(g)反应是吸热反应 |
| D.生成1 mol H2O(g),其反应热为-241.8 kJ |
您最近一年使用:0次
10-11高三上·江苏盐城·期中
解题方法
8 . 一些烷烃的燃烧热如下表:
下列表达正确的是 
| 化合物 | 燃烧热/kJ·mol-1 | 化合物 | 燃烧热/kJ·mol-1 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 异戊烷 | 3531.3 |

| A.正戊烷的燃烧热大于3531.3kJ·mol-1 |
| B.稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)△H= -1560.8 kJ·mol-1 |
| D.相同物质的量的烷烃CnH2n+2,n越大,燃烧放出的热量越多 |
您最近一年使用:0次
9 . 下列热化学方程式书写正确的是(△H的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=" —1367.0kJ/mol" (△H代表乙醇的燃烧热) |
| B.HCl (aq)+NaOH(aq)=NaCl(aq)+H2O(1) △H=—57.3kJ/mol(△H代表中和热) |
| C.2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ/mol (反应热) |
| D.C(s)+O2(g)=CO2(g) ΔH=+393.5 kJ/mol (反应热) |
您最近一年使用:0次
2011高三·广东揭阳·学业考试
解题方法
10 . 下列依据热化学方程式得出的结论正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H = a、2C(s)+O2(g)=2CO(g);△H = b,则a>b |
| D.已知C (石墨,s)=C (金刚石,s)△H>0,则石墨比金刚石稳定 |
您最近一年使用:0次



